


《高中化学电解质 离子反应PPT课件下载》是由用户上传到老师板报网,本为文库资料,大小为443 KB,总共有22页,格式为ppt。授权方式为VIP用户下载,成为老师板报网VIP用户马上下载此课件。文件完整,下载后可编辑修改。
- 文库资料
- 22页
- 443 KB
- VIP模板
- ppt
- 数字产品不支持退货
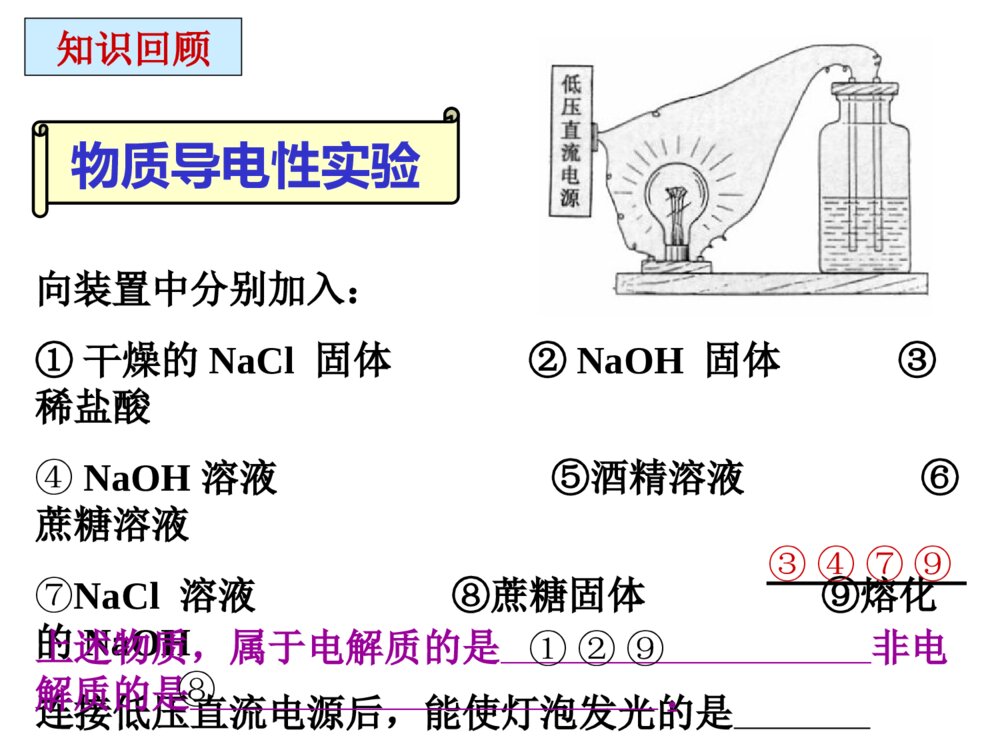
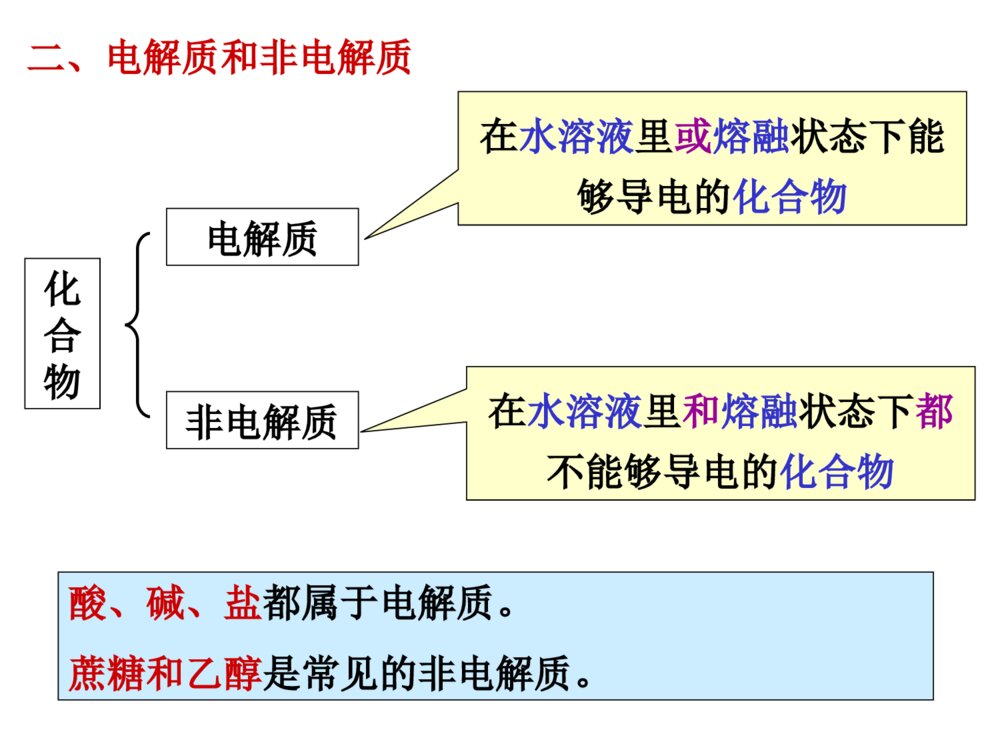
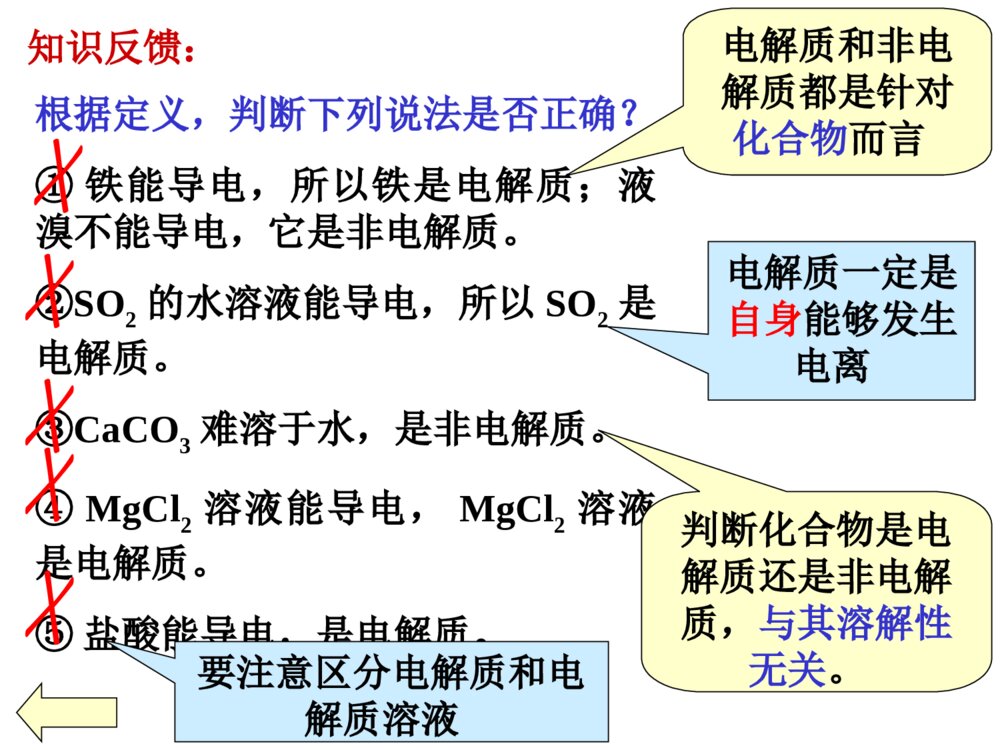
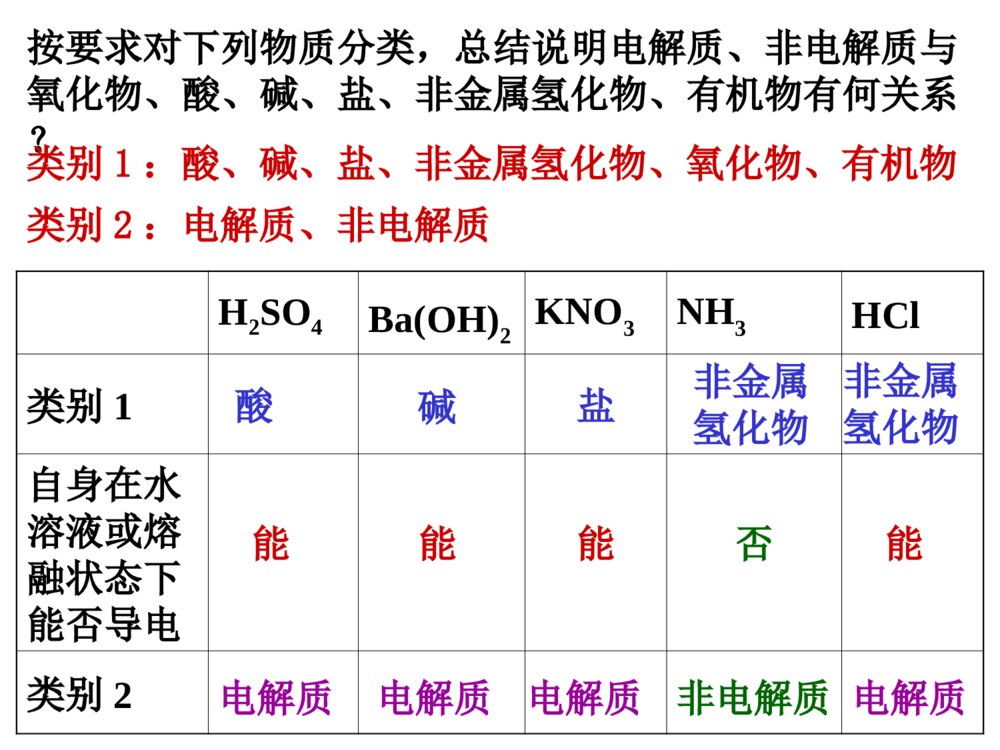
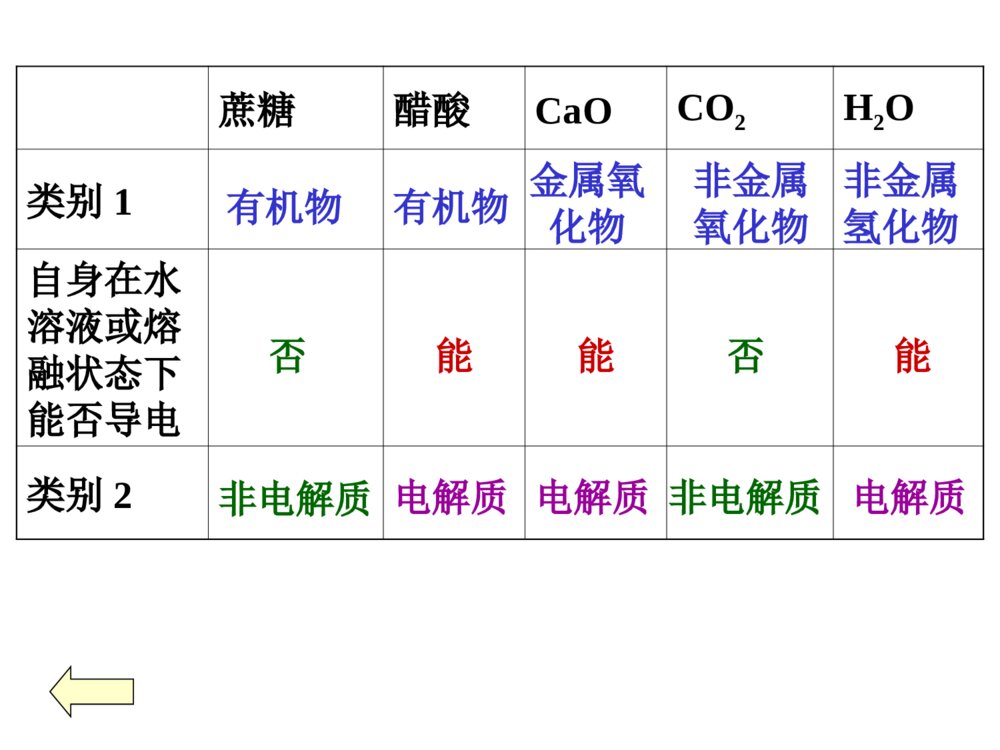
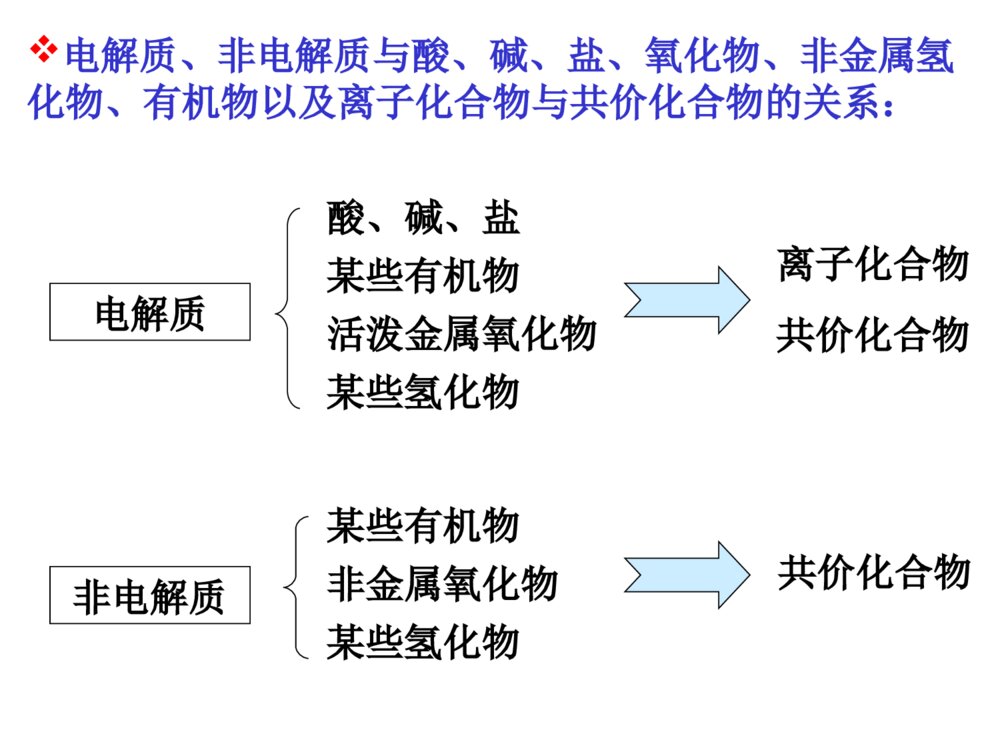
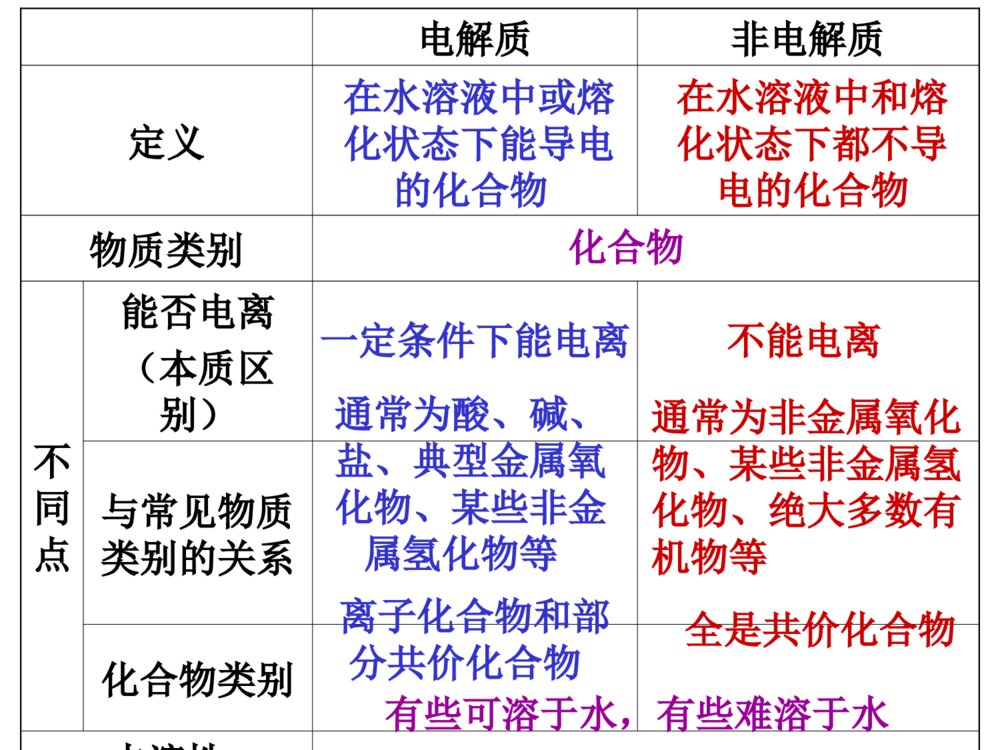
第2节电解质离子反应课程目标:1、掌握电解质、非电解质、强弱电解质的概念,2、会判断区分常见的电解质与非电解质、强电解质与弱电解质。3、理解电解质的电离过程和导电过程的实质。4、会书写强、弱电解质的电离方程式。一、电离1、定义:化合物溶解于水或受热熔化时,离解成能够自由移动的离子的过程。2、表示方式:用电离方程式表示。HCl======H++Cl-NaOH======Na++OH-NaCl======Na++Cl-向装置中分别加入:①干燥的NaCl固体②NaOH固体③稀盐酸④NaOH溶液⑤酒精溶液⑥蔗糖溶液⑦NaCl溶液⑧蔗糖固体⑨熔化的NaOH连接低压直流电源后,能使灯泡发光的是③④⑦⑨物质导电性实验知识回顾上述物质,属于电解质的是非电解质的是.①②⑨⑧二、电解质和非电解质化合物电解质非电解质在水溶液里或熔融状态下能够导电的化合物在水溶液里和熔融状态下都不能够导电的化合物酸、碱、盐都属于电解质。蔗糖和乙醇是常见的非电解质。知识反馈:根据定义,判断下列说法是否正确?①铁能导电,所以铁是电解质;液溴不能导电,它是非电解质。②SO2的水溶液能导电,所以SO2是电解质。③CaCO3难溶于水,是非电解质。④MgCl2溶液能导电,MgCl2溶液是电解质。⑤盐酸能导电,是电解质。电解质和非电解质都是针对化合物而言电解质一定是自身能够发生电离判断化合物是电解质还是非电解质,与其溶解性无关。要注意区分电解质和电解质溶液按要求对下列物质分类,总结说明电解质、非电解质与氧化物、酸、碱、盐、非金属氢化物、有机物有何关系?H2SO4KNO3NH3HCl类别1自身在水溶液或熔融状态下能否导电类别2类别1:酸、碱、盐、非金属氢化物、氧化物、有机物类别2:电解质、非电解质Ba(OH)2酸碱盐非金属氢化物非金属氢化物电解质电解质电解质电解质非电解质能能能能否蔗糖醋酸CaOCO2H2O类别1自身在水溶液或熔融状态下能否导电类别2非金属氧化物有机物有机物非金属氢化物金属氧化物非电解质电解质电解质电解质非电解质能能能否否电解质、非电解质与酸、碱、盐、氧化物、非金属氢化物、有机物以及离子化合物与共价化合物的关系:酸、碱、盐某些有机物活泼金属氧化物某些氢化物电解质某些有机物非金属氧化物某些氢化物非电解质离子化合物共价化合物共价化合物电解质非电解质定义物质类别不同点能否电离(本质区别)与常见物质类别的关系化合物类别水溶性在水溶液中或熔化状态下能导电的化合物在水溶液中和熔化状态下都不导电的化合物化合物有些可溶于水,有些难溶于水一定条件下能电离不能电离通常为酸、碱、盐、典型金属氧化物、某些非金属氢化物等通常为非金属氧化物、某些非金属氢化物、绝大多数有机物等离子化合物和部分共价化合物全是共价化合物1、下列物质:①Cu②SO2③NH3④NaCl溶液⑤NaOH⑥HCl气体⑦酒精⑧AgCl属于电解质的是()属于非电解质的是()A.⑤⑥⑧B.①④⑦C.②③⑦D.④⑤⑥课堂检测1AC思考:醋酸、盐酸都是电解质溶液。在相同条件下,两种物质的导电能力相同吗?实验:体积相同条件下,0.1mol/L盐酸和醋酸溶液的导电性情况比较。弱电解质:在水溶液中只能部分电离的电解质。电解质强电解质:在水溶液里能完全电离的电解质HCl======H++Cl-CH3COOHH++CH3COO-溶液中,只存在H+和Cl-,不存在HCl分子溶液中,既存在H+和CH3COO-,也存在CH3COOH分子三、强电解质和弱电解质很稀的盐酸和比较浓的醋酸溶液,哪一个的导电性较强?电解质溶液导电能力取决于什么因素?与电解质的强弱有关吗?①电解质溶液导电能力的强弱只取决于在相同条件下(温度、外电压等)溶液中自由移动离子的浓度大小和离子所带电荷的多少②与电解质的强弱没有直接关系③弱电解质溶液的导电能力不一定弱(例较浓的醋酸溶液),强电解质溶液的导电能力不一定强(如很稀的盐酸)BaSO4、CaCO3是难溶于水的物质,他们是强电解质还是弱电解质?判断电解质强弱的关键是:看溶于水的部分是否完全电离,而不是看其溶解了多少。关注的是其电离程度,而不是其溶解性强电解质弱电解质水溶性电离程度溶液中的微粒电离过程实例完全电离部分电离阴、阳离子离子、电解质分子不可逆可逆强酸:H2SO4HCl强碱:NaOHBa(OH)2大多数盐:NaClAgNO3弱酸:H2SH2SO3CH3COOH弱碱:Al(OH)3NH3·H2O少数盐、水Pb(CH3COO)2★强弱电解质的区别有的可溶有的难溶有的可溶有的难溶1、在下列物质中:①CH3COOHHClFeH②③④2O⑤NaOHCO⑥2Na⑦2CO3⑧C2H5OH1.属于强电解质的是____________2.属于弱电解质的是____________3.属于非电解质的是____________4.既不属于电解质也不属于非电解质.②⑤⑦①④⑥⑧③课堂检测22、下列说法正确的是()A、强电解质溶液一定比弱电解质溶液的导电能力强B、强电解质都是离子化合物,而弱电解质都是共价化合物C、强电解质的水溶液中,不存在溶质的分子D、不同电解质溶液,只要物质的量浓度相同,导电能力就相同C综合练习1、实验表明,BaSO4在熔融状态下能够导电,其导电的实质原因是()A、是电解质B、存在离子C、存在电子D、存在自由移动的离子2、下列说法正确的是()A、NaCl溶液在电流作用下电离成Na+和Cl-B、固体硫酸钠不能导电,所以它是非电解质C、水难电离,纯水几乎不导电,所以水是非电解质D、蔗糖在水溶液或熔化时都不导电,它是非电解质DD5、强电解质和弱电解质的本质区别是()A、强电解质易溶于水,弱电解质难溶于水B、水溶液的导电能力不同C、水溶液里的电解质是否完全电离D、是离子化合物还是共价化合物3、下列物质的水溶液能导电,但属于非电解质的是()A、CH3COOHB、Cl2C、NaHCO3D、NH34、下列物质中,能导电又是强电解质的是()A、氯化钾溶液B、氨水C、熔融的硝酸钠D、氢氧化钡晶体DCC6、下列物质,①NaCl晶体②CO2③H2SO4溶液④石墨⑤H2SO3⑥熔融KCl⑦蔗糖⑧CaCO3固体⑨新制氯水1、能导电的是.2、属于强电解质的是.属于弱电解质的是.属于非电解质的是.3、水溶液能导电的是.4、水溶液中溶质全部以离子形式存在的是.③④⑥⑨①⑧⑥②⑦①②③⑤⑥⑧⑨①③⑥⑧⑤7、写出下列物质在水中的电离方程式H2SO4、CaCO3、NH3·H2O、Al(OH)3、NaHCO3、NaHSO4、H2CO3H2SO42H++SO42-(易溶强电解质)CaCO3Ca2++CO32-(难溶强电解质)NH3·H2ONH4++OH-(易溶弱电解质)Al(OH)3Al3++3OH-(难溶弱电解质)NaHCO3Na++HCO3-(弱酸酸式盐强电解质)NaHSO4Na++H++SO42-(强酸酸式盐强电解质)H2CO3H++HCO3-HCO3-H++CO32-多元弱电解质



















