



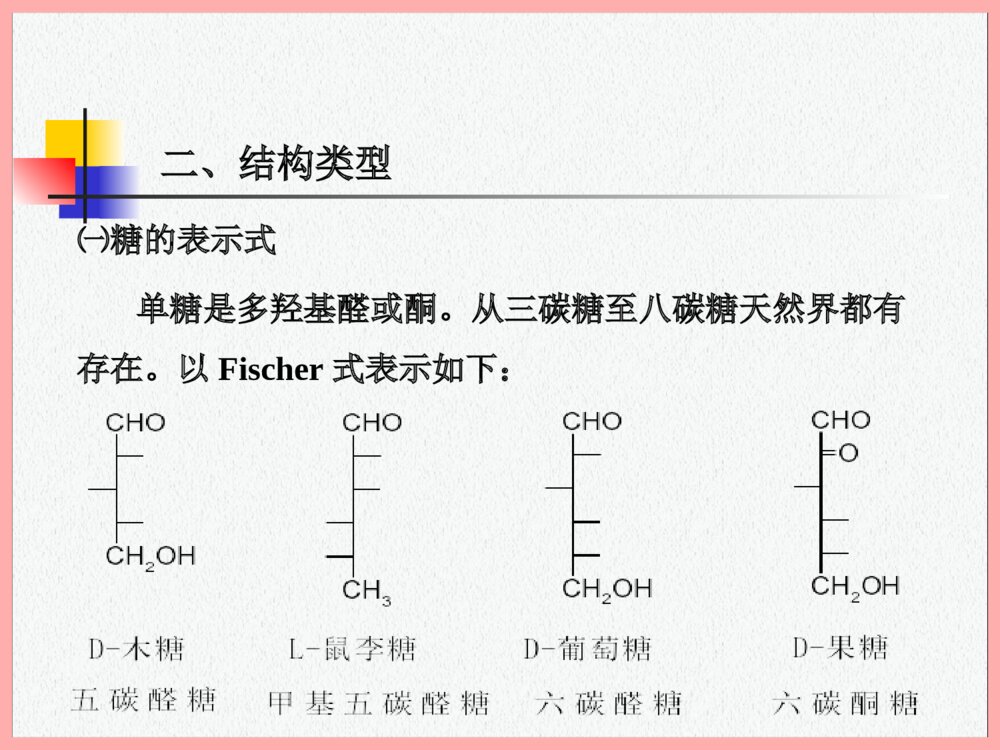
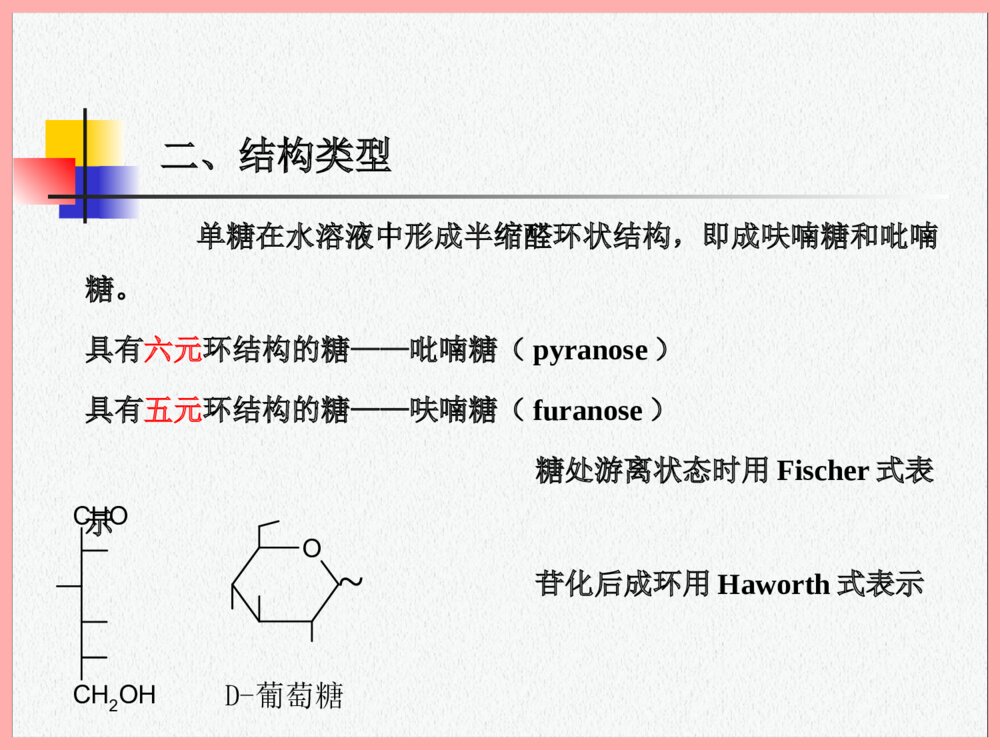
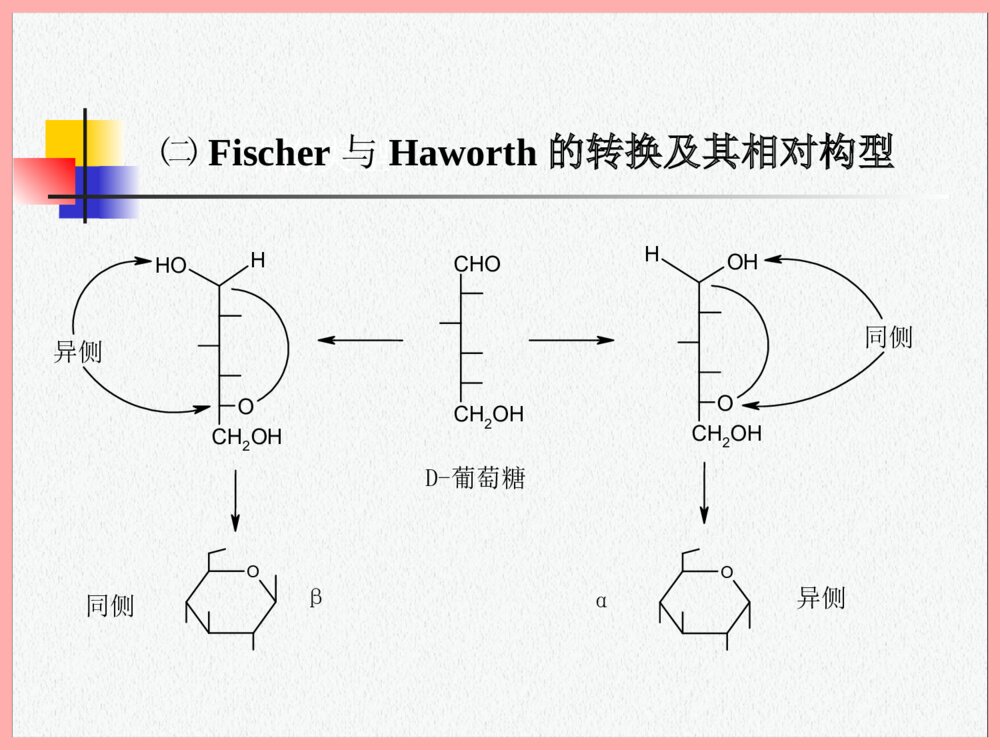



《天然药物化学《第二章 塘和苷》教学PPT课件下载》是由用户上传到老师板报网,本为文库资料,大小为1.27 MB,总共有103页,格式为ppt。授权方式为VIP用户下载,成为老师板报网VIP用户马上下载此课件。文件完整,下载后可编辑修改。
- 文库资料
- 103页
- 1.27 MB
- VIP模板
- ppt
- 数字产品不支持退货
第二章天然药物化学NatureMedicinalchemistry糖和苷武汉理工大学制药工程系Carbohy第二章糖和苷本章基本内容一、概述二、结构类型三、糖苷分类四、糖和苷的物理性质五、糖的化学性质六、苷键的裂解七、糖的提取分离八、糖的鉴定和糖链结构的测定一、概述糖类又称碳水化合物(carbohydrates),是植物光合作用的初生产物,是一类丰富的天然产物,如:蔗糖、粮食(淀粉)、棉布的棉纤维等。糖类、核酸、蛋白质、脂质——生命活动所必需的四大类化合物。化学结构:多羟基内半缩醛(酮)及其缩聚物。根据其分子水解反应的情况,可以分为单糖、低聚糖和多糖。一、概述单糖:不能水解的最简单的多羟基内半缩醛(酮)。如葡萄糖等。低聚糖:水解后生成2~9个单糖分子的糖。如:蔗糖(D-葡萄糖-D果糖)麦芽糖(葡萄糖1→4葡萄糖)多糖:水解后能生成多个单分子的,称为多糖。如:淀粉、纤维素等二、结构类型㈠糖的表示式单糖是多羟基醛或酮。从三碳糖至八碳糖天然界都有存在。以Fischer式表示如下:二、结构类型单糖在水溶液中形成半缩醛环状结构,即成呋喃糖和吡喃糖。具有六元环结构的糖——吡喃糖(pyranose)具有五元环结构的糖——呋喃糖(furanose)糖处游离状态时用Fischer式表示苷化后成环用Haworth式表示CHOCH2OHOD-葡萄糖~二、结构类型㈡Fischer与Haworth的转换及其相对构型CHOCH2OHOOCH2OHHOHOCH2OHOHHOD-葡萄糖异侧同侧αβ异侧同侧二、结构类型Fischer式:(C1与C5的相对构型)C1-OH与原C5(六碳糖)或C4(五碳糖)-OH,顺式为α,反式为β。Haworth式:C1-OH与C5(或C4)上取代基之间的关系:同侧为β,异侧为α。二、结构类型㈢糖的绝对构型(D、L)以α-OH甘油醛为标准,将单糖分子的编号最大的不对称碳原子的构型与甘油醛作比较而命名分子构型的方法。CCH2OHOHHCHOCCH2OHHOHCHOα-OH甘油醛D型L型二、结构类型Fischer式中最后第二个碳原子上-OH向右的为D型,向左的为L型。Haworth式中C5向上为D型,向下为L型。OCCH2OHOHHCHOCHOCH2OHCHOCH3CH3Oα-OH甘油醛D型D-葡萄糖L-鼠李糖β-D-葡萄糖α-L-鼠李糖二、结构类型戊醛糖和已酮糖的绝对构型判断:吡喃型Haworth式,由于原构型标准(C4-OH和C5-OH)不参与成环,故可直接根据它们的位置判断构型。二、结构类型即:戊醛糖的C4或已酮糖的C5-OH处于环上者为L构型;环下者为D构型。习惯上将D型糖中C1-OH处环上者为体,环下者为体。在L型糖中相反。D-木糖(D-xylose)D-果糖(D-fructose)45二、结构类型已醛糖由Fischer转成呋喃型的Haworth,由于C5-C6部分成为环外侧链,判断构型时仍以C5为标准,C5-R者为D型糖;C5-S者为L型糖。同样,将D型糖中C1-OH处环上者为体,环下者为体。在L型糖中相反。RD-呋喃半乳糖二、结构类型㈣环的构象OOO1234(2)(3)(4)(5)二、结构类型Angyal用总自由能来分析构象式的稳定性,比较二种构象式的总自由能差值,能量低的是优势构象。如:葡萄糖的二种构象式的比较:OOOβ-D-葡萄糖C1式1C式三、糖苷分类㈠糖匀体均由糖组成的物质。如单糖、低聚糖、多糖等。1.常见单糖OCHOCH2OHCHOCH3CH3OCHOCH2OHOD-葡萄糖L-鼠李糖βαβαD-半乳糖三、糖苷分类CHOCH2OHOCHOCH2OHOOOCHOCH2OHOR1R2OR1R2-OH-OHβαβαD-甘露糖βαD-木糖D-果糖βαβα当构成二糖或多糖时呋喃当游离存在时吡喃三、糖苷分类2.氨基糖是指单糖的伯或仲醇基置换成氨基的糖类。OOHONH2OHNH32--2--D-glucose氨基去氧三、糖苷分类3.糖醇单糖的醛或酮基还原成羟基后所得的多元醇。4.去氧糖单糖分子的一个或二个羟基为氢原子代替的糖。CH2OHCH2OHCH2397CHOCH3D-山梨醇D-毛地黄毒糖(2,6-二去氧糖)三、糖苷分类5.糖醛酸单糖分子中伯醇基氧化成羧基的化合物。OOCOOHαC5-OH氧化成酸D-葡萄糖醛酸-三、糖苷分类㈡糖杂体糖与非糖组成的化合物——苷苷的分类:1.按苷原子不同分类⑴氧苷如:红景天苷OOOH红景天苷三、糖苷分类⑵氮苷:如腺苷。⑶硫苷:如萝卜苷。⑷碳苷:如牡荆素。OSN-OSO3SOOglcOHOHOOH牡荆素-萝卜苷ONNNNNH2腺苷三、糖苷分类2.按苷元不同分类如:黄酮苷、蒽醌、香豆素、强心苷、皂苷等3.按苷键不同分类⑴醇苷:是通过醇羟基与糖端基羟基脱水而成的苷。如红景天苷。⑵酚苷:是通过酚羟基而成的苷。如天麻苷。⑶酯苷:苷元以-COOH和糖的端基碳相连接的是酯苷。如山慈菇苷A。⑷氰苷:是指一类α羟腈的苷。如野樱苷。三、糖苷分类CH2OHOglcOOCH2OHOOOROCHCN野樱苷苦杏仁苷β天麻苷山慈菇苷AR=HR=-D-glc三、糖苷分类4.按端基碳构型分α苷,多为L型;β苷,多为D型。 5.按连接单糖个数分1个糖——单糖苷2个糖——双糖苷3个糖——叁糖苷三、糖苷分类6.按糖链个数分1个位置成苷——单糖链2个位置成苷——双糖链7.按生物体内存在分原级苷——在植物体内原存在的苷;次级苷——原级苷水解掉一个糖或结构发生改变。四、糖和苷的物理性质㈠溶解性糖——小分子极性大,水溶性好聚合度增高水溶性下降。多糖难溶于冷水,或溶于热水成胶体溶液。单糖极性>双糖极性(与羟基和碳的分担比有关,即按-OH/C的分担情况而定)苷——亲水性(与连接糖的数目、位置有关)苷元——亲脂性四、糖和苷的物理性质㈡味觉①单糖~低聚糖——甜味。②多糖——无甜味(随着糖的聚合度增高,则甜味减小)③苷类——苦、甜等(人参皂苷)(甜菊苷)四、糖和苷的物理性质㈢旋光性及其在构型测定中的应用具有多个不对称碳原子——用于苷键构型的测定(即α、β苷键)。多数苷类呈左旋。利用旋光性→测定苷键构型Klyne法:将苷和苷元的分子旋光差与组成该苷的糖的一对甲苷的分子旋光度进行比较,数值上相接近的一个便是与之有相同苷键的一个。五、糖的化学性质㈠氧化反应㈠氧化反应单糖的分子有醛(酮)、伯醇、仲醇和邻二醇等结构,氧化条件不同其产物也不同。如:CH2OHCHOBr2/H2OCH2OHCOOH稀HNO3COOHCOOH五、糖的化学性质㈠氧化反应糖分子化学反应的活泼性:端基碳原子>伯碳>仲碳(即C1-OH、C6-OH、C2C3C4-OH)以过碘酸反应为例来了解糖的氧化反应的应用过碘酸反应主要作用于:邻二醇、α-氨基醇、α-羟基醛(酮)、邻二酮和某些活性次甲基等结构。五、糖的化学性质㈠氧化反应邻羟基:RCCR\'HHOHOHIO4R-CHOR\'-CHO-+CCCHHOHOHHOHIO4R-CHOR\'-CHOHCOOH-2++五、糖的化学性质㈠氧化反应-羟基酮:-氨基醇:邻二酮:RCCR\'HOHOIO4R-CHOR\'-COOH-+CCHHNH2OHIO4R-CHOR\'-CHONH3-++CCOORR\'IO4R-COOHR\'-COOH+五、糖的化学性质㈠氧化反应反应特点:①反应定量进行(试剂与反应物基本是1:1);②在水溶液中进行或有水溶液(否则不反应);③反应速度:顺式>反式(因顺式易形成环式中间体);④游离单糖产物及消耗过碘酸用Fischer式计算;成苷时糖产物及消耗过碘酸用Haworth式计算;⑤在异边而无扭转余地的邻二醇不起反应。五、糖的化学性质㈠氧化反应Fischer式和Haworth式消耗过碘酸的计算:CHOCH2OHOIO4OCHOOHCOHOHOHCIO4D-葡萄糖5需消耗分子过碘酸3-+2HCOOH醚键开袭+HCOOH2-HCHO+2HCOOH五、糖的化学性质㈠氧化反应在异边无扭转余地的邻二醇:OOHOHOOHOOHOHOOH611,6β-D-葡萄呋喃糖酐1,6α-D-半乳呋喃糖酐五、糖的化学性质㈠氧化反应用途:①推测糖中邻二-OH多少;(试剂与反应物基本是1:1);②同一分子式的糖,推测是吡喃糖还是呋喃糖;OOHOHOHOROOHCH2OHORHIO4HIO4-OH具邻三可产生甲酸无甲酸产生五、糖的化学性质㈠氧化反应③推测低聚糖和多聚糖的聚合度;④推测1,3连接还是1,4连接(糖与糖连接的位置)OOROR\'OOROR\'β-D-葡萄糖五、糖的化学性质㈡糠醛形成反应㈡糠醛形成反应(Molish反应)单糖浓酸4~10N()加热-3H2O呋喃环结构矿酸10%HCl()单糖脱水多糖RCHO糠醛5-羟甲糠醛R=HR=CH2OH五、糖的化学性质㈡糠醛形成反应Molish反应:样品+浓H2SO4+α-萘酚→棕色环多糖、低聚糖、单糖、苷类——Molish反应=?糠醛衍生物+芳胺或酚类(苯酚、萘酚、苯胺、蒽酮等)缩合显色五、糖的化学性质㈢羟基反应㈢羟基反应糖的-OH反应——醚化、酯化和缩醛(酮)化。反应活性:最高的半缩醛羟基(C1-OH)其次是伯醇基(C6-OH)仲醇次之。(伯醇因其处于末端的空间,对反应有利,因此活性高于仲醇。)五、糖的化学性质㈢羟基反应1.醚化反应(甲基化)①Haworth法(不常用)含糖样品+Me2SO4+30%NaOH→醇-OH全甲基化(需反复6~8次)判断反应是否完全的方法:甲基化物可用红外光谱测试,直到无-OH吸收峰为止。制备成甲苷——用限量试剂,即克分子比11∶时,可得甲苷。五、糖的化学性质㈢羟基反应②Purdie法样品+MeI+Ag2O→全甲基化(醇-OH)只能用于苷,不宜用于还原糖(即有C1-OH的糖)。因Ag2O有氧化作用,可使C1-OH氧化。③Hakomori法(箱守法)样品+DMSO+NaH+MeI→全甲基化(一次即可)该反应是在非水溶剂中,即二甲基亚砜(DMSO)溶液中进行反应。五、糖的化学性质㈢羟基反应④重氮甲烷法(CH2N2)样品+CH2N2/Et2O+MeOH→部分甲基化(-COOH、-CHO等)2.酰化反应(酯化反应)羟基活性与甲基化反应相同,即(C1-OH、C6-OH、C3最难)(由于C2位取代后,引起的空间障碍,使得C3最难被酰化。)利用酰化可判断糖上-OH数目、保护-OH等。五、糖的化学性质㈢羟基反应3.缩酮和缩醛化反应酮或醛在脱水剂如矿酸、无水ZnCl2、无水CuSO4等存在下可与多元醇的二个有适当空间位置的羟基易形成环状缩酮(ketal)和缩醛(acetal)。酮类易与顺邻-OH生成——五元环状物醛类易与1,3-双-OH生成——六元环状物五、糖的化学性质㈢羟基反应糖+丙酮→五元环缩酮(异丙叉衍生物)糖+丙酮→六元环缩酮(双异丙叉衍生物)例:当糖具有顺邻-OH时,其生成五元环状物(异丙叉衍生物):OOMeMeOOOOO+H2SO4-H2Oα-D-半乳糖1,2;3,4--O-二异丙叉-α-D-半乳吡喃糖五、糖的化学性质㈢羟基反应当糖结构中无顺邻-OH时,则易转变为呋喃糖结构,再生成五元环状物(异丙叉衍生物)。OOOOOD-葡萄糖转变成呋呋喃糖硫酸丙酮1,2;5,6--O-二喃糖结构-D-异丙叉葡萄糖五、糖的化学性质㈢羟基反应糖+苯甲醛→六元环状缩醛(苯甲叉衍生物)例如:葡萄糖甲苷+苯甲醛⇒(具1,3-OH结构)以上方法主要目的是保护-OH。OOOHC6H5OMe4,6-O--α-D-反式的苯甲叉葡萄吡喃糖甲苷五、糖的化学性质㈣羰基反应㈣羰基反应还原糖+苯肼→糖腙(多为水溶性的)还原糖+3分子苯肼→糖脎(较难溶于水)2-去氧糖不能成脎(因C2上无-OH)。应用——糖的鉴定、分离和纯化。CHOHRCHOPhNHNH2CHOHRCH=NHNH2PhPhNHNH2CRCH=NHNH2PhOPhNHNH2NNHNNHROHHPhPh糖脎糖腙糖C2五、糖的化学性质㈤硼酸络合反应㈤硼酸络合反应糖的邻二-OH可与许多试剂生成络合物,借生成络合物的某些物理常数的改变,可以有助于糖的分离、鉴定和构型推定。重要的如:硼酸络合物、钼酸络合物、铜氨离子络合物等。糖+硼酸→络合物(酸性增加、可离子化)(H3BO3是接受电子对的Lewis酸)五、糖的化学性质㈤硼酸络合反应硼酸络合反应的应用:①络合后,中性可变为酸性,因此可进行酸碱中和滴定;②可进行离子交换法分离;③可进行电泳鉴定;④在混有硼砂缓冲液的硅胶薄层上层析。六、苷键的裂解研究苷类的化学结构,必须了解苷元结构、糖的组成、糖和糖的连接方式,以及苷元和糖的连接方式等。为此必先使用某种方法使苷键切断。㈠酸催化水解反应㈡乙酰解反应㈢碱催化水解和β消除反应㈣酶催化水解反应㈤氧化开裂法(Smith降解法)六、苷键的裂解㈠酸催化水解反应㈠酸催化水解反应苷键属于缩醛结构,易为稀酸催化水解。水解反应是苷原子先质子化,然后断键生成阳碳离子或半椅型的中间体,在水中溶剂化而成糖。OOROOROHOHOOH2OH,OHH++H+-ROH+阳碳离子半椅式中间体+H2O+-H+六、苷键的裂解㈠酸催化水解反应酸水解的规律:⑴苷原子不同,酸水解难易顺序:N>O>S>C(C-苷最难水解,从碱度比较也是上述顺序)⑵呋喃糖苷较吡喃糖苷易水解。因五元呋喃环的颊性使各取代基处在重叠位置,形成水解中间体可使张力减小,故有利于水解。⑶酮糖较醛糖易水解酮糖多为呋喃结构,而且酮糖端基碳原子上有-CH2OH大基团取代,水解反应可使张力减小。六、苷键的裂解㈠酸催化水解反应⑷吡喃糖苷中:①吡喃环C5上取代基越大越难水解,水解速度为:五碳糖>甲基五碳糖>六碳糖>七碳糖②C5上有-COOH取代时,最难水解(因诱导使苷原子电子密度降低)⑸氨基取代的糖较-OH糖难水解,-OH糖又较去氧糖难水解。2,3-二去氧糖>2-去氧糖>3-去氧糖>羟基糖>2-氨基糖六、苷键的裂解㈠酸催化水解反应⑹在构象相同的糖中:a键(竖键)-OH多则易水解。⑺芳香属苷较脂肪属苷易水解。如:酚苷>萜苷、甾苷(因苷元部分有供电结构,而脂肪属苷元无供电结构)⑻苷元为小基团苷键横键比竖键易水解(e>a)(横键易质子化)苷元为大基团苷键竖键比横键易水解(a>e)(苷的不稳定性促使其易水解)六、苷键的裂解㈡乙酰解反应㈡乙酰解反应1.常用试剂:醋酐+酸所用酸如:H2SO4、HClO4、CF3COOH或Lewis酸(ZnCl2、BF3)等。2.反应条件:一般是在室温放置数天。3.反应机理:与酸催化水解相似,以CH3CO+(乙酰基,Ac)为进攻基团。六、苷键的裂解㈡乙酰解反应※乙酰解反应易发生糖的端基异构化。OOAcOAcOAcOAcOAcOOAcOAcOAcOAcOAcOAcOAcOAcOAcOAcORHOOAcOAcOAcOAcOAcAcOOAcOAcCH2OAcAcOOAcH,OAcOAcOAcOAcOAc++++__αβ六、苷键的裂解㈡乙酰解反应4.反应速率:⑴苷键邻位有电负性强的基团(如环氧基)可使反应变慢。⑵β-苷键的葡萄糖双糖的反应速率:(乙酰解易难程度)(1→6)>>(1→4)>>(1→3)>>(1→2)六、苷键的裂解㈡乙酰解反应5.用途⑴酰化可以保护苷元上的-OH,使苷元增加亲脂性,可用于提纯和鉴定。⑵乙酰解法可以开袭一部分苷键而保留另一部分苷键。六、苷键的裂解㈢碱催化水解㈢碱催化水解和β消除反应一般苷键对稀碱是稳定的,但某些特殊的苷易为碱水解,如:酯苷酚苷烯醇苷β-吸电子基取代的苷六、苷键的裂解㈢碱催化水解C1-OH与C2-OH:反式易水解,其产物为1,6-葡萄糖酐;顺式产物为正常的糖。利用水解产物可判断苷键构型OOHOC6H5OOOC6H5OOOOOOHOH脱水---OH--苯酚β-葡萄糖苷1,6-葡萄糖酐六、苷键的裂解㈢碱催化水解β-消除反应:苷键的β-位有吸电子基团者,使α-位氢活化,在碱液中与苷键起消除反应而开裂,称~。作用机理:在1→3或1→4连接的聚糖中,还原端的游离醛(或酮)邻位氢活化而与3-O-或4-O-苷键起消除反应。这样碱能使多糖还原端的单糖逐个被剥落,对非还原端则无影响。剥落生成的是α-羟基糖酸。六、苷键的裂解㈢碱催化水解β-消除反应作用过程:OHROOHOHCH2OHCHOHOHOHROOHOHCH2OHCHOCH457OHOHOHCH2OHCHOCH2467OOHOHCH2OHCHOCH2476OHOHOHCH2OHCOOHCH2485OHOHOHCH2OHCOOH---OR+互变重排-3-脱氧-D-阿拉伯已糖酸核已糖酸3-脱氧-D-苷键β位苷键3-O-代糖六、苷键的裂解㈢碱催化水解用途:可从多糖剥落反应生成的糖酸中了解还原糖的取代方式。3-O-代的糖可形成——3-脱氧糖酸4-O-代的糖可形成——3-脱氧-2-羟甲基糖酸二个以上取代的还原糖——难生成糖酸六、苷键的裂解㈣酶催化水解反应㈣酶催化水解反应用酶水解苷键可以获知苷键的构型,可保持苷元结构不变的真正苷元。酶专属性高,选择性地催化水解某一构型的苷。如:苦杏仁酶(emulsin)——水解——β-葡萄糖苷键纤维素酶(cellulase)——同上麦芽糖酶(maltase)——水解——α-葡萄糖苷键六、苷键的裂解㈤氧化开裂法㈤氧化开裂法(Smith降解法)可得到原苷元(除酶解外,其它方法可能得到的是次级苷元)试剂:过碘酸(HIO4)、四氢硼钠(NaBH4)、稀酸反应过程:OOROOROHCOHCHOH2CCH2OHOORROHCH2OHCHOCH2OHHOH2COH++IO4-BH4-H+氧化还原水解苷二元醛二元醇苷元七、糖的提取分离㈠提取㈠提取主要为溶剂法——水、稀醇(单糖、低聚糖、多糖)糖类的提取可根据它们对乙醇和水的溶解度不同,而采用冷热水、冷热稀醇等条件。苷类分子的极性随着糖基的增多而增大。可根据其极性大小,来选择相适应的溶剂。破坏或抑制植物体内酶的方法:采集新鲜材料——迅速加热干燥——冷冻保存等七、糖的提取分离㈡分离㈡分离1.活性炭柱色谱2.纤维素色谱3.离子交换柱色谱4.凝胶柱色谱5.季铵氢氧化物沉淀法6.分级沉淀或分级溶解法7.蛋白质除去法七、糖的提取分离㈡分离1.活性炭柱色谱⑴概述用途——分离水溶性物质较好如:氨基酸、糖类及某些苷类。特点:(对于活性炭柱色谱)①上样量大,分离效果较好,适合大量制备;②来源容易,价格廉;③缺点:无测定其吸附力级别的理想方法。七、糖的提取分离㈡分离分类:①粉末状活性炭——颗粒细,总表面积大,吸附力及吸附量大。②颗粒状活性炭——颗粒较上者大,吸附力及吸附量也较上者次之。③绵纶-活性炭——以锦纶为粘合剂,将粉末状活性炭制成颗粒,吸附力最弱。七、糖的提取分离㈡分离⑵活性炭对物质的吸附规律对分子量大的化合物吸附力大于分子量小的化合物,即:多糖>单糖活性炭在水溶液中的吸附力最强,在有机溶剂中吸附力较弱。洗脱顺序:H2O、10%、20%、30%、50%、70%乙醇液无机盐→二糖→三糖→多糖单糖等七、糖的提取分离㈡分离2.纤维素色谱原理与PC相同,属分配层析。溶剂系统:水、丙酮、水饱和的正丁醇等。用水溶性的溶剂如HAc:H2O进行展开时,其原理属吸附层析。七、糖的提取分离㈡分离3.离子交换柱色谱①除水提液中的酸、碱性成分和无机离子;②制成硼酸络合物——强碱性阴离子交换树脂(不同浓度硼酸盐液洗脱)七、糖的提取分离㈡分离4.凝胶柱色谱常用商品名称及型号:葡聚糖凝胶(商品名:SephadexG)G-10、G-15、G-200等[10—表示吸水量乘以10,即1.0ml/g的吸水量]琼脂糖凝胶(Sepharose,Bio-GelA)聚丙烯酰胺凝胶(Bio-GelP)羟丙酰基交联葡聚糖凝胶(SephadexLH-20)(亲脂性,可在有机溶剂中进行分离的分子筛)七、糖的提取分离㈡分离操作过程:除LH-20外,均在H2O中进行。①将凝胶在适当的溶液中浸泡(多为洗脱剂);②待充分膨胀后装入层析柱;③用洗脱液洗脱;④收集、回收溶液,干燥。七、糖的提取分离㈡分离洗脱溶剂的选择:分离中性物质——水及电解质溶液(酸、碱、盐溶液及缓冲液)阻滞较大的组分——水+有机溶液(水-甲醇、水-乙醇、水-丙酮等)LH-20可用有机溶液进行溶胀(如:CHCl3、丁醇、二氧六环等)(适用:有机物质的分离,如:脂类、固醇类等)七、糖的提取分离㈡分离5.季铵氢氧化物沉淀法季铵氢氧化物是一类乳化剂。C16H33NMeMeMeOH季铵氢氧化物+酸性糖(含-COOH)沉淀CTA-OH(cetyltrimethylammoniumhydroxide).-+七、糖的提取分离㈡分离6.分级沉淀或分级溶解法在糖的水溶液中,逐步加入乙醇,即逐渐增大EtOH浓度,可得到各部分的沉淀物。为使多糖稳定,多糖通常在pH=7时进行酸性多糖在pH=2~4时进行处理酸性多糖时,为防酸水解苷键,操作宜迅速。七、糖的提取分离㈡分离7.蛋白质除去法用分级沉淀法得到的多糖,常夹杂有较多的蛋白质,为除之,通常选择能使蛋白质沉淀而使多糖不沉淀的试剂来处理,如:酚、三氯乙酸、鞣酸等。注意:处理时间要短,温度要低。(避免多糖降解)三氟三氯乙烷法和Sevag法(用氯仿:戊醇或丁醇4:1混合)在避免降解上有较好效果。七、糖的提取分离㈡分离㈢糖的提取分离实例地黄根中单糖和低聚糖的分离取鲜根→热EtOH、H2O提→阴阳离子交换树脂(除酸碱成分)得中性成分活性炭柱(15%HOAc处理)以H2O、稀EtOH(5、10、15、25%顺次洗脱),经PC检定,合并D-葡萄糖D-半乳糖D-果糖蔗糖棉子糖甘露三糖水苏糖(四糖)毛蕊糖(五糖)八、糖的鉴定和糖链结构的测定㈠糖的鉴定1.纸层析展开系统:常用水饱和的有机溶剂展开。如:正丁醇:醋酸:水(4:1:5上层)BAW水饱和苯酚等溶剂系统。显色剂:邻苯二甲酸苯胺、硝酸银试剂(使还原糖显棕黑色)、三苯四氮唑盐试剂(单糖和还原性低聚糖呈红色)、3,5-二羟基甲苯盐酸试剂(酮糖呈红色)等。八、糖的鉴定和糖链结构的测定2.薄层层析可用(硼酸液+无机盐)+硅胶→制板吸附剂:硅胶(用0.03M硼酸液或无机盐的水液代水制板)常用的无机盐:0.3M磷酸氢二钠或磷酸二氢钠0.02M乙酸钠0.02M硼酸盐缓冲液0.1M亚硫酸氢钠/H2O八、糖的鉴定和糖链结构的测定硼酸与无机盐制板的特点:增加糖在固定相中的溶解度,使硅胶薄层吸附能力下降,利于斑点集中,又可增加样品的承载量。显色剂:除纸层析应用的以外,还用如:H2SO4/H2O或乙醇液茴香醛-硫酸试剂苯胺-二苯胺磷酸试剂等八、糖的鉴定和糖链结构的测定3.气相层析将糖制备成三甲基硅醚(增加其挥发性)将醛糖用NaBH4还原成多元醇(避免形成端基异构体)制成乙酰化物或三氟乙酰化物。4.液相色谱填充材料——化学修饰的硅胶优:不必制备成衍生物。适合分析对热不稳定、不挥发的低聚糖和多糖。分析单糖和低聚糖,其灵敏度不及气相层析。八、糖的鉴定和糖链结构的测定5.离子交换层析糖的硼酸络合物——可进行离子交换层析优:不必制成衍生物,而直接用水溶液进行分离(与气相比较)糖自动分析仪:显色:3,5-二羟基甲苯-浓硫酸波长:425nm上样量:每种组成不超过1mg洗脱剂:四硼酸钾的缓冲溶液八、糖的鉴定和糖链结构的测定㈡糖链结构的测定主要解决的问题——单糖的组成、糖之间的连接位置和顺序、苷键构型1.单糖的组成2.单糖之间连接位置的决定3.糖链连接顺序的决定4.苷键构型的决定5.13C-NMR在糖链结构测定中的应用八、糖的鉴定和糖链结构的测定1.单糖的组成低聚糖、多糖的结构分析,首先要了解由哪些单糖所组成,各种单糖之间的比例如何。一般是将苷键全水解,用PC检出单糖的种类,经显色后用薄层扫描仪求得各种糖的分子比。也可用GLC或HPLC对单糖定性定量。GLC常以甘露醇或肌醇为内标,用已知单糖作标准。八、糖的鉴定和糖链结构的测定2.单糖之间连接位置的决定①将糖链全甲基化→水解→甲基化单糖的定性和定量(气相层析)(甲基化单糖中游离-OH的部位就是连接位置)②13C-NMR测定:主要归属各碳信号,以确定产生苷化位移的碳。八、糖的鉴定和糖链结构的测定3.糖链连接顺序的决定①缓和水解法:将糖链水解成较小的片段,然后分析这些低聚糖的连接顺序。②质谱分析。4.苷键构型的决定⑴分子旋光差(klyne法)⑵酶催化水解方法⑶1H-NMR判断糖苷键的相对构型⑷其它八、糖的鉴定和糖链结构的测定⑶1H-NMR判断糖苷键的相对构型在糖的1H-NMR中:端基质子——δ5.0ppm左右其它质子——δ3.5~4.5ppm可通过C1-H与C2-H的偶合常数,来判断苷键的构型(α、β)例如:D-葡萄糖八、糖的鉴定和糖链结构的测定D-葡萄糖OORHHOHOORHHOH18060。。-D-glucose-D-glucoseC1-HC2-H近180(双面角)J=6~8Hz。C1-HC2-H近60(双面角)J=3~4Hz。αβ八、糖的鉴定和糖链结构的测定用1H-NMR可判断一些糖的相对构型,但还有一些糖由于其结构上的原因,而无法利用1H-NMR来判断相对构型。如:OORHOHHOOROHHH-D-甘露糖-D-甘露糖C1-HC2-H都约为60(双面角)。αβJ所以无法从值判断构型八、糖的鉴定和糖链结构的测定再如:⑷其它IR——α葡萄糖苷在770、780cm-1有强吸收峰;MS——葡萄糖苷乙酰化物331碎片峰强度:α>βOORMeHOHHOORMeHOHHC1-HC2-H都约为60(双面角)-L-鼠李糖-L-鼠李糖αβJ所以无法从值判断构型八、糖的鉴定和糖链结构的测定5.13C-NMR在糖链结构测定中的应用端基碳——δ97~106ppm一般在13C-NMR谱中:如:D-葡萄糖~100~~78~~62~C1C3C5C2C4C6八、糖的鉴定和糖链结构的测定D-葡萄糖苷C1——α型97~101ppmβ型103~106ppmCH-OH(C2、C3、C4)70~85ppmCH2-OH(C6)62左右CH3<20ppm用门控去偶技术,可判断呋喃糖的端基碳与端基质子的偶合常数。α苷键JC-H≈170Hzβ苷键JC-H≈160Hz八、糖的鉴定和糖链结构的测定苷化位移(glycosidationshift)糖苷化后,端基碳和苷元α-C化学位移值均向低场移动,而邻碳稍向高场移动(偶而也有向低场移动的),对其余碳的影响不大,这种苷化前后的化学变化,称苷化位移。OOCH2CH2R+5.0~6.5-3.5~5.0αβ八、糖的鉴定和糖链结构的测定苷元β位有取代时的苷化位移:①苷元α-碳手性和糖端基手性都为R(或S)时,苷化位移值与苷元为位无取代的环醇相同。如:OORR+3.4+6.8-0.6-4.7R-R八、糖的鉴定和糖链结构的测定②苷元α-碳和糖端基碳手性不同时,端基碳和α-碳的苷化位移值比苷元为β-无取代的相应碳的苷化位移值大约为3.5ppm。OORS+7.6+10.6+0.2-1.7相应增加约3.5ppmR-S八、糖的鉴定和糖链结构的测定酯苷、酚苷的苷化位移:当糖与-OH形成酯苷键或酚苷键时,其苷化位移值较特殊,端基碳和苷元α-碳均向高场位移。OOHOHOHOH-D-GlcβC1=101.1-0.7-0.9+1.6+0.8酚苷键八、糖的鉴定和糖链结构的测定三萜类化合物——齐墩果酸:OHCOOH-D-Glcβ-D-GlcβC1=106.9C1=95.7+0.3-0.8-0.2-3.9-1.2+10.3+0.334172215酯苷键醇苷键本章重点内容掌握常见几种单糖的结构(Haworth式);掌握化学反应的特点及应用;掌握苷键裂解的各种方法及其特点;(如:酸解、碱解、酶解、Smith降解等)1H-NMR及13C-NMR在糖苷中的应用(如:苷键构型的测定、化学位移值大致区间、糖端基碳的化学位移值、利用J值判断苷键构型、苷化位移(含酚苷和酯苷)等。)theend



















