







《《酸和碱》化学性质教学PPT课件下载》是由用户上传到老师板报网,本为文库资料,大小为20.7 MB,总共有38页,格式为ppt。授权方式为VIP用户下载,成为老师板报网VIP用户马上下载此课件。文件完整,下载后可编辑修改。
- 文库资料
- 38页
- 20.7 MB
- VIP模板
- ppt
- 数字产品不支持退货
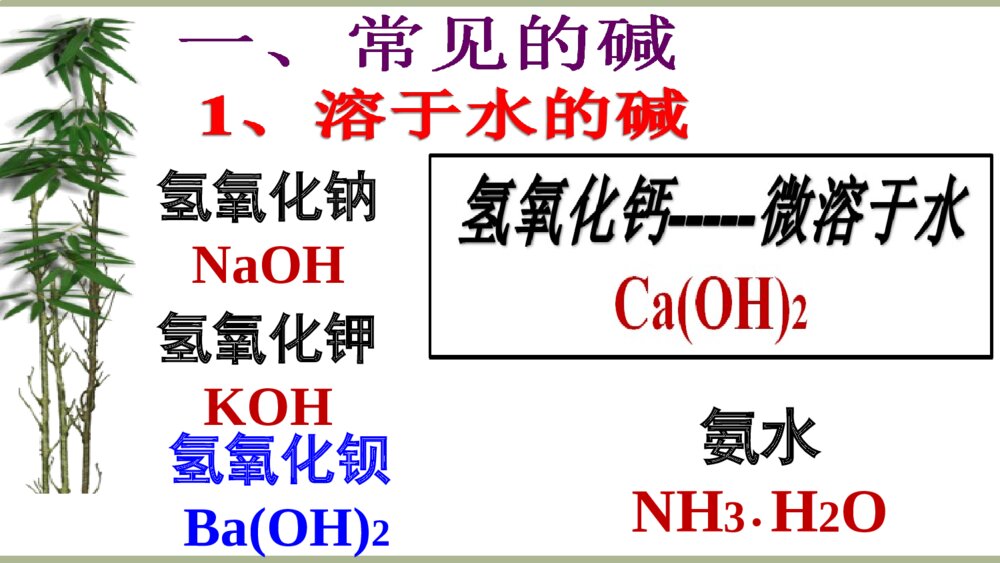
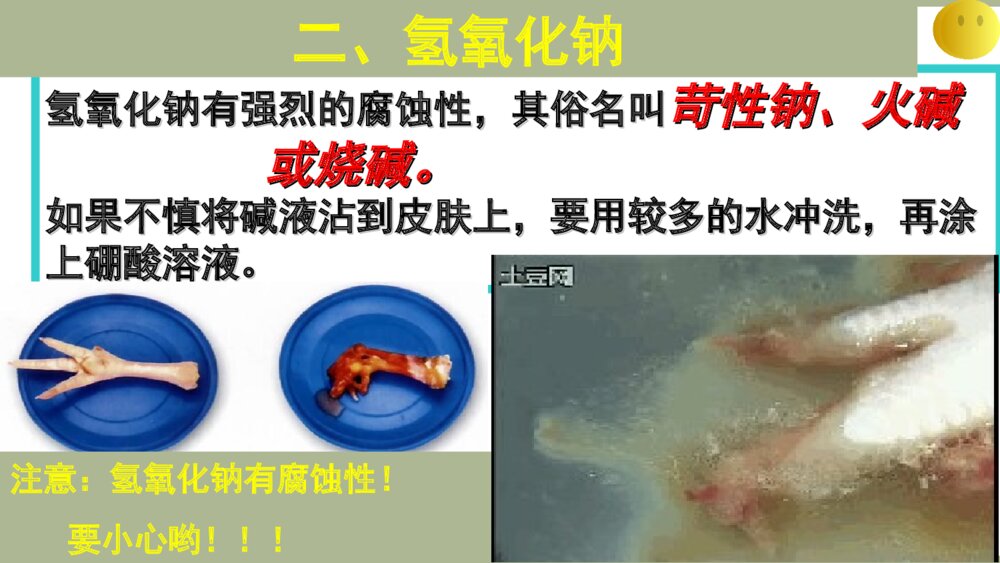
第十单元酸和碱课题1常见的酸和碱<2>氢氧化钠NaOH氢氧化钾KOH氨水NH3H2O.氢氧化钡Ba(OH)22、不溶于水的碱(1)白色沉淀:Mg(OH)2Al(OH)3(2)蓝色沉淀:Cu(OH)2红褐色沉淀:Fe(OH)3氢氧化钠有强烈的腐蚀性,其俗名叫氢氧化钠有强烈的腐蚀性,其俗名叫苛性钠、火碱苛性钠、火碱或烧碱。或烧碱。如果不慎将碱液沾到皮肤上,要用较多的水冲洗,再涂如果不慎将碱液沾到皮肤上,要用较多的水冲洗,再涂上硼酸溶液。上硼酸溶液。注意:氢氧化钠有腐蚀性!要小心哟!!!二、氢氧化钠11、、氢氧化钠氢氧化钠((NaOHNaOH)的物理性质)的物理性质实验实验现象现象分析分析观察观察放表面皿上放表面皿上放入水中放入水中白色块状固体白色块状固体表面潮湿溶解表面潮湿溶解溶液温度升高溶液温度升高氢氧化钠氢氧化钠易易吸吸收空气中的水收空气中的水分而分而潮解潮解溶解时放热溶解时放热色态:白色固体溶解性:极易溶于水,并放出大量的热氢氧化钠特性吸水性腐蚀性(化学性质)可做某些气体的干燥剂,如O2、H2等但不能干燥CO2、SO2、SO3、HCl等易吸水潮解并能和二氧化碳反应皮肤、织物和纸张等都能被它腐蚀用天平称量NaOH时应注意什么?为什么要密封保存?能垫纸称量吗?水溶液有涩味和滑腻感为什么要密封保存?(2).(2).氢氧化钙氢氧化钙[Ca(OH)[Ca(OH)22]]俗称:俗称:熟石灰或消石熟石灰或消石灰灰注意:注意:氢氧化钙也有腐蚀性,使用时应注意安全。氢氧化钙也有腐蚀性,使用时应注意安全。CaO+HCaO+H22O=Ca(OH)O=Ca(OH)22放出大量的热CaOCaO俗俗称称生石灰生石灰制取:CaCO3=CaOCaO+CO+CO22高温CaO+HCaO+H22O=Ca(OH)O=Ca(OH)22放大量的热CaOCaO生石生石灰灰氢氧化钙的用途:CO2+Ca(OH)2=H2O+CaCO3↓Na2CO3+Ca(OH)2=CaCO3↓+2NaOH1、用于建筑,制三合土,石灰浆2、工业制碱、漂白粉3、和硫酸铜一起配制农药波尔多液.4、农业改良酸性土壤5、处理泄露的浓硫酸本节重点无色酚酞试液变为红色蓝色使紫色石蕊试液变为1、氢氧化钠溶液能与酸碱指示剂反应化学魔术的奥妙你见过“白纸显字”吗?能解释吗?雨落红花开喷泉试验喷泉试验↙↙蒸馏水中蒸馏水中滴有酚酞滴有酚酞↙↙浓氢氧化钠溶液浓氢氧化钠溶液CO2氢氧化钠能不能与一些非金属氧化物反应呢?NaOH+CO2=——氢氧化钠要密封保存哦NaOH+SO2=——可吸收工业尾气中的二氧化硫CO2NaOH本节重难点想看看吗神奇吧Na2SO42.氢氧化钠+非金属氧化物盐+水NaOH+SO3=+H2O想一想2Na2CO3+H2O2Na2SO3+H2O2Ca(OH)2+CO2=CaCO3↓+H2O1.实验室盛装NaOH溶液的试剂瓶用橡皮塞而不用玻璃塞,你知道为什么吗?【提示】防止玻璃塞中的SiO2与NaOH溶液反应生成粘稠的Na2SiO3,使瓶塞和瓶口粘在一起(SiO2+2NaOH====Na2SiO3+H2O)。【思考与交流】【方法点拨】盛有硅酸钠溶液的试剂瓶也不能用玻璃塞,因为它本身是一种粘合剂。4、碱+酸NaOH+HCl=NaOH+H2SO4=本节重点盐+水NaOH+HNO3=NaNO3+H2ONaCl+H2ONa2SO4+H2O想一想22现象:红色溶液变为无色Cu(OH)2+Na2SO44、氢氧化钠+盐FeCl3+NaOH=本节重难点↓新碱+新盐蓝色溶液中生成一种蓝色的沉淀黄色溶液中生成一种红褐色的沉淀想一想MgCl2+NaOH=Mg(OH)2+NaCl白色沉淀现象:现象:32CuSO4+NaOH=22Fe(OH)3+NaCl↓3现象 化学方程式分析溶液产生白色沉淀含有CO32-的碳酸盐溶液与石灰水能反应产生白色沉淀Na2CO3+Ca(OH)2=CaCO3↓+2NaOH向盛有少量Na2CO3溶液的试管滴入澄清的石灰水,观察现象。Ca(OH)2溶液与Na2CO3溶液的反应5、氢氧化钠有强腐蚀性三、氢氧化钠的用途石油化工制皂氢氧化钠的用途(另纺织上、做干燥剂、除去二氧化碳)3、能使酚酞变红的溶液,一般能使石蕊试液显()A、红色B、蓝色C、紫色D、无色1、下列对氢氧化钠的描述中,不正确的是()A、NaOH固体极易溶于水,溶解时吸收大量的热B、其水溶液有涩味和滑腻感C、对皮肤、衣服都有强烈的腐蚀性D、其水溶液能使紫色石蕊试液变蓝色A、NaOH固体极易溶于水,溶解时吸收大量的热2、下列气体其中能用氢氧化钠干燥的是()A、CO2B、O2C、SO3D、HClB、O244、下列物质暴露在空气中,质量增加且变质的是()、下列物质暴露在空气中,质量增加且变质的是()(A)(A)浓硫酸浓硫酸(B)(B)火碱火碱(C)(C)水水(D)(D)浓盐酸浓盐酸(B)(B)火碱火碱B66、用天平称量固体氢氧化钠时,、用天平称量固体氢氧化钠时,应把氢氧化钠直接放在应把氢氧化钠直接放在()()(A)(A)天平的托盘上天平的托盘上(B)(B)滤纸滤纸上上(C)(C)小烧杯内小烧杯内(D)(D)试试管中管中C例1、喷泉是一种常见的自然现象,其产生原因是存在压强差。(1)如图甲为喷泉实验装置。在烧瓶中充满干燥气体,胶头滴管及烧杯中分别盛有液体。下列组合中不可能形成喷泉的是()A、HCl和H2OB、O2和H2OC、NH3和H2OD、CO2和NaOH甲乙B、6B、D、这节课你该有哪些收获?1.与酸碱指示剂的作用2.氢氧化钠+非金属氧化物盐+水3.氢氧化钠+酸4.氢氧化钠+盐盐+水新盐+新碱2NaOH+CO2=2NaOH+SO2=NaOH+HCl=2NaOH+H2SO4=CuSO4+2NaOH=↓↓Na2CO3+H2ONa2SO3+H2O亚硫酸钠NaCl+H2ONa2SO4+2H2OCu(OH)2+Na2SO4Fe(OH)3+3NaCl火碱、烧碱、苛性钠Na2SO35.有腐蚀性FeCl3+3NaOH=1、含铵根的盐类用碱溶液(NaOH、Ca(OH)2等)和湿润的红色石蕊试纸检验。------看是否变蓝2、含铵根的盐类和熟石灰氢氧化钙在一起研磨(或和氢氧化钠等碱溶液反应),会产生有刺激性气味的气体(氨气)碱溶液能与硝酸铵或硫酸铵等铵盐反应3、“旺旺雪饼”袋内有一个小纸袋,上面写着:干燥剂,主要生石灰⑴、生石灰做干燥剂的理由是?⑵我对它做了一系列探究,获得较多收益,其实验方案如下问题与猜想实验步骤实验现象实验结论1、小纸袋中的物质能否继续做干燥剂?取小纸袋中的固体放入烧杯中,加入适量的水,触摸杯壁不能做干燥剂2、我猜想变质后的物质可能是____⑶、对它还有一个要探究的新问题:不放热CaCO3等有气泡产生固体中含有碳酸钙变质后有多少碳酸钙生成;完全变质需要多少时间等取少量固体于试管中,注入盐酸问道题:氢氧化钠为什么必须密封保存?为什么氢氧化钠必必须须密密封封保保存存??ÎüÊÕË®·ÖÎüÊÕ二氧化碳Ë®·ÖÕô·¢Na2CO3粉末Na2CO3溶液NaOH溶液NaOH固体1.氢氧化钠要密封保存的原因(1)吸收空气中的___而潮解(2)吸收空气中的_____而变质2.NaOH与C02反应无现象,证实反应发生方法(1)设计有现象的对比实验(密闭容器里NaOH溶液与C02反应了,瓶内压强减少而产生明显现象),但NaOH溶液中有和两种物质,产生现象可能是三种原因造成的:①C02与_____反应②C02与反应③C02与_____和同时反应.(2)验证有新物质Na2C03生成(加入或___)CO2+2NaOH===Na2CO3+H2O水C02水NaOHNaOH水NaOH水足量稀盐酸氯化钙溶液1)利用CO2与NaOH溶液反应后使容器里气体压强减小,产生相应的现象(图1-2)利用CO2与NaOH溶液反应后生成Na2CO3溶液质量增大(图9);3)利用CO2与NaOH溶液反应吸收后不能使澄清石灰水变浑浊(图10)4)检验生成物Na2CO3滴加稀盐酸产生气泡;加CaCl2溶液[或BaCl2溶液、Ba(OH)2溶液、Ca(OH)2溶液等]有白色沉淀。加CaCl2溶液CO2+2NaOH==Na2CO3+H2O12.为探究CO2和NaOH确实发生了化学反应,某实验小组的同学设计出了下列4种实验装置,请回答下列问题:(1)选择任意一种实验装置,简述出现的实验现象,解释产生该现象的原因。选择的实验装置是。实验现象为:。产生该实验现象原因:。(2)某同学质疑上述实验设计,该同学质疑的依据是:。(3)在原实验的基础上,请你设计实验证明CO2和NaOH肯定发生了化学反应。气球胀大3可能是水与二氧化碳反应和二氧化碳溶于水使压强减小NaOH与CO2反应压强减小取少量的反应后的溶液滴入足量稀盐酸,若有气泡产生,证明证明CO2和NaOH肯定发生了化学反应。3.存放不严密的NaOH的成分可能有三种():(1)无变质:滴入或()溶液,无气泡产生(或无白色沉淀)(3)除NaOH中的Na2C03杂质:边搅拌边滴入_______溶液,直至____________为止,过滤,得到NaOH溶液.(注:检验Na2CO3时必须加入_____稀盐酸,CaCl2溶液酚酞酚酞刚好不再产生沉淀过量足量稀盐酸过量CaCl2Ca(OH)2或Ca(OH)2无变质/部分变质/全部变质过量CaCl2因稀盐酸先与溶液中的NaOH反应2.存放不严密的NaOH的成分(1)没有变质:滴入(或____________________)溶液,无气泡(或无白色沉淀)产生。氢氧化钙(或氯化钙)(2)部分变质:加入___________________溶液,目的是检验并完全除去Na2CO3,避免对氢氧化钠检验的干扰,过滤,取滤液少量,滴入__________,变_________红色。酚酞溶液(3)全部变质:加入________________溶液,目的是检验并完全除去Na2CO3,过滤,取滤液少量,滴入__________,不变色。3.除去NaOH中的Na2CO3杂质边搅拌边滴入____________________溶液,直至____________为止,过滤,得到NaOH溶液。刚好不再产生沉淀足量的稀盐酸足量的氯化钙(或氯化钡)酚酞溶液足量的氯化钙(或氯化钡)氢氧化钙(或氢氧化钡)6.怎样证明氢氧化钠是否变了质?1、加稀盐酸或稀硫酸。2、取样品少许,加水溶解后滴入氯化钙或氯化钡溶液(或氢氧化钙、氢氧化钡溶液等)看能否有白色沉淀生成7.怎样证明氢氧化钠部分或全部变质?取样品少许,加水溶解后滴入氯化钙或氯化钡溶液,如果有沉淀生成(说明变质了),过滤(除去碱性物质碳酸钠,避免对氢氧化钠检验的干扰),向滤液中滴入无色酚酞(或硫酸铜溶液),如果酚酞变红(或有蓝色沉淀生成),则说明氢氧化钠部分变质,否则全部变质。过量或足量过量注意:不能加入过量氢氧化钙或氢氧化钡等碱的溶液,会生成了氢氧化钠并引入碱性溶液不能说明氢氧化钠是否有剩余实验后忘记塞上瓶塞的氢氧化钠溶液的试剂瓶瓶口周围有一些白色固体。怀疑氢氧化钠溶液已经变质,于是进行了如下实验探究。【提出问题】氢氧化钠溶液是否变质?【提出猜想】①该氢氧化钠溶液没有变质②部分变质;③全部变质【实验验证】【讨论】上述所给的结论是否正确?为什么?小明认为,根据上述实验(1)(2)可推断,猜想②正确。而小张则认为猜想③也可能正确,理由是。于是小王又设计了如下补充实验:(1)取原溶液少量于试管中,逐滴加入BaCl2溶液至。静置,分层。(2)取上层清液,向其中加入CuSO4溶液,若有蓝色沉淀产生,则说明氢氧化钠溶液部分变质,化学方程式:。反之则说明氢氧化钠溶液已经全部变质。操作现象结论化学方程式取少量溶液于试管中,滴加无色酚酞试液无色酚酞变红溶液中含有氢氧化钠取少量溶液于试管中,滴加足量稀盐酸有气泡产生----------------------讨论:若先向溶液中滴加足量的Ba(OH)2,再滴入酚酞,根据现象不同来判断猜想(2)成立猜想(3)成立。同学们认为此方案不行,原因是________________________过量Ba(OH)2和生成的NaOH都能使酚酞变红,不能检验原溶液中是否有NaOH。氢氧化钠是一种碱性干燥剂干燥范围:碱性气体干燥范围:碱性气体(NH(NH33))中性气体中性气体(H(H22、、OO22、、NN22等等))注意;不能干燥酸性气体注意;不能干燥酸性气体(HCl(HCl、、NONO22、、COCO22、、SOSO22、、HH22SS等等))用锌粒和盐酸反应制取的氢气中,常混有水蒸气和氯化氢气体,为了除去气体杂质,可使混合气体通过下图A、B两装置,气体通过两瓶的导管顺序正确的是()A、abcdB、dcbaC、cdabD、bacdabcd浓硫酸NaOH溶液CAB探究活动2:氢氧化钠的化学性质实验1实验2实验3实验现象:1;2;3。实验结论:1;2;3。



















