





《《空间利用率的计算》高中化学PPT课件下载》是由用户上传到老师板报网,本为文库资料,大小为1.08 MB,总共有17页,格式为ppt。授权方式为VIP用户下载,成为老师板报网VIP用户马上下载此课件。文件完整,下载后可编辑修改。
- 文库资料
- 17页
- 1.08 MB
- VIP模板
- ppt
- 数字产品不支持退货
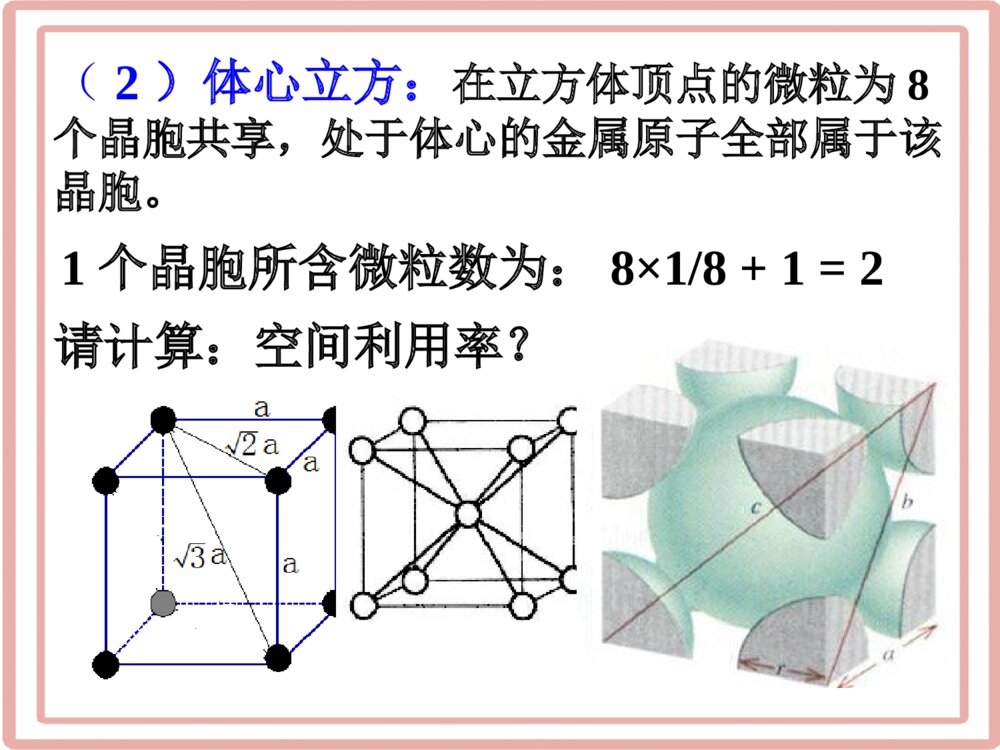
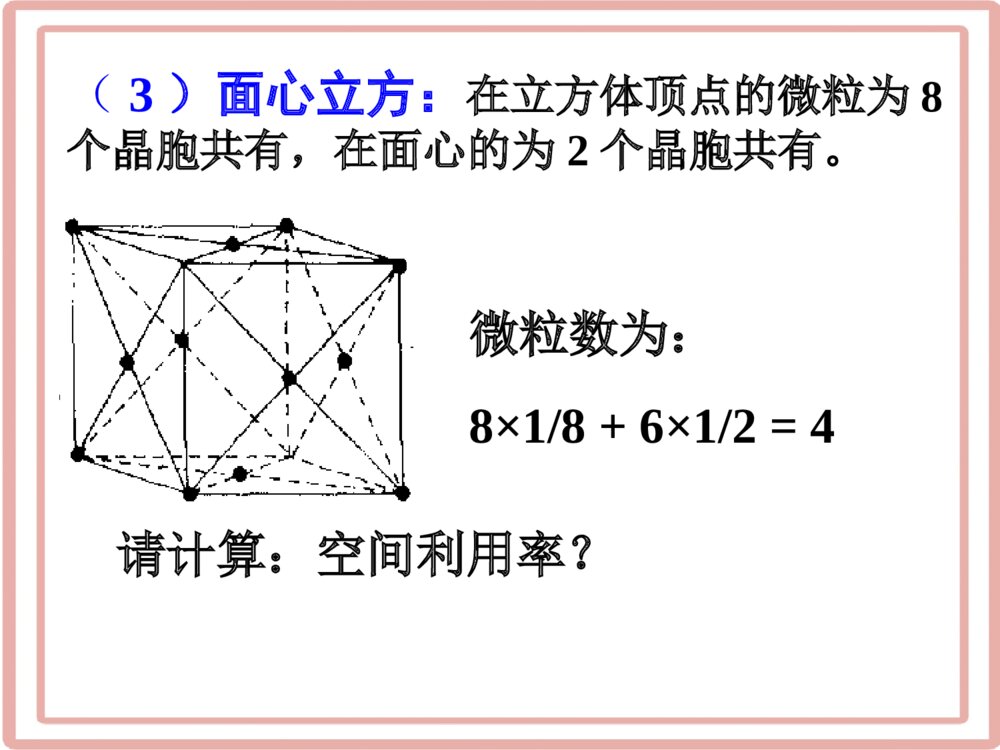
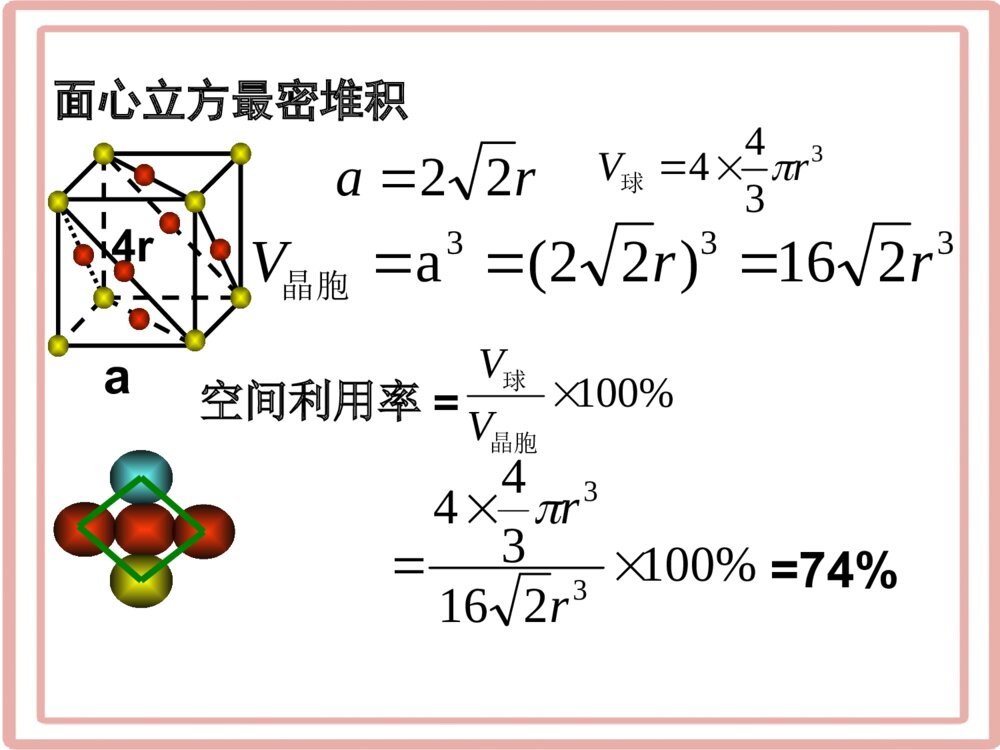
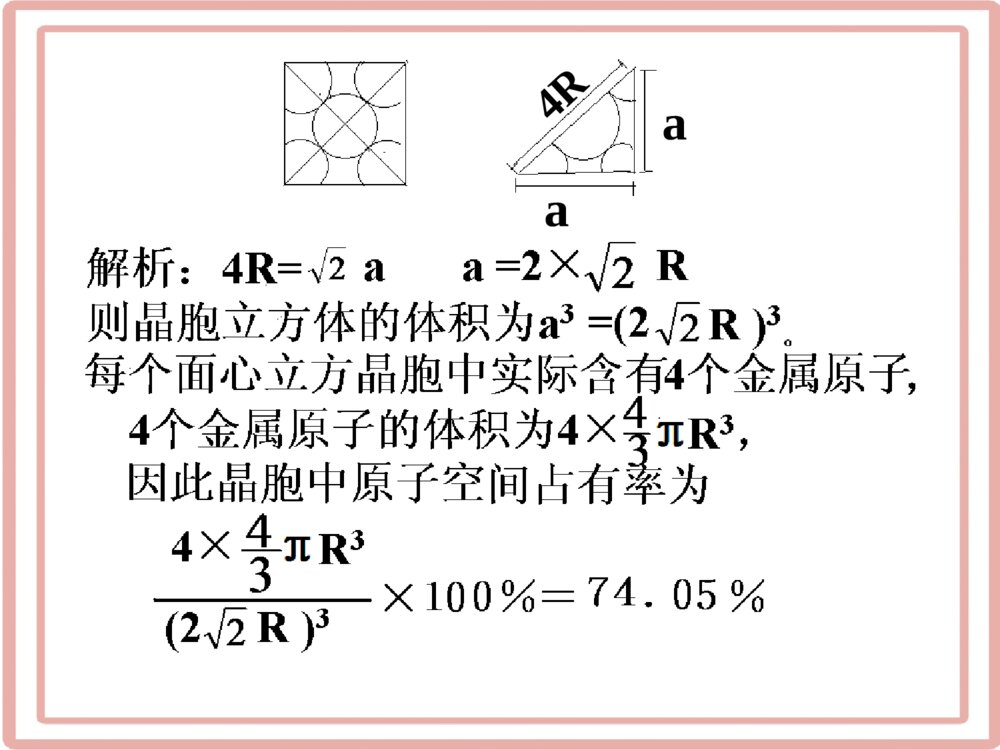
一、空间利用率的计算1、空间利用率:指构成晶体的原子、离子或分子在整个晶体空间中所占有的体积百分比。球体积空间利用率=100%晶胞体积(1)计算晶胞中的微粒数2、空间利用率的计算步骤:(2)计算晶胞的体积1、简单立方堆积立方体的棱长为2r,球的半径为r2r过程:1个晶胞中平均含有1个原子V球=334r%100晶胞球VVV晶胞=(2r)3=8r3空间利用率=%10083433rr=52.06%≈52(2)体心立方:在立方体顶点的微粒为8个晶胞共享,处于体心的金属原子全部属于该晶胞。1个晶胞所含微粒数为:8×1/8+1=2请计算:空间利用率?体心立方堆积ab222aab22223)4(abarra34%10034233ar%1003434233)(rr%68%10083空间利用率=a(3)面心立方:在立方体顶点的微粒为8个晶胞共有,在面心的为2个晶胞共有。微粒数为:8×1/8+6×1/2=4请计算:空间利用率?面心立方最密堆积4rara223344rV球333216)22(arrV晶胞%100晶胞球VV%10021634433rr=74%空间利用率=aa4R222解:(4)六方密堆积(镁型)四点间的夹角均为60°在镁型堆积中取出六方晶胞,平行六面体的底是平行四边形,各边长a=2r,则平行四边形的面积:平行六面体的高:22360sinaaaSaaah3623622的四面体高边长为3、六方最密堆积s2r23232rrrsrh3623342rV球h2r2r32283622322srrrhV晶胞%100晶胞球VV%1002834233rr=74%空间利用率=sh【例题1】现有甲、乙、丙、丁四种晶胞,可推知甲晶体中与的粒子个数比为——————;乙晶体的化学式为——————————;丙晶体的化学式为——————;丁晶体的化学式为———。ABCDFEZXY1:1DC2或C2DEF或FEXY2Z甲乙丙丁【例题2】上图甲、乙、丙三种结构单元中,金属原子个数比为—————————。甲乙丙1:2:3乙晶胞中所含金属原子数为8×1/8+6×1/2=4晶胞中所含金属原子数为12×1/6+2×1/2+3=6堆积方式晶胞类型空间利用率配位数实例面心立方【堆积方式及性质小结】简单立方体心立方六方堆积面心立方六方体心立方简单立方74%74%68%52%121286Cu、Ag、AuMg、Zn、TiNa、K、FePo方法一:把整个晶体拆分成8个小立方晶体,这样来,每相邻的两个晶体的原子才够凑成一个标准的体心立方晶体的原子,这样的话,空间利用率就是标准体心立方晶体的一半,也就是34%金刚石空间利用率方法二:计算:假想体心有一个球,沿着体对角线将有5个球,则体对角线距离为d=8r=√3a,在边长为a的立方体中,有8个碳原子,也可算出为0.34



















