



《化学必修2《第三节 生活中两种常见的有机物乙醇》PPT课件下载》是由用户上传到老师板报网,本为文库资料,大小为2.18 MB,总共有26页,格式为ppt。授权方式为VIP用户下载,成为老师板报网VIP用户马上下载此课件。文件完整,下载后可编辑修改。
- 文库资料
- 26页
- 2.18 MB
- VIP模板
- ppt
- 数字产品不支持退货
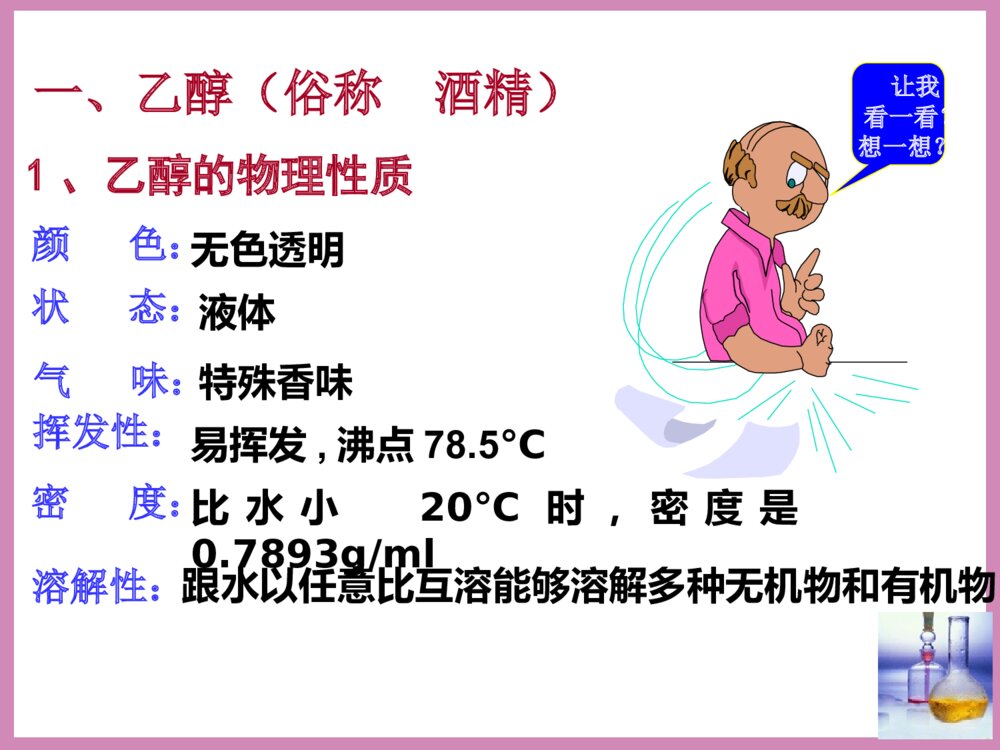
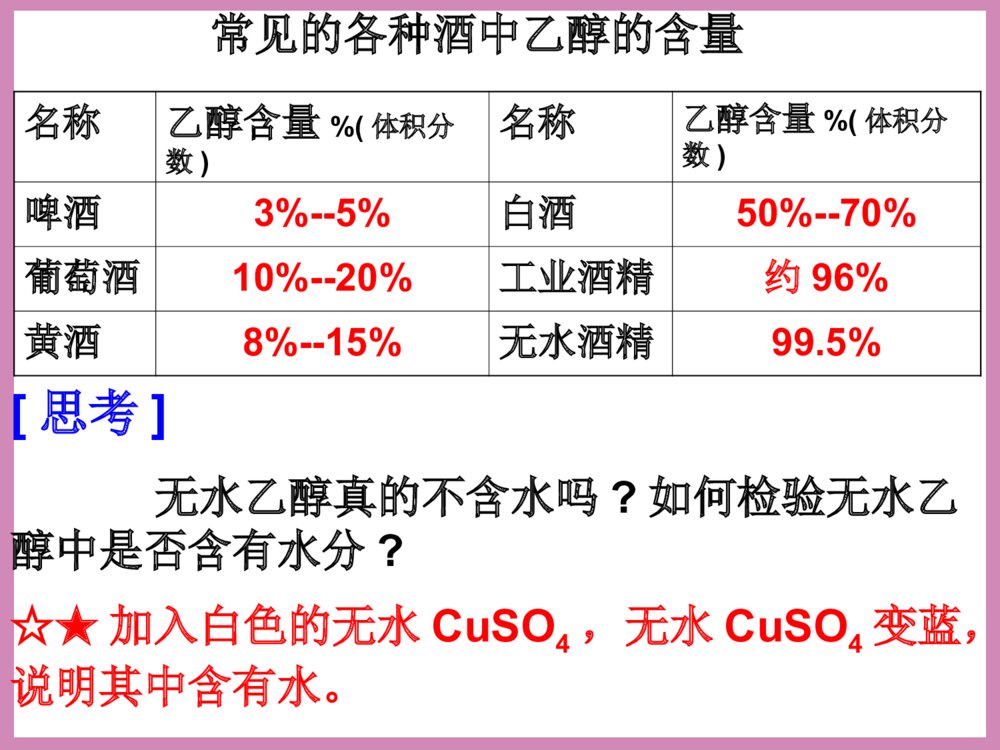
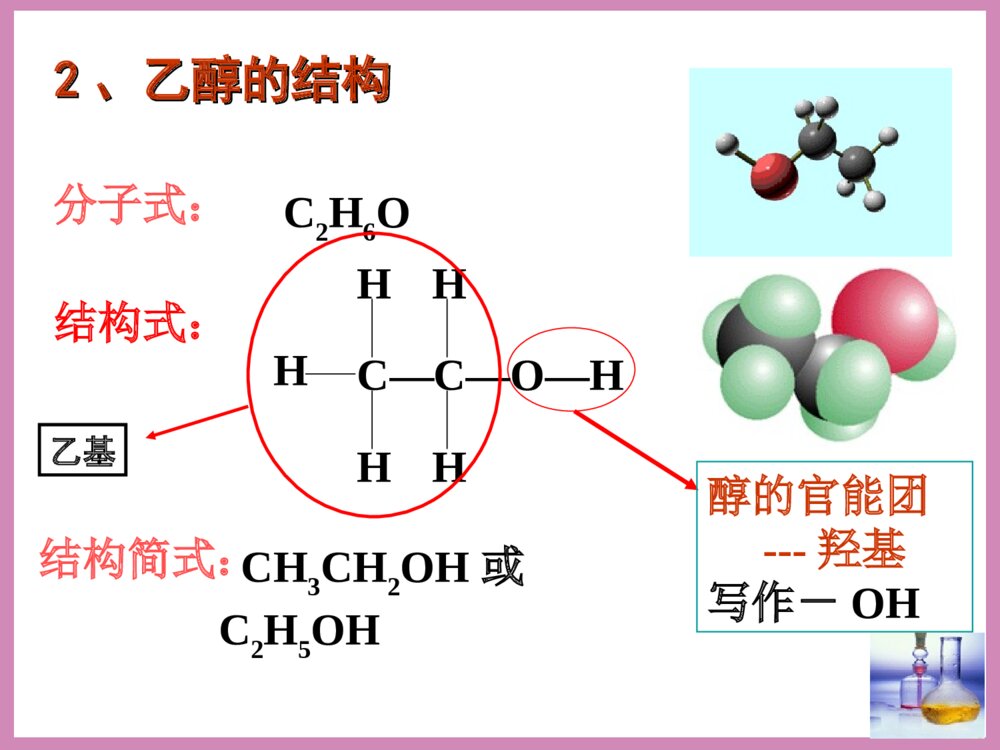
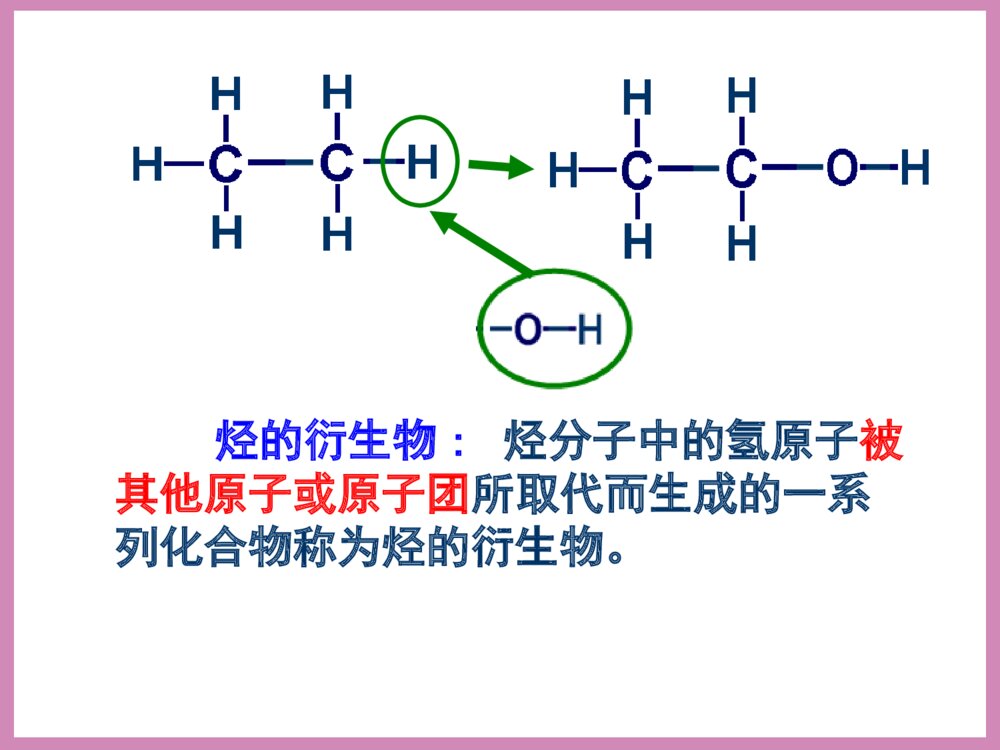
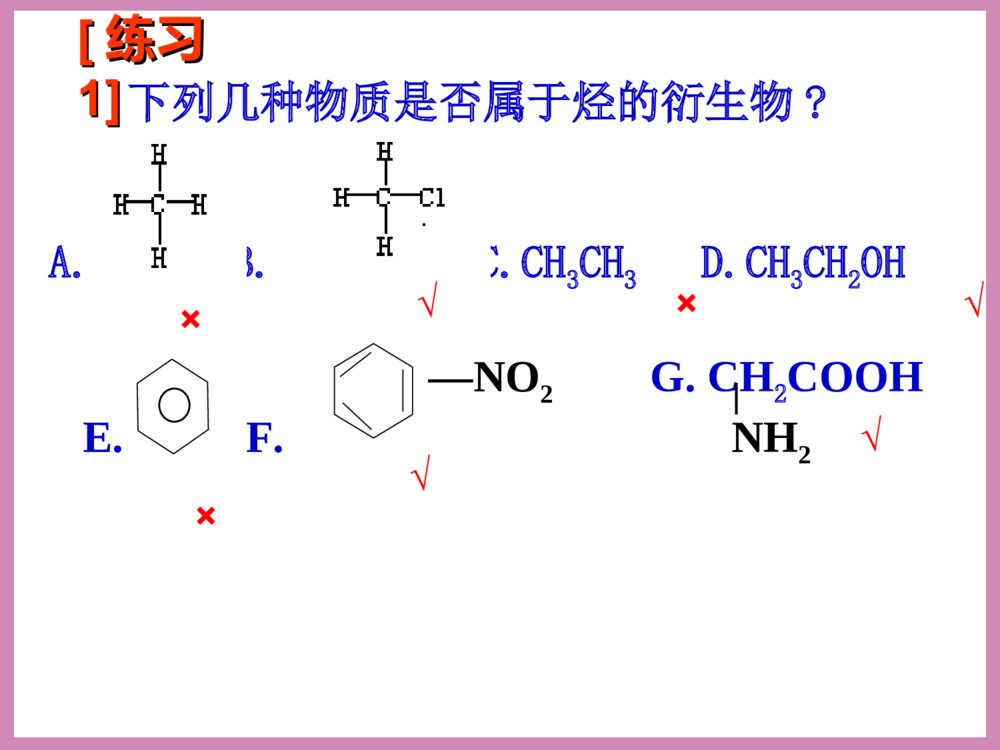
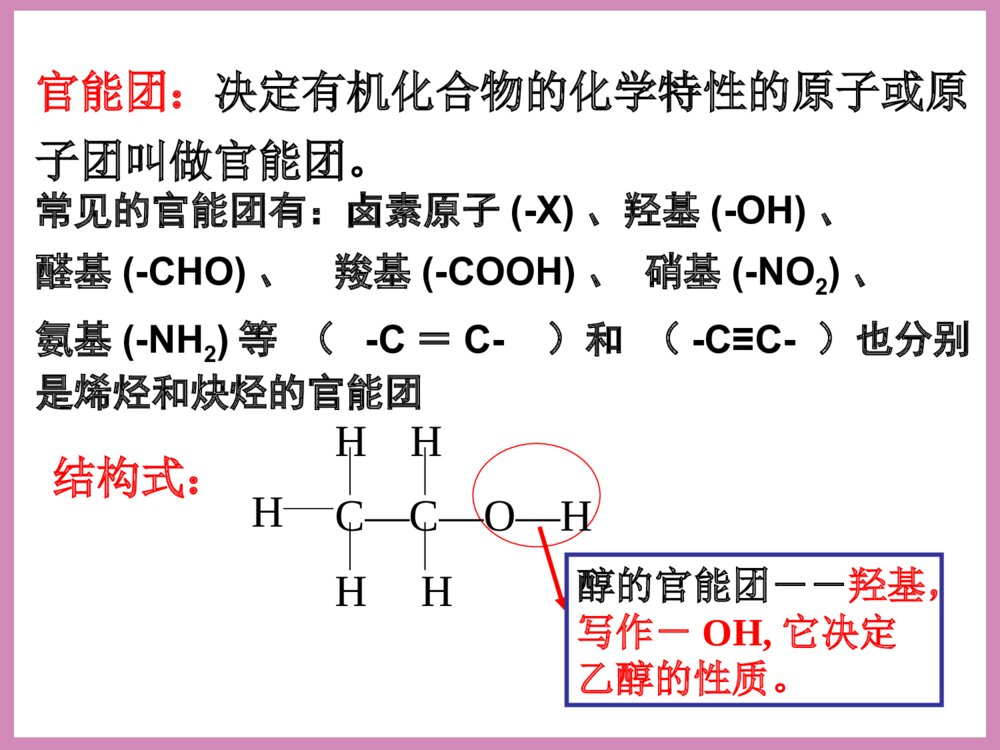
2016年5月18日周三第三节生活中两种常见的有机物(第一课时)清明时节雨纷纷,路上行人欲断魂。借问_____何处有,牧童遥指杏花村。酒家下列应用体现了乙醇的哪些性质或用途(1).“中国汽车要喝酒”(2).高烧病人擦拭酒精或白酒降温(3).碘酒(4).酒精灯和固体酒精(5).“李白斗酒诗百篇”让我看一看?想一想?气味:无色透明特殊香味液体比水小20℃时,密度是0.7893g/ml跟水以任意比互溶能够溶解多种无机物和有机物易挥发,沸点78.5℃一、乙醇(俗称酒精)颜色:溶解性:密度:挥发性:状态:1、乙醇的物理性质名称乙醇含量%(体积分数)名称乙醇含量%(体积分数)啤酒3%--5%白酒50%--70%葡萄酒10%--20%工业酒精约96%黄酒8%--15%无水酒精99.5%常见的各种酒中乙醇的含量[思考]无水乙醇真的不含水吗?如何检验无水乙醇中是否含有水分?☆★加入白色的无水CuSO4,无水CuSO4变蓝,说明其中含有水。C—C—O—HHHHHH结构式:CH3CH2OH或C2H5OH醇的官能团---羟基写作-OH分子式:22、乙醇的结构、乙醇的结构C2H6O结构简式:乙基烃的衍生物:烃分子中的氢原子被其他原子或原子团所取代而生成的一系列化合物称为烃的衍生物。下列几种物质是否属于烃的衍生物?A.B.C.CH3CH3D.CH3CH2OH—NO2G.CH2COOHE.F.NH2[[练习练习1]1]√√√√×××C—C—O—HHHHHH结构式:醇的官能团--羟基,写作-OH,它决定乙醇的性质。官能团:决定有机化合物的化学特性的原子或原子团叫做官能团。常见的官能团有:卤素原子(-X)、羟基(-OH)、醛基(-CHO)、羧基(-COOH)、硝基(-NO2)、氨基(-NH2)等(-C=C-)和(-C≡C-)也分别是烯烃和炔烃的官能团实验促学探究一观察实验用品中的金属钠是怎样保存的;在一支试管中加入无水乙醇,再加入米粒大小的金属钠,观察并记录实验现象。现象:金属钠沉入试管底部,反应缓慢,钠块表面有气泡产生思考:钠与水反应的现象?[交流讨论]1、乙醇与水都能与钠反应并放出气体,说明O—H键上的H原子能被钠原子取代。2、由于CH3CH2-和H原子对-OH的影响不同,乙醇和水与钠反应的速率和剧烈程度明显不同。3、乙醇的化学性质(1)乙醇与钠的反应——CH3CH2OH+Na→CH3CH2ONa+H2↑222H—C—C—O—H,HHHH①处O—H键断开①☆★含有-OH的物质一般都能与活泼金属反应放出H2。(取代反应)2mol-OH→1molH2。乙醇与钠反应的速率水与钠反应的速率﹤[练习]其它活泼金属如钾、镁和铝等也可与乙醇反应,均可产生H2,请写出镁与乙醇反应的化学方程式。2CH3CH2OH+Mg(CH3CH2O)2Mg+H2↑乙醇镁2CH3CH2OH+2K→2CH3CH2OK+H2↑(2)乙醇的氧化反应①燃烧:优质燃料(清洁,可再生,放出热量多)C2H5OH+3O22CO2+3H2O点燃酒精完全燃烧后,生成的产物可用一种物质完全吸收,这种物质是()A、浓硫酸B、NaOH溶液C、碱石灰D、无水氯化钙C[练习]②与强氧化剂反应乙醇还可以与酸性高锰酸钾或重铬酸钾溶液反应,被直接氧化成:乙酸C2H5OHK2Cr2O7(H+)CH3COOH世界卫生组织的事故调查显示,大约50%--60%的交通事故与酒后驾车有关。【探究二】1、将铜丝放在酒精灯外焰灼烧,慢慢移向内焰,上下几次。观察铜丝的变化。铜丝外焰内焰变黑变红2、在试管中加入3-5mL无水乙醇,将铜丝烧热,迅速插入乙醇中,反复多次,观察铜丝颜色和乙醇气味的变化。实验现象将铜丝在火焰上烧热铜丝由红色变成黑色将烧热的铜丝插入无水乙醇中铜丝由黑色变成红色,反复多次后闻到刺激性气味[交流讨论]2Cu+O22CuOCH3CH2OH+CuOCH3CHO+Cu+H2O总式:2CH3CH2OH+O22CH3CHO+2H2OCu红色变为黑色黑色变为红色乙醇乙醛氧原子水动画演示:H—C—C—OHHHHHH—C—C—OHHH氢原子碳原子[结论]③醇的催化氧化2CH3CH2OH+O2Cu2CH3CHO+2H2O课堂反馈1、乙醇分子中不同的化学键如图:化学反应中乙醇的断键位置(1)与活泼金属反应键断裂(2)CH3CH2OH燃烧键断裂(3)在Cu或Ag催化下和O2反应键断裂C—C—O—HHHHHH①②③④⑤①①③全部2.下列有关乙醇的物理性质应用中不正确的是()A.由于乙醇的密度比水小,所以乙醇中的水可以通过分液的方法除去B.由于乙醇能够溶解很多有机物和无机物,所以可用乙醇提取中草药的有效成分C.由于乙醇能够以任意比溶解于水,所以酒厂可以勾兑各种浓度的酒D.由于乙醇容易挥发,所以才有俗语“酒好不怕巷子深”的说法A羟基氢氧根化学式电性电子式来源羟基氢氧根化学式-OHOH--电性电中性带一个单位的负电荷电子式来源水分子失去氢原子的余下部分,不能独立存在水分子失去氢离子的余部分,能独立存在迁移博学★节省石油资源★汽油掺入酒精能让燃料“变绿”小结•乙醇的分子结构•乙醇的物理性质•乙醇的化学性质•作业课后习题



















