






《人教版九年级上册化学·第五单元·课题3 利用化学方程式的简单计算(第2课时)PPT课件》是由用户上传到老师板报网,本为文库资料,大小为303.11 KB,总共有21页,格式为pptx。授权方式为VIP用户下载,成为老师板报网VIP用户马上下载此课件。文件完整,下载后可编辑修改。
- 文库资料
- 21页
- 303.11 KB
- VIP模板
- pptx
- 数字产品不支持退货
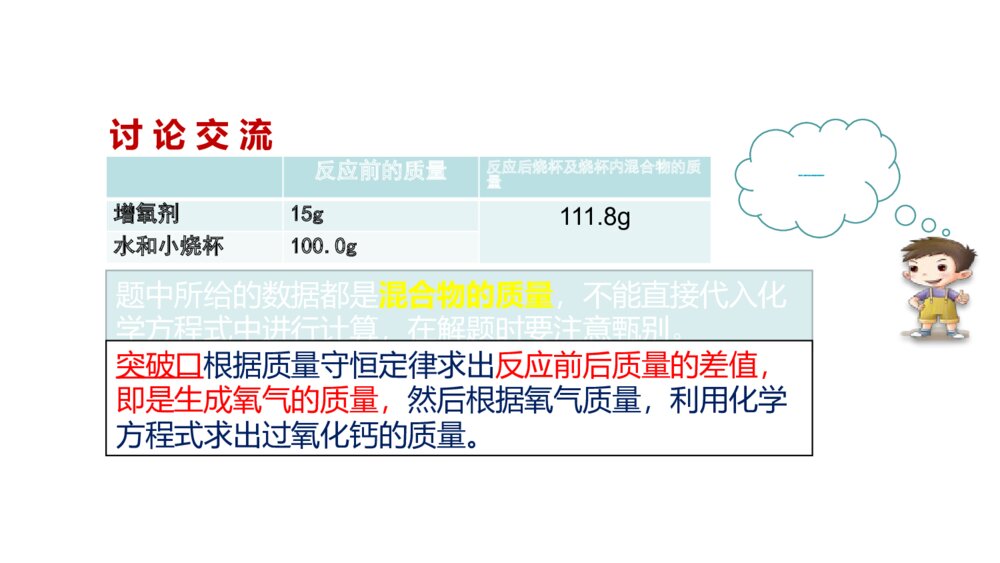
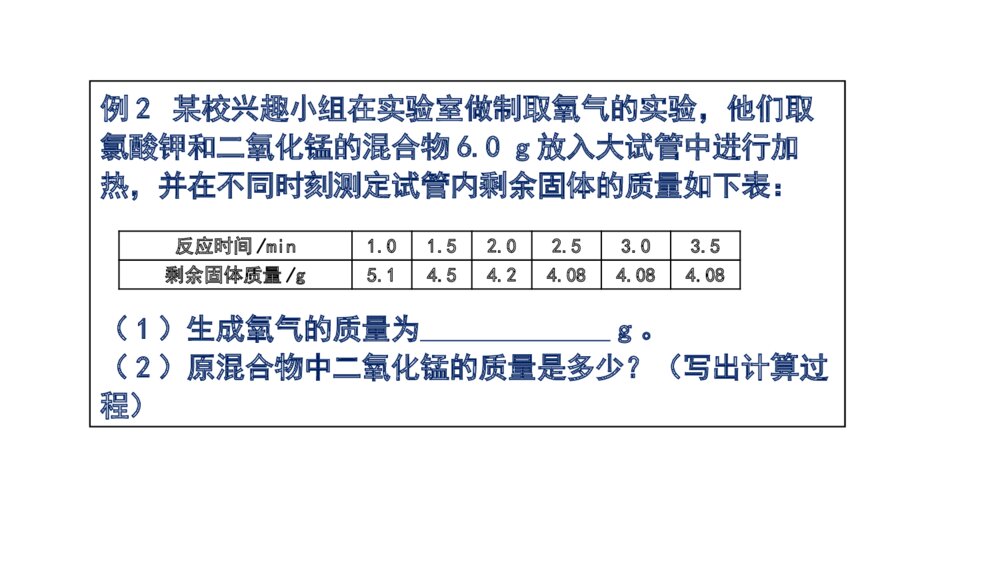
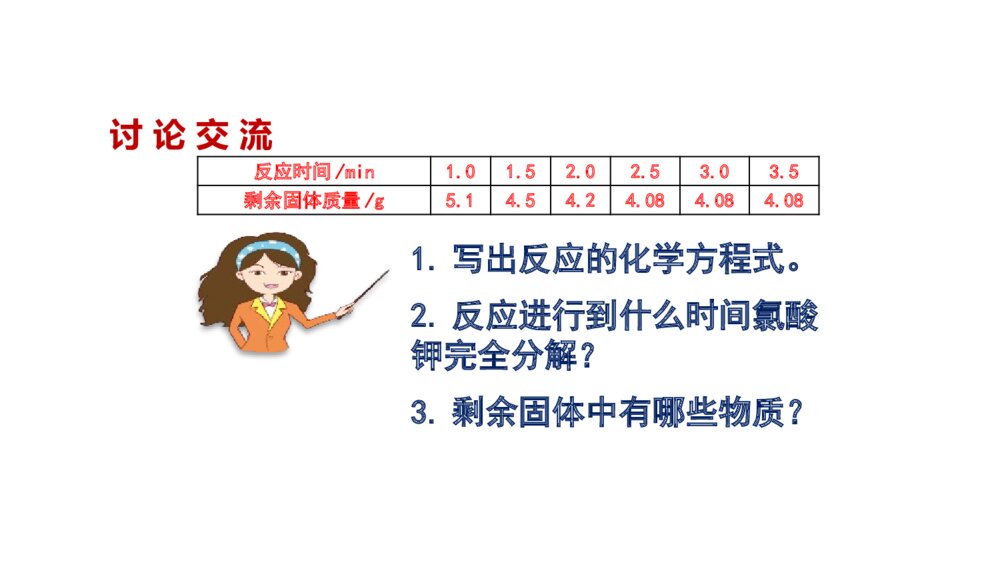
第五单元化学方程式第2课时课题3利用化学方程式的简单计算1.通过练习,能熟练进行化学方程式的简单计算。2.通过交流讨论,会运用质量守恒进行化学方程式的综合计算,能解决生产生活实际中的一些有关计算问题。学习目标例1饲养观赏鱼,可以陶冶人的情操,增进人们对生活的热爱。空运观赏鱼,必须密封。为了解决鱼的呼吸问题,可在水中加入增氧剂,主要成分为过氧化钙(化学式为CaO2),过氧化钙与水反应,生成氢氧化钙和氧气。(1)写出过氧化钙与水反应的化学方程式。应用质量守恒定律进行化学方程式计算自主探究2CaO2+2H2O=2Ca(OH)2+O2↑(2)一位养鱼爱好者做如下实验:取少量增氧剂加入到足量的水中,称量数据如下。求参加反应的过氧化钙的质量。反应前的质量反应后烧杯及烧杯内混合物的质量增氧剂15g111.8g水和小烧杯100.0g讨论交流题中所给的数据都是混合物的质量,不能直接代入化学方程式中进行计算,在解题时要注意甄别。突破口根据质量守恒定律求出反应前后质量的差值,即是生成氧气的质量,然后根据氧气质量,利用化学方程式求出过氧化钙的质量。反应前的质量反应后烧杯及烧杯内混合物的质量增氧剂15g111.8g水和小烧杯100.0g表中哪一数据可以代入到方程式中进行计算?解:氧气的质量为15g+100.0g-111.8g=3.2g设参加反应的过氧化钙的质量为x。2CaO2+2H2O=2Ca(OH)2+O214432x3.2g144:32=x:3.2gx=14.4g答:参加反应的过氧化钙的质量为14.4g。某课外小组为了测定石灰石中碳酸钙的含量,把10g石灰石固体样品进行高温煅烧,完全反应后,冷却、称量,残余固体质量为7.8g(假设杂质不参与反应),计算石灰石样品中碳酸钙的质量分数。变式训练解:二氧化碳的质量为10g-7.8g=2.2g设参加反应的碳酸钙的质量为X。CaCO3CaO+CO210044X2.2g100:44=X:2.2gX=5g×100%=50%答:石灰石样品中碳酸钙的质量分数为50%。5g10g例2某校兴趣小组在实验室做制取氧气的实验,他们取氯酸钾和二氧化锰的混合物6.0g放入大试管中进行加热,并在不同时刻测定试管内剩余固体的质量如下表:(1)生成氧气的质量为 g。(2)原混合物中二氧化锰的质量是多少?(写出计算过程)反应时间/min1.01.52.02.53.03.5剩余固体质量/g5.14.54.24.084.084.08讨论交流1.写出反应的化学方程式。2.反应进行到什么时间氯酸钾完全分解?3.剩余固体中有哪些物质?反应时间/min1.01.52.02.53.03.5剩余固体质量/g5.14.54.24.084.084.08解:氧气的质量为6.0g-4.08g=1.92g设参加反应的氯酸钾质量为x。2KClO32KCl+3O2↑ 245 96 x1.92g245:96=x:1.92gx=4.9g原混合物中二氧化锰的质量:6.0g-4.9g=1.1g答:可制得氧气的质量为1.92g,原混合物中二氧化锰的质量是6.0g-4.9g=1.1g。某小组利用高锰酸钾160g制取氧气,一段时间后发现试管中剩余固体共150.4g,问生成氧气质量是多少?参加反应的高锰酸钾质量是多少?变式训练解:氧气的质量为160g-150.4g=9.6g设参加反应的高锰酸钾质量为x。2KMnO4K2MnO4+MnO2+O2↑△3169.6g31632x=x32x=94.8g答:可以得到9.6g氧气,参加反应的高锰酸钾质量为94.8g。9.6g例314g红磷在16g氧气充分燃烧,生成五氧化二磷的质量是多少?解:设可生成五氧化二磷质量为X点燃4P+5O2===2P2O54×315×322×14214g16gX根据参加反应的磷和氧气的质量比为31:40,可以判断出氧气完全反应,应利用氧气的质量计算五氧化二磷的质量。今有氢气与氧气的混合气共20g,在密闭的容器中点燃,生成水18g,问参加反应的氢气与氧气的质量比是多少?原混合气体中氧气的质量可能是多少?变式训练解:2H2+O2===2H2043236XY18g(1)如果氢气完全参加反应,设氢气质量为X。4:36=X:18gX=2g氧气质量为20g-2g=18g。(2)如果氧气完全参加反应,设氧气质量为Y。32:36=Y:18gY=16g答:原混合气体中氧气的质量可能是18g或16g。点燃本节课你学会了哪些知识?收获了什么方法?还有什么疑惑吗?课堂达标1.把4.5g含杂质(杂质不与盐酸反应)的锌粒和足量的稀盐酸反应,待反应停止后,烧杯中物质的质量减少了0.1g。求:(Zn+2HCl===ZnCl2+H2↑)①参加反应的锌的质量。②这种锌粒中含锌的质量分数。解:设参加反应的锌的质量为X。Zn+2HCl===ZnCl2+H2↑652X0.1g65:2=X:0.1gX=3.25g×=72.2%答:①参加反应的锌的质量为3.25g。②这种锌粒中含锌的质量分数为72.2%。3.25g4.5g100%2.现有家庭食用碱样品12g(主要成分Na2CO3,其他成分不与酸反应),向其中加入某未知浓度的盐酸,生成气体的质量与加入盐酸的质量关系如下图。请计算:食用碱中碳酸钠的纯度是多少?变式训练解:设食用碱中碳酸钠的质量为X。Na2CO3+2HCl===2NaCl+H2O+CO2↑10644X4.4g①106:44=X:4.4gX=10.6g②×=88.3%答:食用碱中碳酸钠的纯度是88.3%。10.6g12g100%



















