


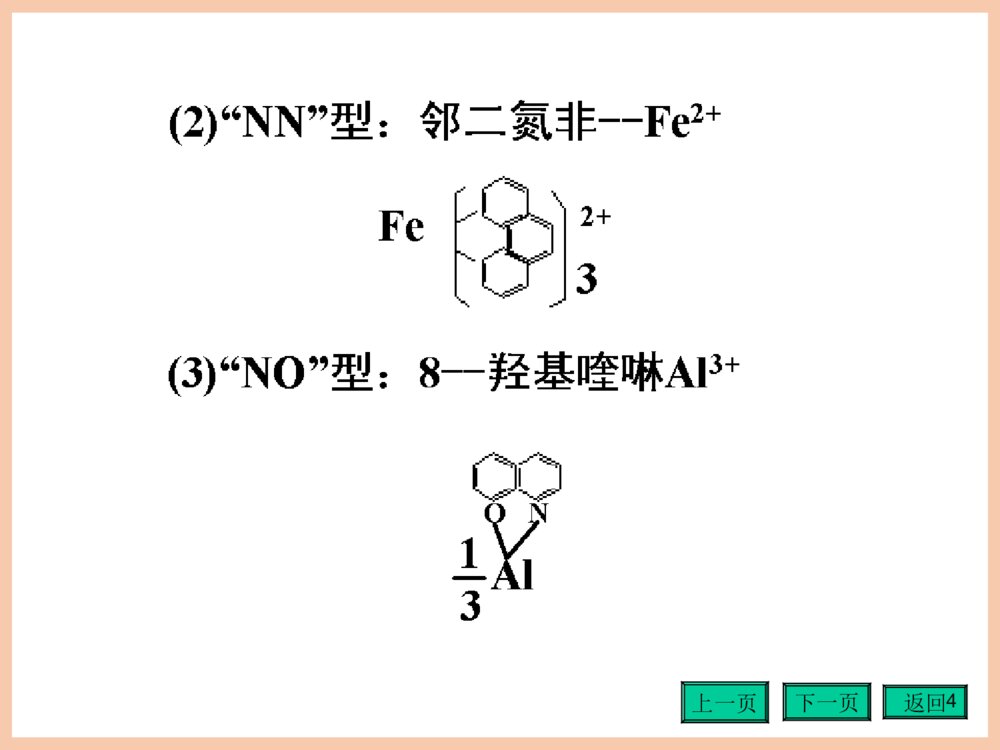





《《第四章配位滴定法》分析化学第四版PPT课件(共152页)》是由用户上传到老师板报网,本为文库资料,大小为4.08 MB,总共有152页,格式为ppt。授权方式为VIP用户下载,成为老师板报网VIP用户马上下载此课件。文件完整,下载后可编辑修改。
- 文库资料
- 152页
- 4.08 MB
- VIP模板
- ppt
- 数字产品不支持退货
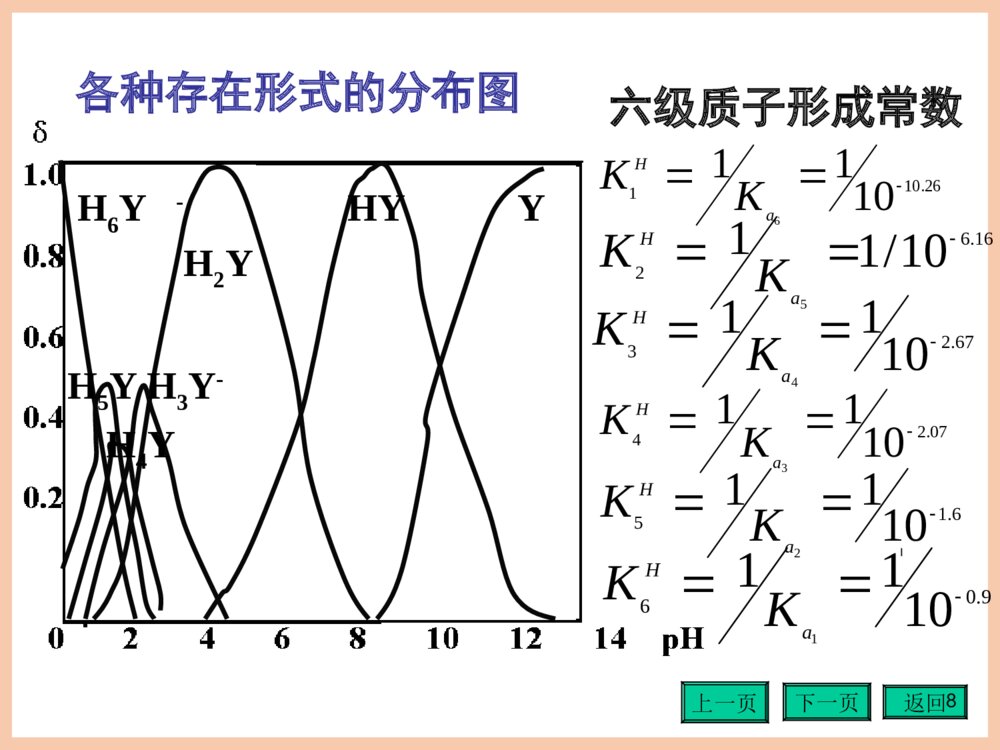
下一页上一页返回第四章:配位滴定法4-1概述4-2配位平衡4-3副反应系数和条件形成常数4-4配位滴定法基本原理4-5金属离子指示剂4-6提高配位滴定选择性的途径4-7配位滴定方式及其应用习题下一页上一页返回下一页上一页返回4.1:概述 一.分析化学中的配合物(Complexometry):具有空轨道的中心离子作为电子对的接受体,d轨道与含有孤对电子的配位原子作为电子对的给予体,配位体形成配位键. 1.简单配合物:Cu(NH3)42+ Cu2+:中心离子,d轨道未充满,电子对接受体; N:配位原子,含有孤对电子,电子给予体; NH3:配位体,络合剂; 4个N:配位数;4:配位体数.下一页上一页返回3 无机配合物很多,但配位反应用于分析的并不多,原因:K小,且逐级形成。 2.螯合物(Complex):多基配体组成,配位能力强,易行成稳定的多环状的可溶性配合物,常见的含有N,O,S配位原子的有机配体可用做滴定剂和掩蔽剂.下一页上一页返回4下一页上一页返回5 二.配位滴定对配位反应的要求 1.K形足够大; 2.配合比固定; 3.反应速度快; 4.有合适的指示剂;Efhylenediaminetetraaceticacid下一页上一页返回6 三.EDTA及EDTA配合物 1.EDTA-己二氨四乙酸(二钠盐)最常见的氮羧螯合剂:平面图 两个羧酸基上的H转移至N原子上,形成双极离子,它的两个羧基可再接受H+ 形成H6Y2+,所以EDTA相当于六元酸.下一页上一页返回7 (1)含有:氨基—NH22个; 羧基—COOH4个 六个配位原子,且均被c原子隔开 (2)六元酸H6Y2+有六级离子平衡Ka1=10-0.9;Ka2=10-1.6;Ka3=10-2.0;Ka4=10-2.67;Ka5=10-6.16;Ka6=10-10.26. (3)七种存在形式随pH变化H6Y2+H5Y+H4YH3Y-H2Y2-HY3-Y4- pKa1pKa2pKa3pKa4pKa5pKa6pH下一页上一页返回816.6210/115aHKK67.2310114aHKK07.2410113aHKK9.0610111aHKK6.1510112aHKK26.10110116aHKK 各种存在形式的分布图H6Y-HYYH2YH5YH3Y-H4Y六级质子形成常数下一页上一页返回9 提问:已知cEDTA=0.02mol/L 推算 pH=6.0时和1.0,4.4各形体的浓度. 1)pH=6.0δH2Y=0.50(50%) δHY=0.50(50%) [H2Y]=cδH2Y=0.02×0.5=0.01mol/L [HY]=cδHY=0.01mol/L 2)pH=1.0δH6Y=δH5Y=0.5 所以pH<1时H6Y为主要形式[H6Y]=[H5Y]=0.01mol/L下一页上一页返回10 3)pH=4.4δH2Y=0.95 [H2Y2-]=cδH2Y=0.02×0.95=0.02 推论:Na2H2Y·2H2O→Na++H2Y 溶液pH=4.4 (4)H4Y:EDTA溶解度小0.02g/100mlH2O22c℃EDTA=7×10-4mol/L Na2H2Y溶解度大11.1g/100mlH2O22c℃EDTA=0.3mol/L配成0.01~~0.02mol/L的水溶液pH=4.4下一页上一页返回11 2.EDTA的分析特性及配合物特性 (1)与众多金属离子形成稳定的多个五元环配合物如图EDTA结构式:(左图)EDTA-M螯合物 的立体结构NMNOOOOOOOO2-下一页上一页返回12 二.三.四价离子形成MYlgK>15 碱土 lgK8-11 过渡元素 lgK>20 (2)配合比固定而简单,多数为1:1型,少数为2:1型(如:Mo(Ⅴ)) 计量数为1,通式略电荷 写成通式: M+Y=MY (3)配合物带电荷且易溶于水 (4)反应快,滴定终点易判断下一页上一页返回13 (5)离子带色,形成MY也带色且颜色加深,可定性分析CuYNiYCoY(深蓝)(蓝绿)(玫瑰)MnYCrYCr(OH)Y2-(紫红)(深紫)(蓝)FeYFe(OH)Y2-(黄) (褐)下一页上一页返回14 四.配位滴定法分类: 1.汞量法→Cl-,SCN- 2.氰量法→Ag-,Ni2+ 3.EDTA法→金属离子Mn+ 4.其它螯合滴定法下一页上一页返回154.2:配位平衡 一.配合物的形成常数(稳定常数)(Stabilityorformationconstant) K形=K稳 1 累积形成常数β=K形=—— K离下一页上一页返回16 1.多配体无机配合物Cu--NH3下一页上一页返回17 根据平衡常数推导出三种常数的关系:[Cu(NH3)2+] β1=————————=K形1 [Cu][NH3] 配合物形体分布: [Cu(NH3)2+]=β1[Cu][NH3][Cu(NH3)22+] β2=——————=K形1K形2 [Cu][NH3]2 配合物形体分布: [Cu(NH3)22+]=β2[Cu][NH3]2下一页上一页返回18[Cu(NH3)32+] β3=———————=K形1K形2K形3 [Cu][NH3]3 配合物形体分布:[Cu(NH3)32+]=β3[Cu][NH3]3[Cu(NH3)42+] β4=——————=K形1K形2K形3K形4 [Cu][NH3]4 配合物形体分布:[Cu(NH3)42+]=β4[Cu][NH3]4 通式:M+L=ML [ML] [M][L] K形=———=β1 K离=——— [M][L] [ML]下一页上一页返回19 MLn-1+L=MLn [MLn][MLn][MLn-1][L] K形=————βn=———K离=————— [MLn-1][L][M][L]n[MLn] 1 1 β1=K形1——— β2=K形1K形2———— K离1 K离1K离21 β总=K总形=———K总不稳或lgβn=in(lgβi)=1∏∑下一页上一页返回20 2.有机配体:配位数为1如EDTA Ca2++H2Y2-=CaY2-+2H+ [CaY] K形=K稳=———— [Ca][Y]1 =1010.69=β=——K不稳 lgK形=pK离介下一页上一页返回21 二.溶液中各级配合物的分布: 1.Cu(NH3)42+配合物的分布Cu2+_Cu(NH3)42+nCu(NH3)22+Cu(NH3)2+Cu(NH3)32+下一页上一页返回22 ①Cu2+与NH3逐级形成配合物 ②没有一种配合物的存在形式的分布系数接近1_ ③n在变,配比在变 所以,不能用NH3作配合剂滴定Cu2+下一页上一页返回23 [例1]在铜氨溶液中,当氨的平衡浓度为[NH3]=1.00×10-3mol/L时:计算5种形体的分布系数(已知:Cu--NH3配合物lgβ1--β4分别为:4.13,7.61,10.48,12.59) [解] 为了便于计算 可设cT cT=[Cu2+]+[Cu(NH3)2+]+[Cu(NH3)22+] +[Cu(NH3)32+]+[Cu(NH3)42+]以下同)下一页上一页返回24[Cu][Cu2+]δCu=———=————cCucT [Cu(NH3)2+] δ[Cu(NH3)]=——————c β1[NH3]13.49 =—————=————=15.1% cT89.32下一页上一页返回25 β2(NH3)2 δ[Cu(NH3)22+]=———— cT 40.70 =———=45.6% 89.32 30.20 δ[Cu(NH3)32+]=———=33.8% 89.32 3.89δ[Cu(NH3)42+]=———=45.6% 89.32下一页上一页返回26 2.汞量法 Hg2+-Cl-体系的lgKi如下: lgK1=6.74,lgK2=6.48,lgK3=0.85,lgK4=1.0 因K2与K3差别较大.当lg[Cl-]为-5〜-3时,δHgCl2≈100% 故可用Hg2+滴定Cl-,sp生成HgCl2 如图:(见下页)下一页上一页返回27Hg2+HgCl2_HgCl2nHgCl42-HgCl+HgCl3-平均配位数为2Cl在一定范围内n不变下一页上一页返回28 三.平均配位数 用EDTA作滴定剂时,配合比为1:1,配位数为1_ 用n表示M离子的络合配位体的平均数,M的生成函数n1iiin1iiiML]L[1]L[ic]L[cn下一页上一页返回29 如[例1] Cu(NH3)42+β4[NH3]4 1×13.49+2×40.74+3×30.20+4×3.89 =————————————————— 89.32 201.13 =————=2.25(平均配位数不定)见下图 89.32n是[L]的函数下一页上一页返回30 四.金属离子缓冲溶液 M视为路易斯酸Y视为路易斯碱 与酸碱缓冲溶液不同的是,以总反应构成缓冲体系. cY[MY] pM=pK离+lg———[M]=K离———cMY[Y]下一页上一页返回31 对n配位的多配体络合物MLn,其公式为: cLn[ML] pM=pK离+lg———[M]=K离———cMLn[L]n 或用形成常数表示 [Y] pM=lgKMY+lg——— [MY][L]npM=lgKMLn+lg———[MLn]应用于解释在配位滴定中曲线形状,当加入少量Y,pM基本不变,而在+0.1%有突跃下一页上一页返回32 根据平衡移动原理:副反应的存在,使主反应能力降低,配合物稳定性下降;引入副反应系数α,并用条件形成常数K\'MY来表示受副反应影响时的MY的稳定程度.4.3:副反应系数和条件形成常数一.副反应及副反应系数1.主反应与副反应下一页上一页返回33 2.副反应系数:总浓度c或[Y\']与平衡浓度的比值:c[Y\'] α=——=—— [Y][Y] 林邦建立的处理复杂平衡体系的简易方法 此处 EDTA=Y下一页上一页返回34 二.络合剂(滴定剂)Y的副反应系数 定义式: [Y\'](平衡时各种形体的总浓度) αY=———[Y](平衡时游离Y的浓度)[Y\'][Y]+[HY]+....+[H6Y]+[NY] αY=——=————————————[Y][Y] [Y]+[HY]+...+[H6Y][Y]+[NY] =——————————+———— [Y][Y] =αY(H)+αY(N)-1下一页上一页返回35 1.(EDTA的)酸效应与酸效应系数 定义式: [Y\'][Y]+[HY]+......+[H6Y] αY(H)=———=————————— [Y][Y] =1+β1[H]+β2[H]2+……+β1[H]6下一页上一页返回36 由于[H+]的影响使Y参与主反应的能力降低的效应称为酸效应,用αY(H)来衡量 EDTA是多元酸,如同δ一样δY(H)是[H+]的函数: 1 [H+][H+]2[H+]3 αY(H)=——=1+——+———+———— δY Ka6Ka6,5Ka6,5,4[H+]4[H+]5[H+]6+————+—————+—————Ka6,5,4,3Ka6,5,4,3,2Ka6,5,4,3,2,1 =1+β1[H+]1+β2[H+]2+......+β6[H+]6下一页上一页返回37**[Y],[Y\'],cY\'δY\'αY(H)之间的关系** 1.[Y\']:平衡时未与M配位的EDTA总浓度;[Y]:游离浓度;cY:EDTA原始浓度. 2.因为[Y\']>[Y],所以αY(H)≥1;δY≤1 3.[H+]高,[Y]愈小,δY愈小,αY(H)愈大,副反应愈严重,K\'MY愈小;反之则相反 4.当[Y]=[Y\'],αY(H)=1,lgαY(H)=0无副反应发生.下一页上一页返回38 [例1]计算pH=5.0时EDTA的αY(H),lgαY(H) [解] 已知EDTA的Ka1----Ka6为: 10-0.9,10-1.6,10-2.07,10-2.74,10-6.24,10-10.34 质子化常数K1-----K6: 1010.34,106.74,102.75,102.07,101.6,100.9 累积质子化常数β1----β6: 1010.34,1016.58,1019.33,1021.00,1023.0,1下一页上一页返回39 ∴αY(H)=1+β1[H+]+β2[H+]2+...+β6[H+]6 =106.60 则:lgαY(H)=6.60下一页上一页返回40 [例2]求不同pH值下[Y]=?([Y\']=10-5mol/L) (1)pH=1.0查表:lgαY(H)=18.0[Y\'][Y]=——=10-23.0mol/LαY(H) (2)pH=5.0 lgαY(H)=6.45 [Y]=10-11.45mol/L (3)pH=12.0lgαY(H)=0.0110-5 [Y]=——=1无副反应100.01下一页上一页返回41 2.(EDTA的)共存离子效应与共存离子效应系数 溶液中共存离子也能与Y反应,从而影响了Y参与主反应的能力,影响的程度用αY(N)表示:[NY]KNY=———[Y][N][Y]+[NY] αY(N)=——————=1+KNY[N][Y]下一页上一页返回42 3.EDTA的总副反应系数αY 当体系中既有共存离子N,又有酸效应时的副反应系数为: αY=αY(H)+αY(N)-1下一页上一页返回43 [例3]在pH=6.0时,滴Zn2+,试计算当cY=cZn=cCa=0.010mol/L时,αY(Ca)=?αY=? (1)pH=6.0时lgαY(H)=4.65 αY(Ca)=1+KCaY[Ca]sp=1+1010.69·0.010=108.69 (2)αY=αY(H)+αY(Ca)--1=104.65+108.69-1 ≈αY(Ca)=108.692CaspCCa下一页上一页返回44 [例4]在pH=1.5时,滴定Fe3+,已知: cY=cFe3+=cCa=0.010mol/L,求αY(Ca)和αY [解]αY(H)=1015.55αY(Ca)=108.69 αY=αY(H)+αY(Ca)-1=1015.55+108.69-1 ≈αY(H)=1015.55下一页上一页返回45 三.金属离子M的副反应及副反应系数 1.副配位效应与配位效应系数:缓冲剂,掩蔽剂等;另一配体L的存在与M发生副反应使M参与主反应的能力降低的效应,用αM(L)表示:下一页上一页返回46 [M\'][M]+[ML]+...+[MLn] αM(L)=———=—————————— [M][M] =1+β1[L]+β2[L]2+..........+βn[L]n 游离金属M的分布函数δ与α互为倒数 1[M] δM——=———— αM[M\'] cM [M]游=δM·[M\']=δMcM=———— αM(L)下一页上一页返回47 [例5]在0.10mol/L的AlF63-溶液中,含有F-为[F-]=0.010mol/L时,求[Al3+]=? [解]已知:AlF63+的各级累积常数为: 106.1,1011.5,1015.0,1017.7,1019.4,1019.7 [Al\']=[Al3+]+[AlF2+]+[AlF2+]+[AlF3] +[AlF4-]+[AlF52-]+[AlF63-] =cAl=0.10mol/L下一页上一页返回48 αAl(F)=1+β1[F]+β2[F]2+...........+β6[F]6 =109.93 [Al\']cAl0.10 故:[Al3+]=————=———=——— αAlαAl(F)109.93=10-10.93mol/L F掩蔽Al3+很完全下一页上一页返回49 2.M的总副反应系数αM:溶液有多种配体存在并与M配位,对M的影响用αM表示αM=αM(OH)+αM(L)+...+αM(L)n-(n-1)下一页上一页返回50 [例6]在pH=10.0,cZn=0.010mol/L,如果含[NH3]=0.10mol/L求αZn=? [解]pH=10.0αZn(OH)=102.4 已知:Zn(NH3)42+的lgβ1--lgβ4: 2.37,4.81,7.31,9.46 故:αZn(NH3)=1+β1[NH3]+...+β4[NH3]4 =105.49 αZn=αZn(NH3)+αZn(OH)-1=105.49+102.4-1 ≈αZn(NH3)=105.49下一页上一页返回51 [例7]现已知在cZn=1.0×10-2mol/L的溶液中,[NH3]=0.17mol/L(pH=10),cCN=0.03mol/L 计算αZn=?[Zn2+]=?有无Zn(OH)2生成 解:已知 HCN的pKa=9.20 Zn(CN)42-的lgβ4=16.7 KspZn(OH)2=10-15.3 Zn(NH3)42+的lgβi:2.37,4.81,7.31,9.4 αZn=αZn(NH3)+αZn(CN)+αZn(OH)-2下一页上一页返回52 1)αZn(NH3)=105.94Ka (2)[CN-]=δCN-·c=————=0.026mol/L[H+]+Ka 3)αZn(CN)=1+β4[CN]4=1010.36 4)查αZn(OH)=102.4 5)αZn=105.94+1010.36+102.4--2=1010.36cZn (6)[Zn]=———=10-12.36αZn 7)[Zn2+][OH-]2=10-20.36lgK\'CaY)下一页上一页返回58 结论:[H+]↑,pH↓,lgαY(H)↑,lgK\'MY↓ 主反应能力下降;[OH-]↑,pH↑,lgαM(OH)↑,lgK\'MY↓ 主反应能力下降. 因为αY>1,αY>1,所以K\'MY6能准确滴定下一页上一页返回69 δMg=([Mg]/csp)×100%=0.074% 游离Mg所占的百分数为0.074%, MgY完全度为99.93% (2)pH=5.0,lgαY(H)=6.45 lgK\'MgY=8.70-6.45=2.25<6不能准确滴定 [Mg]sp=5.2×10-3mol/LδMg=52% 说明只有48%参与配位,故不能准确滴定L/mol104.710Kc]Mg[:sp613.5MgYMspsp下一页上一页返回70 四.配位滴定中酸度的控制 1.最高允许浓度(单一离子滴定而言) 已知:c0=0.02mol/L,lgcMK\'MY≥6, 则有lgK\'MY≥8 若αM=1,则lgK\'MY=lgKMY-lgαY(H)≥8 最大值对应的pH值为滴定的最高酸度查对应的pH值下一页上一页返回71 2.最低酸度: 若αM(L)=1,则pH高限即为用Ksp 求M(OH)n↓时[OH-]=? 例题见下页下一页上一页返回72 [例2]EDTA滴Zn2+时,求pH的低限和高限 (lgKZnY=16.5,pKsp=15.3) [解]orpZnsp=(pCZn+lgK\'ZnY) (1)lgαY(H)=16.5-8=8.5,查P330表pH低=4.0 低于4.0不能滴定 pH高=14.0-6.7=7.3 高于此值Zn(OH)2↓7.62sp10]Zn[K]OH)[2(12spK\'C[Zn]ZnYZnspsp下一页上一页返回73 3.缓冲溶液在配位滴定中的应用 M+H2Y2-=MY+2H+ 不断产生[H+]↑,αY(H)↑,K\'↓ [H+]也影响指示剂的变色,故需加缓冲溶液维持一定的pH下K\'不变 (1)pH<2强酸(Bi3+,Fe3+,HNO3) (2)pH>12强碱(Ca2+,NaOH,Mg(OH)2↓) (3)pH4-6HAc-NaAc (4)pH8-10NH3-NH4Cl下一页上一页返回74 4.酸效应曲线的应用意义 (1)查滴定M时的pH低限; (2)利用lgαY(H)与lgKMY的关系定性考察M与N分别滴定时pH(分为酸性组,中性组,碱性组) (3)控制H+选择滴定时lgαY(H)→pH值下一页上一页返回75下一页上一页返回764.5:金属离子指示剂 一.作用原理:一种与金属离子生成有色化合物的显色剂来指示滴定过程中金属离子浓度的变化,这种显色剂-------金属指示剂 是酸碱染料:H++In-=HIn碱色酸色有αIn(H) 有酸度范围下一页上一页返回77 1.铬黑T(EBT)H3In三元酸 (1)酸碱平衡关系: (2)滴定中作用原理Mg2++In=MgIn(红色)络合反应MgIn+Y→MgY置换反应In(蓝色)酸碱反应→HIn用于指示ZnCdPbHgInMgCa(pH=7.0--11.0)下一页上一页返回78 2.二甲酚橙(XO)H6In (2)络合反应M---In红色络合物,所以XO只能用于pH<6.3时指示剂pH1--2Bi;pH2--3.5Th; pH5----6Cd,Co,Cu,Pb,Zn,La下一页上一页返回79 3.K--B指示剂:酸性络兰K与萘酚绿B混合比例指示剂pH=10--12 pH=10测Mg,Zn,Mn;pH=12测CaCu,Co,Ni 4.PAN吡啶偶氮类显色剂: 使用范围pH2---12(Al,Cu,Zn)下一页上一页返回80 二.金属离子指示剂应具备的条件 1.MIn与In的颜色要有明显的差别 2.lgK\'MY>lgKMIn\',ep时易发生置换反应若lgKMIn>lgKMY,ep时不变色,称为指示剂的封闭 3.M与In反应灵敏,迅速,可逆性好.下一页上一页返回81 三.理论变色点和终点误差 1.MIn的条件稳定常数 [MIn][MIn]KMIn KMIn\'=————=—————=——— [M][In\'][M][In]αIn(H)αIn(H) lgK\'MIn=lgKMIn–lgαIn(H)下一页上一页返回82 2.理论变色点pMt(酸碱滴定中的pHep) [MIn] 已知:KMIn\'=——— [M][In] [MIn] 11 当———=1时 KMIn’=——=——[In’] [M][Mt] pMt=lgKMIn’=lgKMIn-lgαIn(H)=pMep 可以计算不同pH下的pMt值下一页上一页返回83 pMlgKMIn\'+1In色 lgKMIn-1lgKMgY但lgKCa--EBTpMgsp负误差且pH越小,Et越负 当pH>9.84时pMgeplgKMY,ep不置换不变色 消除:1)干扰因素引起的,加掩蔽剂 2)被测离子本身引起的,改变滴定方式 2.僵化:M--In在水中溶解度小, 使得Y与MIn变换慢. 消除:1)加入有机溶剂,增大溶解度 2)加热,加快反应速度,趁热滴定下一页上一页返回95 五.常用金属离子指示剂一览表EBT7-10红-蓝MgZnCd1:100NaCl PbMnXO<6.3红-黄BiTh(1-3)0.5%水溶液 ZrO(1)ZnPbCdHg(5-6)PAN2-12红-黄BiTh(2-3)0.1%乙醇液 CuNi(4-5)K-B8-13红-蓝MgZn(10)1:100NaCl Ca(13)磺基水扬酸2—3紫红-无色Fe2+2%水溶液钙试剂10-13Ca1:100NaCl下一页上一页返回964.6:提高配位滴定选择性的途径 一.选择滴定的可能性 M,N离子共存,能否滴定M而N不干扰,lgKMY>KNY的差有多大,能实现选择性滴定和分布滴定.可能性判断:若:Et=+0.1%,△pM=+0.2,lgcspMK\'MY≥6下一页上一页返回97 则有如下推导: lg(αY(H)+αY(N))有三种可能: αY(H)>αY(N);αY(H)<αY(N);αY(H)=αY(N) 求N干扰最严重的极限条件: αY(N)>>αY(H) αY(N)+αY(H)=αY(N)=KNYcNsp)lg(lgKclg6lglgKclgKclg)N(Y)H(YMMYspMYMMYspMMYspM下一页上一页返回98 若αM=1 则有: 若:Et≤0.3%,△pM=±0.2 则△lgKC≥56cKlgKclgKclgspNNYMYspMMYspM6lg6lg6lglglglglg00KCKcKcKccKKKcccNYNMYMNMNYMYMYspMspMspN所以:或:则:因为:下一页上一页返回99 二.选择滴定中的酸度控制 单一离子最高酸度lgαY(H)=lgKMY–8,有条件的cM0=0.020mol/L,混合离子滴定指示剂非专属性的,滴完M后,In又与N显色,无法指示M的ep,所以必须考虑指示剂的酸效应. 1.要求: lgK\'MY最大,△lgKC≥5,Et≤0.3%下一页上一页返回100 2.最高酸度:11 αY(H)=—αY(N)=—(1+[N]KNY)1010 故:lgαY(H)=lgαY(N)-1=lgKNYcNsp-1 此式为N干扰时,滴定M的pH高限,或滴M的最低酸度,也即N的干扰警戒限,大于此值,N与指示剂、Y配位.下一页上一页返回101 [例1](P215)设计XO指示剂滴Pb2+,Bi2+混合液的方案.设△pM=0.2,Et=0.3%,cPb=cBi=0.02 (lgKBiY=27.94,lgKPbY=18.04) (2)可利用酸效应选择滴定Bi,而Pb不干扰 最高酸度:lgαY(H)=lgKBiY-lgK\'BiY=20.94 查表P330pH=0.559.9KcKclg1][PbYspPbBiYspBi)(解下一页上一页返回1026.104.151lglg)(pHPcKspPbPbYHY查表最低酸度:9.2pH87.10)clg5(KlglgPb)3(spPbPbY)H(Y2最高酸度:测54.7pH102cK]OH[46.6sp最低酸度:330下一页上一页返回103(4)因为XO在pH<6.3使用,所以在pH=1滴Bi;在pH=5--6滴Pb书P117:Zn-Mg混合液能否滴定Zn?∆lgKC>6若Zn-Ca混合液能否滴定Zn?∆lgKC>5若XO指示终点:Zn-Mg体系∆pM=0.15,Et=0.02%,Zn-Ca体系∆pM=1.15,Et=4%,干扰。提高酸度,增大αIn(H)在pH4.8-5.0时滴定,∆pZn=0.25,Et=0.3%下一页上一页返回104 三.利用掩蔽剂提高配位滴定的选择性 当∆lgK<5,不能利用酸效应来消除干扰 可以利用降低[N],使αY(N)减小,加掩蔽剂 可以沉淀,降低游离N 可以氧化还原,改变价态,从而改变KNY,提高选择性.下一页上一页返回105 1.配位掩蔽法 αN(A)→→掩蔽指数:使KNY降低αN(A)倍 增大αN(A)提高掩蔽效率,从而达到选择性滴定M的目的.NYANspNNYNYKcKN)()(1][1下一页上一页返回106 [例2]溶液含mAl3+=27mg,mZn2+=65.4mg,能否用0.020mol/L的EDTA滴Zn2+; 若加入1gNH4F,调pH=5.5,XO指示剂,能否滴Zn2+Et%=? [解]设Vep=100mLL/mol010.0V1000MmcL/mol010.0V1000MmcspspZnspAl23时:下一页上一页返回107 (2)加入1gNH4F→AlF63- lgβ1--β6: 6.13 11.15 15.0 17.76 19.32 19.84形成AlF63-络和物,若先以AlF52-为主要形体计算 (cV)F-5(cV)Al [F-]sp=—————— Vsp =0.27-5×0.01=0.22mol/LZn52.0)23.16()25.16(cKlgcKlg)1(spAlAlYspZnZnY故不能选择滴下一页上一页返回108(3)pH=5.5αF(H)=1+β1[H+]=1+103.18×10-5.5=1[F-]sp故:[F-]游=———=0.22mol/LαF(H) (4)αAl(F)=1+β1[F]+β2[F]2+......+β6[F]6=1016.30L/mol10c]lA[]Al)[5(3.18)F(AlspAl)F(Al331K]Al[1)6(YAl)H(Y下一页上一页返回109 (7)αY=αY(H)+αY(Al)-1=αY(H)=105.50 (8)lgK\'ZnY=lgKZnY-lgαZn-lgαY=11.05.6)pcK(lg21P)10(Zn60.920.11Kclg)9(spZnZnYZnsp2ZnYspZn能准确滴定02.0%E)12(8.05.67.5pZnpZnpZn)11(tspep下一页上一页返回110 尽管△pZn>0.3.但K\'大,所以Et小 pH>3.2时,F-用于掩蔽Al3+ pH>9.3时,CN-用于掩蔽Zn2+,Cu2+下一页上一页返回111 常用的掩蔽剂: (1).氟化物(NaF,NH4F) pH=4--6掩蔽Al3+,Ti4+,Sn4+ pH=10掩蔽Mg,Ca,Ba (2).氰化物:pH>9.31掩蔽 Cu2+,Ni2+, Co2+,Hg2+,Cd2+,Ag+,Zn2+ 不能与CN-配合的Ca2+,Mg2+,Pb2+,RE3+ 能被甲醛解蔽的氰化物:Zn2+,Cd2+下一页上一页返回112 2.沉淀掩蔽法:△LgKc<6,不能利用酸效应分步滴定,加入沉淀剂降低cN [例3]白云石中Ca,Mg的测定 (1)Ca+Y=CaYV1 MgPH>12Mg(OH)2↓CaOcV1———1000 CaO%=—————×100mS下一页上一页返回113MgOc(V2-V1)———1000 MgO%=————————×10025.0mS——250 该法的缺点: (1).沉淀溶解大时,掩蔽效率不高; (2).共沉淀现象使准确度受影响; (3).有色沉淀影响终点观察. 但沉淀掩蔽 操作简便下一页上一页返回114 3.氧化还原掩蔽法:改变价态,而改变KMY使△lgK>6 pH=1.0滴定Bi3+,Fe2+不干扰; 再调pH=2-3滴Fe3+下一页上一页返回115 pH=2.5滴Fe3+lgK=25.1 pH=5滴Zn2+lgK=16.5下一页上一页返回116 4.利用选择性解蔽剂 (1)释放出Y:Al3++TiO22+混合液+EDTA→AlY(TiY) TiYTiF42- →AlY→Ti---苦 +Y→ZnY VTi量+NaF→Zn滴+苦杏仁酸下一页上一页返回117 (2)释放出M下一页上一页返回118 5.选择其它滴定剂 (1)EGTA(乙二醇二乙醚二胺四乙酸) 同族元素MgCaSrBa lgKM--EGTA5.2110.978.508.41 lgKM--EDTA8.710.698.737.86 可利用EGTA掩蔽Ca,用EDTA滴定Mg下一页上一页返回119 (2)EDTP(乙二胺四丙酸) 过渡元素CuZnCdMn lgKM--EDTP15.47.86.04.7滴Cu(Zn中Cu) lgKM--EDTA18.816.516.4613.87 (3)无机掩蔽剂 CN-Cu,Zn,Co,Hg,Ni,Cd,Ag, Fe2+,Fe3+ F-Al,Ti,Zr,Sn,Th下一页上一页返回120 I-Hg,Cd,Bi,Ag,Pb C2O42-Fe3+,Al3+ (4)有机掩蔽剂 OO配体 pH=5--6Al,Fe,Be,Pd NN配体 pH=5–6 Fe2+,Cu,Ni,Zn, Cd,Hg,Co,Mn SS配体SN配体 SO配体磺基水扬酸Fe,Al ON配体Fe,Al,Ti,Sn,Mn下一页上一页返回1214.7:配位滴定方式及其应用 一.直接滴定法(DirectTitration) 满足的条件: 1.lgcMK\'MY≥6 2.反应速度快 3.有变色敏锐的指示剂lgKMY>>lgKMIn 4.在测定条件下M不水解沉淀下一页上一页返回122 Bi2+1HNO3XO红--亮黄Fe3+2HCl磺基水扬酸紫红--无Cu2+3--10HAcNaAcPAN/乙醇`80-90℃黄--紫红 ZnPb5--6(CH2)6N4XO红--黄Mg10NH3-NH4ClK—B酒红--蓝Ca10--13NaOHEBT酒红--蓝下一页上一页返回123 二.返滴定法(BackTitration) 1.缺乏合适的指示剂,或M对指示剂封闭 2.M与Y反应慢 3.M易发生水解等副反应 Al3+封闭XO,与Y反应慢,易水解成多核羟基化合物 采用返滴定测Al下一页上一页返回124 三.置换滴定(SubtitutionTitration) 1.混合离子相互干扰时,提高选择性滴定 2.ep指示剂变色不敏锐时,改善变色敏锐性 3.MY配合物不稳定,反应不稳定下一页上一页返回125 (一)置换出金属离子 AgY不稳定lgK7.32,但Ag+加入Ni(CN)42-溶液中,发生置换反应 nAg=2nNi=2nY下一页上一页返回126 (二)置换出EDTA 测白金中Sn: Mg--EBT灵敏,滴Ca时加入MgY发生置换反应下一页上一页返回127 四.间接滴定法(IndirectTitration) 不与EDTA发生反应的离子,如Na+ Na++醋酸铀酰锌→NaAc·Zn(Ac)2·3UO2(Ac)2·9H2O 测P→PO43-→MgNH4PO4↓ →Mg2++EDTA过量→MgY→Mg标下一页上一页返回128P(cV)Y-(cV)Mg——1000 P%=—————————×100mS1P2O5(cV)Y·—·——21000 P2O5%=—————————×100mS下一页上一页返回129 五.EDTA标准溶液的配制与标定 1.配制:Na2H2Y·2H2O.(372.2g/mol) 配成0.01--0.05mol/LpH=4--5(H2Y2-)372.2 粗配mEDTA=0.02×250mL×———1000 溶解盛于朔料瓶或硬质玻璃瓶中(软质玻璃瓶易形成CaY)下一页上一页返回130 2.标定:纯金属ZnPbCuZnOBi(99.9%)pH=5--6XO CaCO3,MgSO4·7H2OpH=10K--B为减小方法误差,标定与测定条件必须相同,如测白云石中CaO采用CaCO3标定EDTA 测Al合金,Bi—Pb混合液用纯Zn标定CaCO3 mCaCO3=cEDTA·VEDTA·———=0.04--0.06g1000下一页上一页返回131称大量m×10→250mL容量瓶→25.00/250mL 3.标定结果讨论25.00mCaCO3·———250 cEDTA=————————M——VEDTA1000 (1)若配制EDTA蒸馏水中含少量Ca,Mg,用基准CaCO3标定EDTA浓度cEDTAc小偏低,有效浓度变小下一页上一页返回132 (2)若用纯Zn标定EDTA,则正常无影响 (3)用CaCO3标后的EDTA测水的硬度结果c小,V大误差抵消 (4)用Zn标后的EDTA在pH=10测水硬度结果偏高(部分Ca也消耗EDTA) 总硬度CaOmg/L (cV)EDTAMCaO =——————×1000(ppm)Vml下一页上一页返回133 [例1]计算pH=5.00,[F-]=1.0×10-3mol/L,[Mn2+]=0.0100mol/L的溶液中AlY的条件常数? [解]已知:lgαY(H)=6.45lgKMnY=13.87 αY(Mn)=1+KMnY[Mn2+]=1+1013.87×10-2.00=1011.87 则αY=αY(H)+αY(Mn)—1(约)=1011.87下一页上一页返回134 又因为:Al3+--F的各级配合物的lgβ依次为:6.13,11.15,15.00,17.75,19.37,19.84αAl(F)=1+β1[F]+β2[F]2+.......+β6[F]6=106.24 则αAl=αAl(F)+αAl(OH)-1=106.24 所以: lgK\'AlY=lgKAlY-lgαY-lgαAl=-1.8下一页上一页返回135 例2.用2.00×10-3的EDTA滴同浓度的Pb2+,已知pH=5.00,用XO作为指示剂,求Et%=?以及[S2O32-]ep=0.01时的Et%=? [解](1)lgK\'=18.04-6.45=11.59 0.7p30.7)pcK(lg21pp00.3pc100.12ccbPepspPbspbPspsp3spPb2又下一页上一页返回136 所以△PPb=7.0-7.3=-0.3Et%=-0.01 (2)有副反应时Pb----S2O32-配合物的 lgβ1=5.1lgβ3=6.4 αPb(S2O3)=1+105.1×10-2.0+106.4×10-2×3=103.1 lgK\'PbY=18.04-6.45-3.1=8.49 pPb’sp=5.75p△Pb’=3.9-5.75=-1.85 所以Et%=-13因为副反应,S2O32-的副配位效应所致.下一页上一页返回137习题 1.某含铅溶液中cNH3=0.20mol/LcCN-=0.03mol/L,pH=10.0,计算αZn(NH3)=?αZn(CN)=?查αZn(OH)=? 2.已知某含铅溶液,cAc-=0.5mol/L,pH=10.0,计算αPb(AC)=?查该pH下的αPb(OH)=?计算αPb值.已知Pb--Ac-络合物lgβ1=1.9,lgβ2=3.3. 3.在0.10mol/LNH3--0.10mol/LNH4Cl溶液中,能否以0.02mol/LEDTA准确滴定0.02mol/LZn2+?答案下一页上一页返回138 4.往浓度为0.0100mol/L的Zn2+Cd2+混合离子溶液中加入过量的KI,使终点时I-的游离浓度为0.5mol/L.在pH=5.5时,能否用等浓度的EDTA准确滴定Zn2+?若以二甲酚橙作指示剂,计算终点误差Et%=? 5.在pH=9.26,[NH3]+[NH4+]=0.2mol/L时,以0.02mol/LEDTA滴定0.02mol/LZn2+,计算化学计量点的pZn’和pZn. 6.pH=5.5,用0.020mol/LEDTA滴定0.20mol/L的Mg2+和0.02mol/LZn2+溶液中的Zn2+时,Mg2+是否干扰滴定,等计量点时pZn=?若以二甲酚橙作指示剂,计算终点误差Et%=?下一页上一页返回139 7.在pH=4.0的缓冲溶液中,酒石酸(H2R)总浓度为0.20mol/L,Pb2+的浓度为2.0×10-4mol/L,计算:(Ka1=10-3.04,Ka2=10-4.37,lgKPbY=18.04) (1)溶液中酒石酸根的浓度[R2-]=? (2)此溶液中Pb--EDTA络合物的条件稳定常数? 8.在pH=10,[NH3]终=0.1的溶液中,以0.02mol/L的EDTA滴定含有0.02mol/L的Zn2+和0.02mol/LAg+混合离子溶液中的Zn2+,问Ag+是否干扰? 9.欲要求终点误差在0.2%以内,△pM=0.38用2.0×10-2mol/LEDTA滴定等浓度的Bi3+的最低pH值应是多少?下一页上一页返回140 10.在pH=6.0时,用EDTA滴定Pb2+,溶液中的Al3+有干扰,问加入乙酰丙酮至过量0.1mol/L时,能否消除Al3+的干扰?已知乙酰丙酮与Pb2+不络合.EDTA和Pb2+、Al3+的浓度均为0.020mol/L. 11.现有含1.0×10-2mol/LCa2+和5×10-4mol/LPb2+的试液,计算用1.0×10-2mol/LEDTA滴定其中Pb2+DEpH低限. 12.测定无机盐中的SO42-含量,称取试样3.000g,溶解后,用容量瓶稀释至250毫升,用移液管吸取25.00毫升试液加入0.05000mol/LBaCl2溶液25.00毫升,过滤后,用0.05000mol/LEDTA17.50毫升滴定剩余的Ba2+,求SO42-%.下一页上一页返回141 13.在含0.10mol/LHAc和0.20mol/LNaAc及0.10mol/LCa2+的溶液中,能否以0.020mol/LEDTA准确滴定0.02mol/LPb2+? 14.分析铜锌镁合金,称取0.5000g试样,溶解后,用容量瓶配成100mL试液,取25.00mL,调节pH=6.0,以PAN作指示剂,用0.05000mol/LEDTA滴定到终点,用去37.03mL,另取25.00毫升试液,调节pH=10.0,加入KCN后,以EBT作指示剂,用同浓度的EDTA溶液滴至终点,用去4.10毫升,然后加入甲醛,再用EDTA滴定至终点,又消耗13.40毫升,求合金中Cu%、Zn%、Mg%下一页上一页返回142 15.滴定浩英石中ZrO2和Fe2O3含量时,称取1.000g试样,以适当的溶样方法制成200mL样品溶液,移取50.00mL样品溶液,调节pH=0.8,加入盐酸羟胺还原Fe3+,以二甲酚橙为指示剂,用1.000×10-3mol/LEDTA滴至亮黄色,耗去10.00mL,然后加入弄HNO3加热,使Fe2+氧化为Fe3+,并将溶液滴至pH=1.5再以磺基水杨酸作指示剂,用EDTA滴至黄色耗去20.00mL,计算ZrO2和Fe2O3的百分含量. 16.一含有Fe3+、Al3+、Zn2+(其浓度均为10-2mol/L)的溶液试设计一个以络合滴定方法测定上述元素的方案.(要求:写明测定的理论根据,主要步骤,主要条件,试剂即指示剂).下一页上一页返回143 17.如何分别测定Zn2+、Mg2+混合溶液中Zn2+以及Mg2+的含量.下一页上一页返回14411220.02molLEDTA25ml0.02molLPbPbpH5.0pH0.2pH?例18:用滴定溶液。若溶液的,如何控制溶液的在整个滴定过程中的变化不超过单位由缓冲容量意义:次甲基四胺基本不变,考虑改用六量的控制液还应有足够的缓冲容,此外,选择的缓冲溶络合也会降低与体系,因为,不能用滴为维持会降低。。酸度升高,为倍量的反应时将产生解:有关反应:pHKPbACACHACPb0.5pHKLmol04.0H2H2PbYYHPbPbY22MY122221d0.040.2molLd0.p2Ha2aaN)CH(2aa])H[K(]H[Kc3.2]H[K]H[K3.2246:下一页上一页返回145。和(溶液中加入即在物质的量为加入(用(代入上式解得将34622aHNO3462462N)CH(1N)CH(3.5a10.5mmolHNO5.6N)CHg4.1mlPbH25mmol5.6025.0K]H[]H[39.0nHNOHN)CHN)CHg4.1140025.039.0MVcmLmol39.0c10KLmol10]H[3462462下一页上一页返回1462212MgEBTpH9.0~10.51.010molLEDTAMg例19:此洛合滴定法测定时,通常以为指示剂。在的氨性溶液中进行,试以滴定同浓度为例。讨论酸度与终点误差的关系。)H(EBTEBTMgepspMgMgYsplgKlgpMg)pcK(lg21pMg愈大。愈大,产生正误差,反之为负误差。当。时的即曲线交点tspepspepepspEpHpMgpMg84.9pHpMgpMg84.9pHpHpMgpMg84.9pH下一页上一页返回147pHpMgsppMgeppMgEt/%94.864.4-0.46-0.79.55.094.9-0.19-0.159.75.175.09-0.08-0.059.85.215.19-0.02-0.019.95.245.290.050.03105.285.390.110.0510.55.385.820.440.2pMgsp及pMgep与pH的关系01234567891011pHpMgpMgsppMgep下一页上一页返回1481222222Pbsp0.020molLEDTAPbCaPb1CaPb?2PbpHP?3pH40.2PM例20:欲以的滴定同浓度的混合物中的。问()能否在存在下分步滴定()若能请求滴定的范围,化学计量点时的()若用二甲酚橙为指示剂时,最佳的值?()若此滴定有单位的出入,求由此产生的终点误差为多少?之间。范围在高限为故高限为水解酸度:查低限。的此为滴低限(最高酸度):范围。的)滴定(有可能分步滴定。则判断分步滴定可能性。根据)已知解:(0.7~0.4pH0.7pHpH.Lmol1010210]Pb[K]OH[pH0.4pH7.8lgpHPb101010K]Ca[1pHpHPb23.77.100.18KlgKlgKlg6Klgccc110.727.152sp)H(Y27.87.102CaY2)Ca(Y)H(YCaYPbYCaPbEDTA下一页上一页返回1497.5)0.23.9(21)pcK(lg21pPb...3.97.80.18lgKlgspPbYsp)Ca(YpbY故此时:值。为最佳滴定时,即故。是终点与计量点相等处为指示剂的最佳pH3.4pH3.4pH7.5pPb7.5pPbpPbpPb...pHXO).3(eptspep%)02.0%(02.0100)1010(1010100Kc1010%EPM2.0)4(2/13.90.22.02.0MYMspPMPMt或式求:单位的出入,则误差公若有下一页上一页返回150333MLMLMLMLK[H]HLKa2某金属离子M与络合剂(HL)形成ML、、络合物。是推导出形成络合物形态时的条件形成常数与及络合剂的离解常数的关系式。aLL(H)aa1K[H]c[L][HL][H]1[L][L]KK解:()由络合剂的酸效应系数导出:33333ML333LL(H)aMLaMLaa2[ML][ML]1K[M]C[M][L]KK()K[H]lgK3pK3lg(K[H])3ML()由络合平衡关系导出:两边取对数,得:lgK下一页上一页返回151愈大。愈小,最大最好无此反应时当KKlgKlgKlgMYYMYMY值所对应的时当pH)N(Y)H(Y最高浓度:粗略认为求出最低浓度:nsp]M[K]OH[例21:看图证明滴定M的酸度范围lgαYpHCDEBAlgαY(H)lgαY(N)图pHlgY最大。最小。此时故段:段:故段:KlgDEBDABY)N(YY)H(Y)N(Y)N(Y)H(YY)H(YY)N(Y)H(Y为最高酸度值。点对应的点代替为界限。电不易测。的酸度范围。段为滴会水解点后过pHECDMDE.ME但可作为近似计算单位比最大值还小故此时还不能忽略。因为达到最大。其实故为最高浓度。点时由于3.0Klg2KC)Y(YY)H(Y).N(Y)H(Y下一页上一页返回Ok!Let’sHaveaBreak.Ok!Let’sHaveaBreak.SeeYouNextClassSeeYouNextClassGoodluck!!!Goodluck!!!



















