







《化学电源和物理电源PPT课件下载(共20页)》是由用户上传到老师板报网,本为文库资料,大小为1.29 MB,总共有20页,格式为ppt。授权方式为VIP用户下载,成为老师板报网VIP用户马上下载此课件。文件完整,下载后可编辑修改。
- 文库资料
- 20页
- 1.29 MB
- VIP模板
- ppt
- 数字产品不支持退货
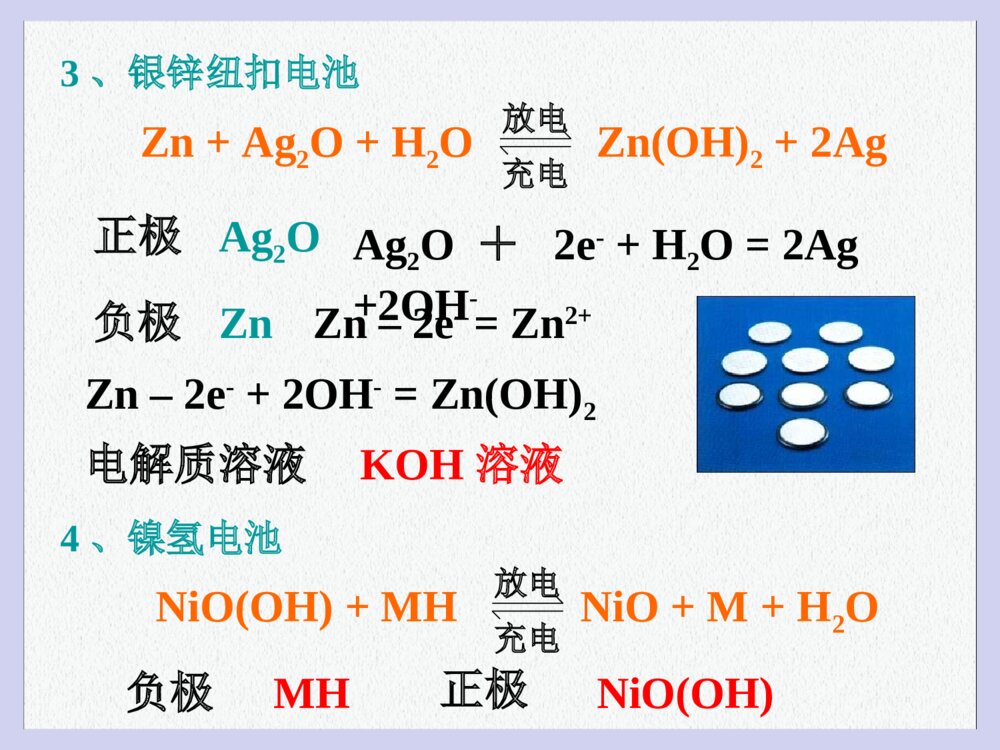
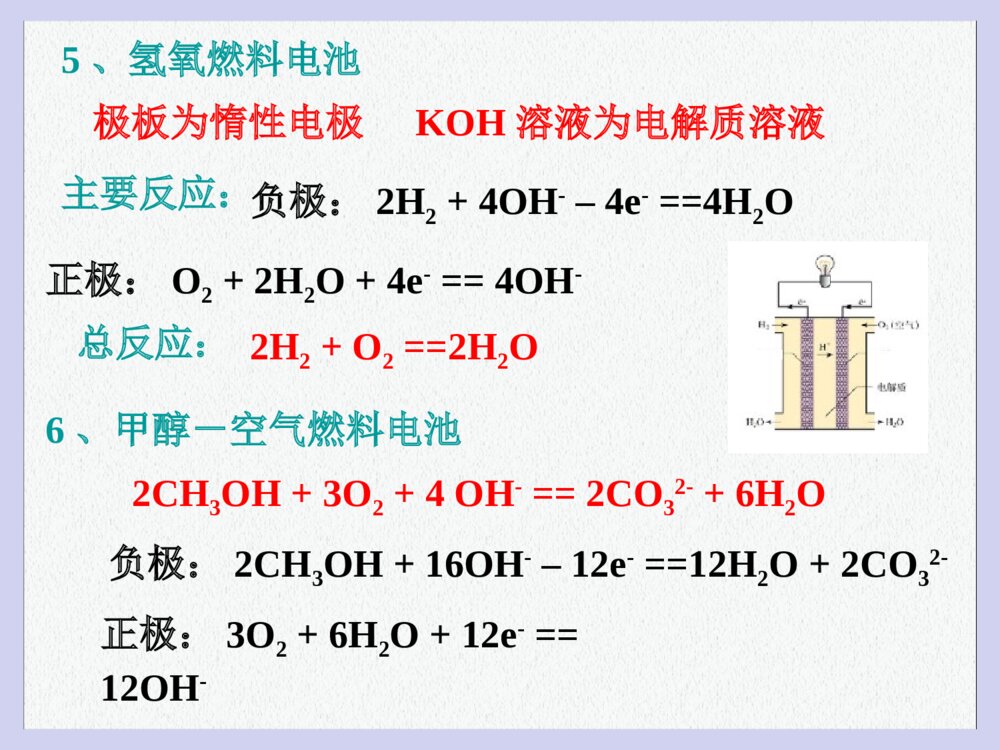
化学电源化学电源1锂电池常见化学电源常见化学电源一、化学电源的种类1.一次电池(如干电池):用过后不能复原2.二次电池(如蓄电池):充电后能继续使用3.燃料电池:将燃料和氧化剂中的化学能直接、连续地转化为电能的发电装置。1、干电池普通锌—锰干电池正极石墨棒负极锌筒电解质溶液调成糊状的氯化铵碱性锌—锰干电池电解液改成碱液负极改作锌粉主要反应:负极:Zn–2e-==Zn2+正极:2MnO2+2NH4++2e-==2MnO(OH)+2NH3Zn+2MnO2+2NH4+==Zn2++2MnO(OH)+2NH32、铅蓄电池正极PbO2负极Pb电解质溶液稀硫酸又叫铅酸蓄电池主要反应:负极:Pb+SO42-–2e-==PbSO4正极:PbO2+SO42-+4H++2e-==PbSO4+2H2O总反应:Pb+PbO2+2H2SO4==2PbSO4+2H2O镍—镉蓄电池可广泛用于收录机、电话机银—锌蓄电池是一种高能电池,体积小,质量轻锂电池也是一种高能电池,体积小,质量轻3、银锌纽扣电池正极负极电解质溶液Zn+Ag2O+H2OZn(OH)2+2Ag放电充电ZnZn–2e-=Zn2+KOH溶液Zn–2e-+2OH-=Zn(OH)2Ag2OAg2O+2e-+H2O=2Ag+2OH-4、镍氢电池NiO(OH)+MHNiO+M+H2O放电充电正极负极MHNiO(OH)5、氢氧燃料电池极板为惰性电极KOH溶液为电解质溶液主要反应:负极:2H2+4OH-–4e-==4H2O正极:O2+2H2O+4e-==4OH-总反应:2H2+O2==2H2O6、甲醇-空气燃料电池2CH3OH+3O2+4OH-==2CO32-+6H2O负极:2CH3OH+16OH-–12e-==12H2O+2CO32-正极:3O2+6H2O+12e-==12OH-家庭小实验要点一、电极反应式、原电池反应式的书写1.电极反应式的书写(1)负极反应式的书写①活泼金属作负极时,本身被氧化:若生成的阳离子不与电解质溶液反应,可直接写成产物为金属阳离子,如:Zn-2e-===Zn2+,Cu-2e-==Cu2+。若生成的金属阳离子与电解质溶液反应,应写成“金属失电子的反应式”与“阳离子与电解质溶液反应的反应式”相叠加的形式。如:Mg—Al(KOH)原电池,负极反应式为:Al-3e-+4OH-===AlO-2+2H2O;铅蓄电池负极反应式为:Pb-2e-+SO2-4===PbSO4。②负极材料本身不反应时,常见书写方法为:H2—O2(H2SO4)燃料电池,负极反应式为:H2-2e-===2H+;H2—O2(KOH)燃料电池,负极反应式为:H2-2e-+2OH-===2H2O。(2)正极反应式的书写首先根据化合价变化或氧化性强弱判断哪种微粒得电子。其次确定该微粒得电子后变成哪种形式。如:H2-—O2(H2SO4)原电池,正极反应式为:O2+4e-+4H+===2H2O;H2—O2(KOH)原电池,正极反应式为:O2+4e-+2H2O==4OH-。2.原电池反应式的书写两电极反应式,得失电子数相等时,将两电极反应式相加即得原电池反应式。特别提醒:在正极上,若是电解质溶液中的某种离子被还原,无论该离子是强电解质提供的,还是弱电解质提供的,一律写离子符号;而在原电池反应中,要遵循离子方程式的书写规则,只有易溶的强电解质用离子符号表示。要点2、燃料电池燃料电池中通燃料的一极作负极,通O2的一极作正极,常见的有CH4、CH3OH、C2H6、H2等燃料电池。例:如图所示,可形成氢氧燃料电池。通常氢氧燃料电池有酸式(当电解质溶液为H2SO4溶液时)和碱式[当电解质溶液为NaOH(aq)或KOH(aq)时]两种。试回答下列问题:氢氧燃料电池示意图(1)酸式电池的电极反应:负极________________,正极______________;电池总反应:______________;电解质溶液pH的变化_______(填“变大”、“变小”或“不变”)。(2)碱式电池的电极反应:负极________________,正极______________;电池总反应:______________;电解质溶液pH的变化_______(填“变大”、“变小”或“不变”)。2H2-4e-=4H+ O2+4e-+4H+=2H2O 2H2+O2=2H2O 变大O2+4e-+2H2O=4OH- 2H2-4e-+4OH-=4H2O 2H2+O2=2H2O 变小【解析】燃料电池所用的介质不同,相应的电极反应就不同;但无论如何书写,两电极反应相叠加始终等于燃料的燃烧反应。这也是验证电极反应是否正确的一种方法。(1)正极上,O2得电子变为O2-,溶液中O2-不能单独存在,酸性条件下与H+结合生成H2O。负极上,H2失电子变为H+,H+进入电解质溶液。电池总反应为H2在O2中燃烧的反应,由于有水生成,溶液将逐渐变稀,故pH增大。(2)正极上,O2得电子变为O2-,溶液中O2-不能单独存在,碱性条件下与H2O分子结合生成OH-;负极上,H2失去电子变为H+,碱性条件下H+不能大量存在,与OH-结合生成水。电池总反应也是H2在O2中的燃烧反应。同样,由于有水生成,c(OH-)变小,pH变小【答案】(1)2H2-4e-===4H+O2+4e-+4H+===2H2O2H2+O2===2H2O变大(2)2H2-4e-+4OH-===4H2OO2+4e-+2H2O===4OH-2H2+O2===2H2O变小变式训练、航天飞机常采用新型燃料电池作为电能来源,燃料电池一般指采用H2、CH4、CO、C2H5OH等可燃物质与O2一起构成的电池装置。它可直接将化学能转化为电能,甲烷电池以KOH溶液为电解质,其总反应的化学方程式为CH4+2O2+2OH-===CO2-3+3H2O。(1)负极上的电极反应为____________________。(2)消耗标准状况下的5.6LO2时,有________mol电子发生转移。(3)开始放电时,正极附近溶液的pH________(填“增大”、“减小”或“不变”)。答案:(1)CH4+10OH--8e-===CO2-3+7H2O(2)1(3)增大1、微型纽扣电池在现代生活中有广泛应用。有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH,电极反应则为:Zn+2OH--2e-=ZnO+H2O;Ag2O+H2O+2e-=2Ag+2OH-根据上述反应式,判断下列叙述中正确的是( ) A、在使用过程中,电池负极区溶液的pH减小 B、使用过程中,电子由Ag2O极经外电路流向Zn极 C、Zn是负极,Ag2O是正极 D、Zn电极发生还原反应,Ag2O电极发生氧化反应巩固练习AC2、电瓶车所用电池一般为铅蓄电池,这是一种典型的可充电电池,电池总反应式为: Pb+PbO2+4H++2SO42-2PbSO4+2H2O 则下列说法正确的是:A.放电时:电子流动方向由B到AB.放电时:正极反应是Pb-2e-+SO42-=PbSO4C.充电时:铅蓄电池的负极应与充电器电源的正极相连D.充电时:阳极反应是PbSO4-2e-+2H2O=PbO2+SO42-+4H+3、据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,其电池反应为:2CH3OH+3O2+4OH—2CO32—+6H2O则下列说法错误的是()A.放电时CH3OH参与反应的电极为正极B.充电时电解质溶液的pH逐渐增大C.放电时负极的电极反应为:CH3OH-6e-+8OH-=CO32—+6H2OD.充电时每生成1molCH3OH转移6mol电子



















