






《高一化学必修1《物质的量的单位-摩尔》PPT课件下载》是由用户上传到老师板报网,本为文库资料,大小为743 KB,总共有23页,格式为ppt。授权方式为VIP用户下载,成为老师板报网VIP用户马上下载此课件。文件完整,下载后可编辑修改。
- 文库资料
- 23页
- 743 KB
- VIP模板
- ppt
- 数字产品不支持退货
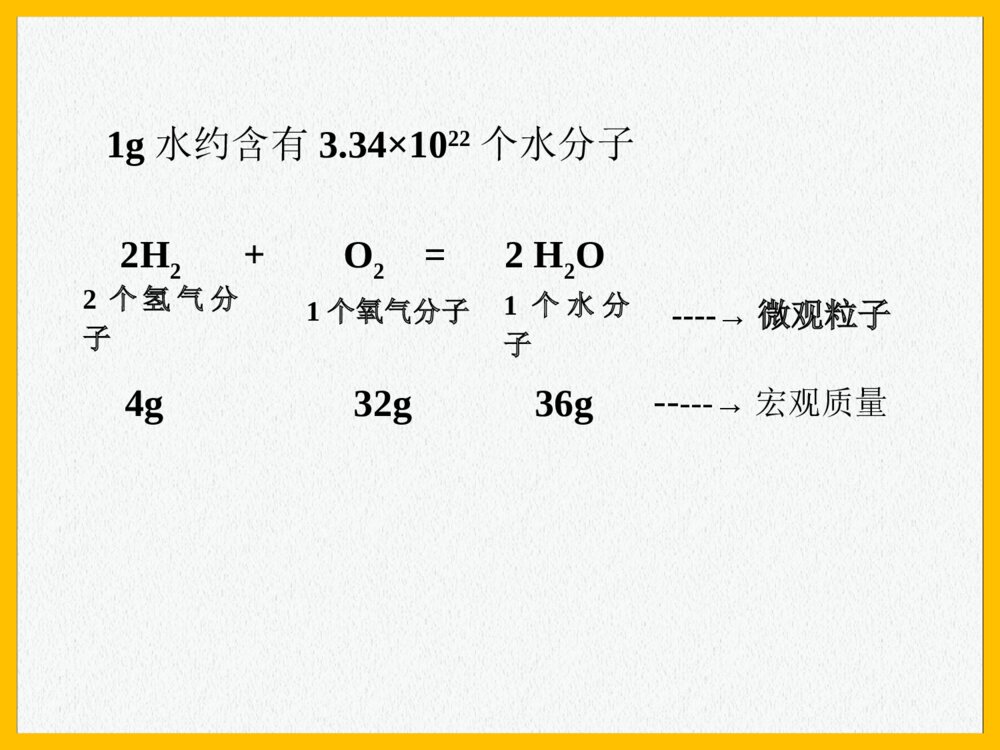
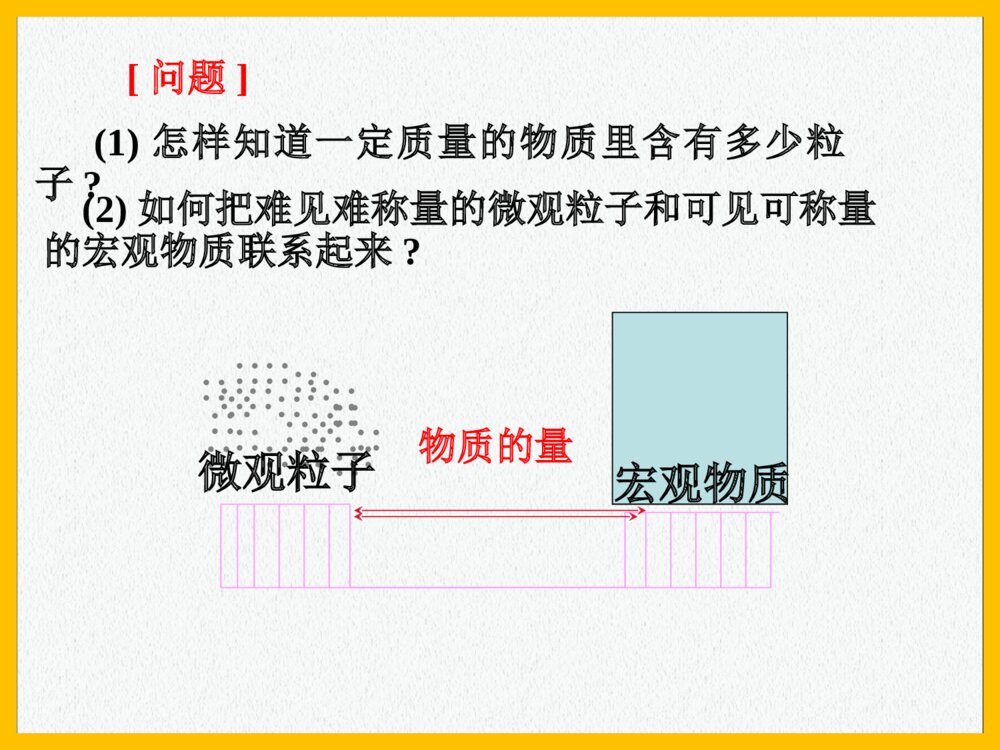
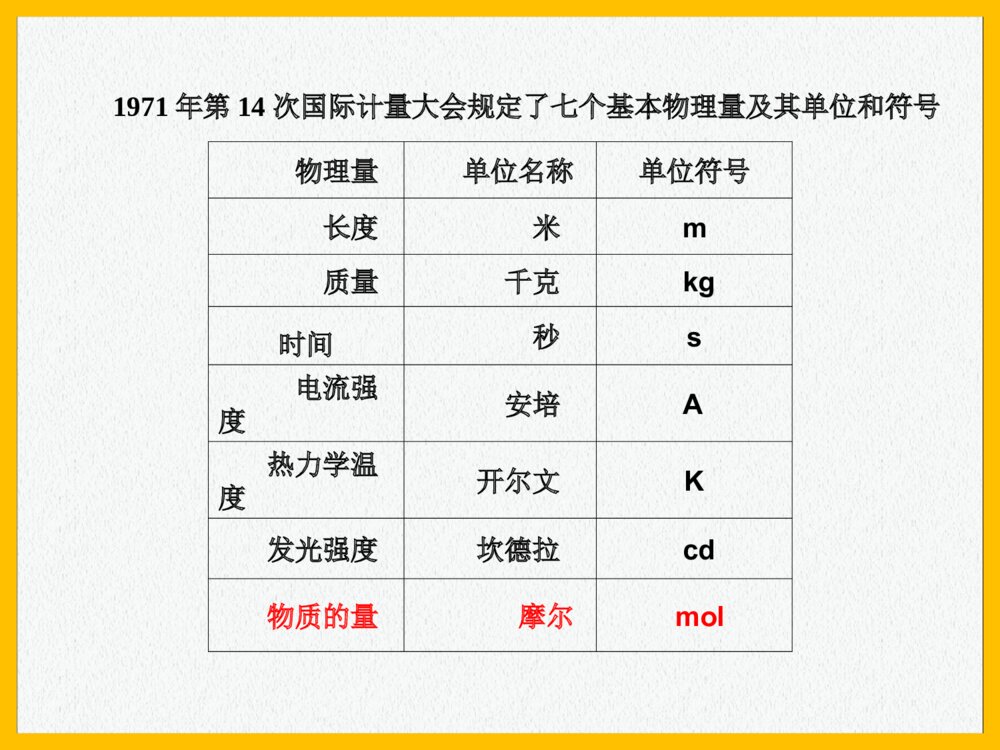
新课标人教版课件系列《高中化学》必修11.2.1《物质的量的单位-摩尔》化学计量在实验中的应用(1)教学目标•知识与能力•掌握物质的量的定义、符号及其单位摩尔的定义、符号等,了解它们的使用范围,使用时的注意事项,使学生对物质的量形成一定的印象。•掌握摩尔质量的概念,理解物质的量、摩尔质量、物质的质量之间的关系。•【教学重点】•物质的量及其单位、摩尔质量的概念和相关计算•【教学难点】物质的量及其单位、摩尔质量与相对原子质量、相对分子质量之间的关系1g水约含有3.34×1022个水分子2H2+O2=2H2O2个氢气分子1个氧气分子1个水分子----→微观粒子4g32g36g-----→宏观质量[问题](1)怎样知道一定质量的物质里含有多少粒子?(2)如何把难见难称量的微观粒子和可见可称量的宏观物质联系起来?∷∷∷∷∷∷∷∷∷∷∷∷∷∷∷∷∷∷∷∷∷∷∷∷宏观物质微观粒子物质的量1971年第14次国际计量大会规定了七个基本物理量及其单位和符号物理量单位名称单位符号长度米m质量千克kg时间秒s电流强度安培A热力学温度开尔文K发光强度坎德拉cd物质的量摩尔mol一、物质的量(n)2、表示含有一定数目粒子的集体1、是一个物理量,专用名词,不能增减3、单位:摩尔(符号:mol)二、摩尔(mol)——物质的量的单位1、每摩尔物质含有阿伏加德罗常数个微粒2、微粒──可以是分子、原子、离子,电子、中子、质子等基本的粒子,也可以是特定微粒的组合,但是一定要说明确。●●3、使用摩尔作单位时,应用化学式(符号)指明粒子种类,而不能使用中文名称。三、阿伏加德罗常数(NA)1、定义:用12g12C所含的碳原子数叫阿伏加德罗常数。2、阿伏加德罗常数的近似值是:6.02×1023mol-112gC:0.012kg1.993×10-26kg/个=6.02×1023个6.02×1023这个数非常庞大。如果把6.02×1023个直径为2.5cm的硬币排成一行,可以来回于地球与太阳之间240.8亿次。6.02×10231mol粒子的粒子数约为阿伏加德罗常数约为0.012Kg12C中所含原子数约为练习判断11mol氧20.25molCO23摩尔为7个基本物理量之一41mol是6.02×1023个粒子的集体50.5molH2有3.01×1023个氢原子63molNH3有3molN原子,9molH原子13molH2SO4中约有-----个H2SO4,可以电离出-----molH+24molO2含有------molO原子,------mol质子310molNa+中约含有-----Na+填空O2的物质的量阿伏加德罗常数粒子数1mol×6.02×1023mol-1=6.02×10232mol×6.02×1023mol-1=1.204×1024n×NA=N四、物质的量(n)、阿伏加德罗常数(NA)、粒子数(N)之间的关系物质的量=微粒个数阿伏加德罗常数N个NA个/mol=n(mol)练习已知一个氢原子的质量为1.674×10-24g,求1molH的质量。氢原子的质量m=1.674×10-24g×6.02×1023=1.0g数值上与氢原子的原子量相等1mol氢原子的质量,以克为单位,数值上与氢原子的原子量相等微粒CHOH2O相对原子(分子)质量12116181mol的质量12克1克16克18克1mol1mol物质的质量质量(gg)在数值数值上等于其相对原子(分子)质量相对原子(分子)质量结论:1mol任何微粒的质量都是以克为单位数值上等于该物质化学式的式量●●1molO2的质量为32克1molNa+的质量为23克1molNaCl的质量为58.5克1molAl的质量为27克五、物质的摩尔质量(M)1、定义:单位物质的量的物质的质量叫物质的摩尔质量。2、单位:g/mol或g.mol-1,kg/mol1molM=mn物质的摩尔质量=物质的质量物质的量数值:等于相对原子(分子)质量总结:物质的质量m、物质的量n、粒子数N之间的关系如下:mN(÷M)(×M)(×NA)(÷NA)n微观宏观练习:3.01×1022个OH-的物质的量为0.05mol,质量为,含有质子的物质的量为,含有电子的物质的量为,这些OH-与NH3的质量相同,这些OH-和Na+含有的离子数相同。0.85g0.45mol0.5mol0.05mol1.15g练习:将4gNaOH溶于多少克水中,才能使每100个H2O分子溶有一个Na+?解:n(Na+)=n(NaOH)=m(NaOH)M(NaOH)=4g÷40g/mol=0.1moln(H2O)=100×n(Na+)=100×0.1mol=10molm(H2O)=n(H2O)×M(H2O)=10mol×18g/mol=180g



















