



《初中化学实验改进与创新PPT课件下载》是由用户上传到老师板报网,本为文库资料,大小为1.91 MB,总共有48页,格式为ppt。授权方式为VIP用户下载,成为老师板报网VIP用户马上下载此课件。文件完整,下载后可编辑修改。
- 文库资料
- 48页
- 1.91 MB
- VIP模板
- ppt
- 数字产品不支持退货
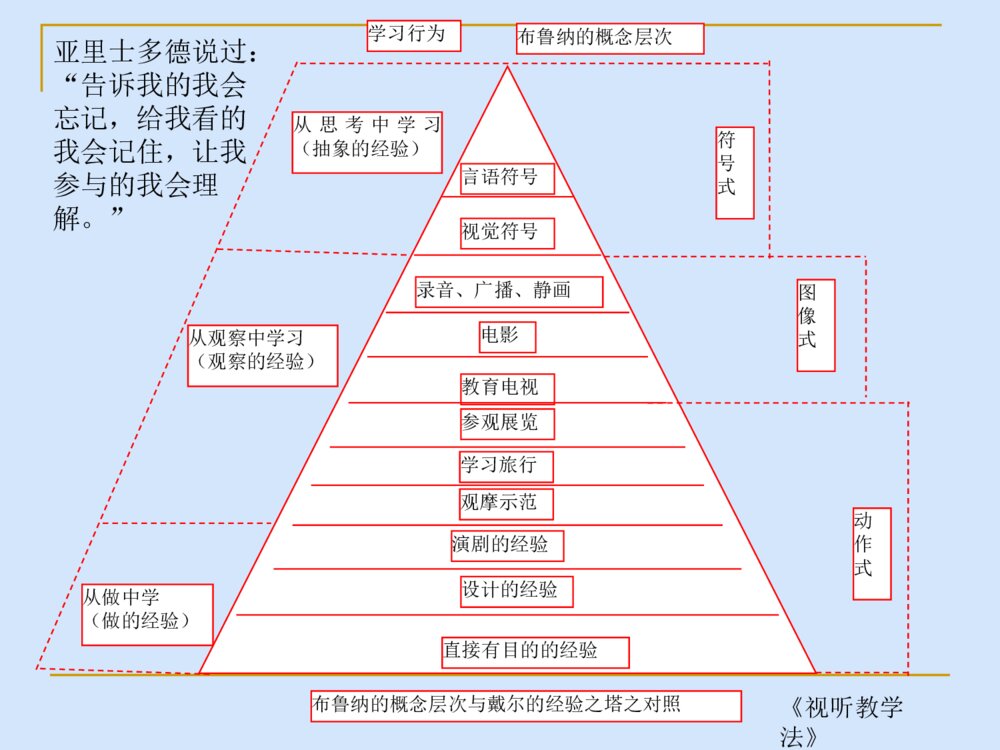
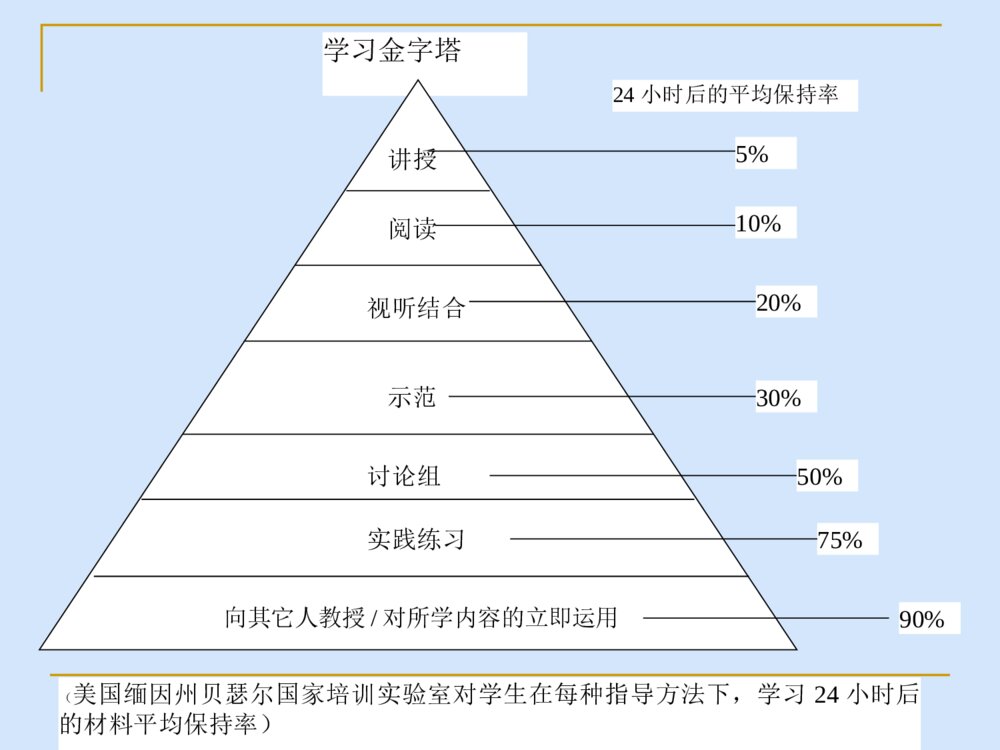
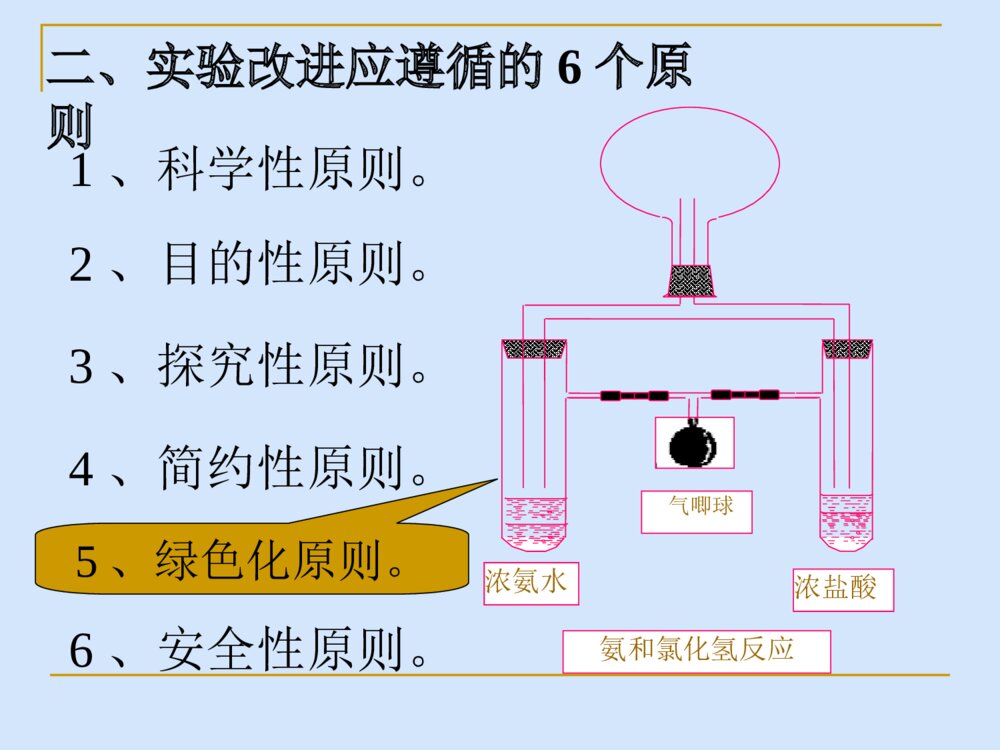
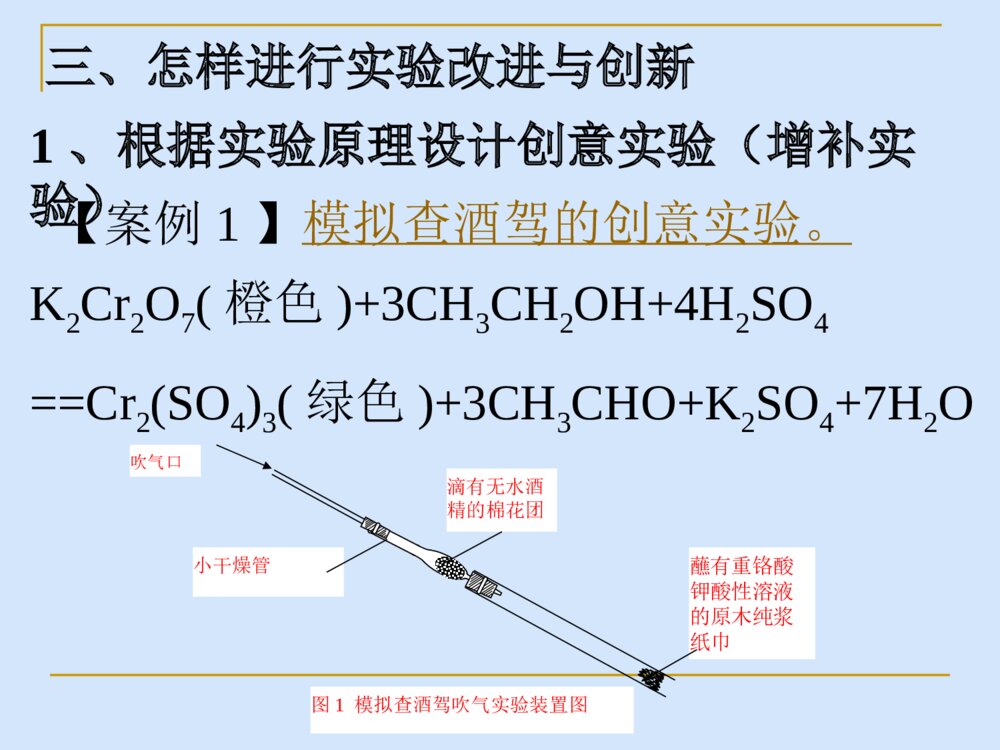
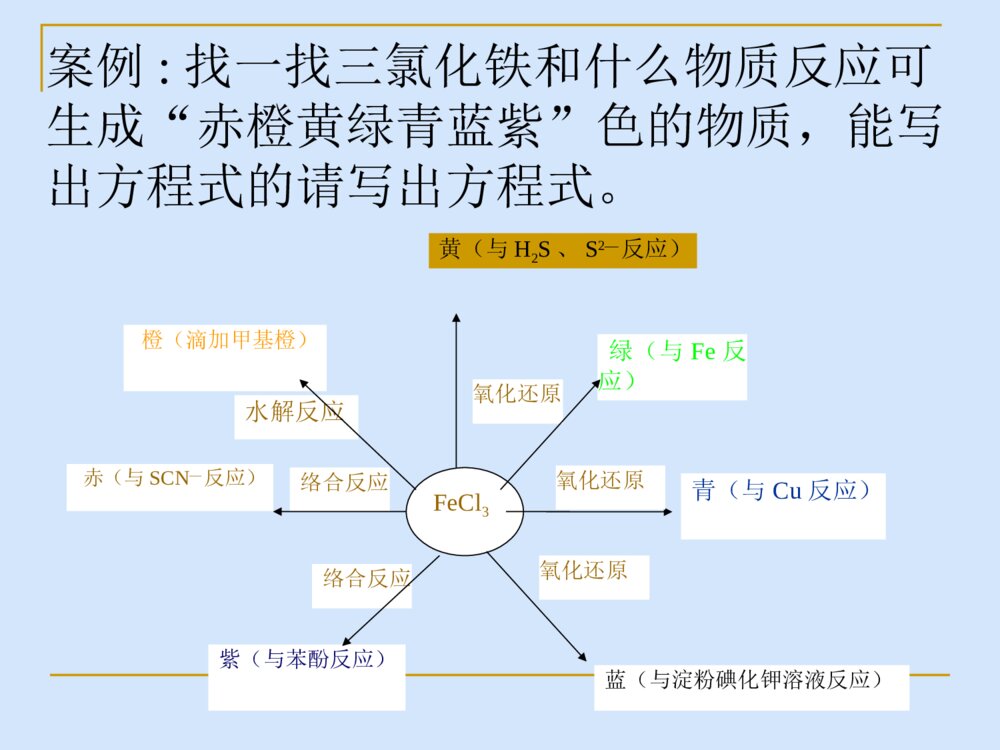
有理想信念——行动方向有道德情操——价值判断有扎实知识——专业素养有仁爱之心——教育灵魂什么样的老师是好老师?五有:有理想信念;有良好的师德和仁爱之心;有扎实的专业知识;有良好的教学艺术;有一定的科研能力。一、为什么要进行实验改进与创新二、实验改进与创新应遵循的6个原则三、怎样进行实验改进与创新四、实验改进的典型案例五、实验研究一、为什么要进行实验改进与创新1、现行化学教材存在的问题操作过程繁琐;现象不鲜明;成功率不高;产生有毒气体;探究性不强。2、从教材的发展和人的发展的角度来看实验创新将有利于人的发展。3、“做中学”是学生发展的一个重要途径。美国华盛顿大学有这样一个条幅:“我听见了,就忘记了;我看见了,就领会了;我做过了,就理解了。” 我们要特别重视对学生四种精神的培养,即科学精神、冒险精神、质疑精神和创新精神的培养,缺少上述四种精神的民族不可能成为伟大的民族。 改进与创新的关系,改进中有创新,但有差别。改进相当于修修补补,使之完美;创新相当于另起炉灶(颠覆性的或新概念),促进发展。言语符号视觉符号录音、广播、静画电影教育电视参观展览学习旅行观摩示范演剧的经验设计的经验直接有目的的经验学习行为布鲁纳的概念层次符号式图像式动作式从思考中学习(抽象的经验)从观察中学习(观察的经验)从做中学(做的经验)布鲁纳的概念层次与戴尔的经验之塔之对照亚里士多德说过:“告诉我的我会忘记,给我看的我会记住,让我参与的我会理解。”《视听教学法》(美国缅因州贝瑟尔国家培训实验室对学生在每种指导方法下,学习24小时后的材料平均保持率)学习金字塔阅读讲授视听结合示范讨论组实践练习向其它人教授/对所学内容的立即运用5%10%20%30%50%75%90%24小时后的平均保持率二、实验改进应遵循的6个原则2、目的性原则。1、科学性原则。3、探究性原则。4、简约性原则。6、安全性原则。5、绿色化原则。浓氨水浓盐酸氨和氯化氢反应气唧球三、怎样进行实验改进与创新1、根据实验原理设计创意实验(增补实验)【案例1】模拟查酒驾的创意实验。K2Cr2O7(橙色)+3CH3CH2OH+4H2SO4==Cr2(SO4)3(绿色)+3CH3CHO+K2SO4+7H2O滴有无水酒精的棉花团吹气口蘸有重铬酸钾酸性溶液的原木纯浆纸巾小干燥管图1模拟查酒驾吹气实验装置图案例:找一找三氯化铁和什么物质反应可生成“赤橙黄绿青蓝紫”色的物质,能写出方程式的请写出方程式。青(与Cu反应)绿(与Fe反应)络合反应氧化还原水解反应络合反应FeCl3橙(滴加甲基橙)黄(与H2S、S2—反应)赤(与SCN—反应)蓝(与淀粉碘化钾溶液反应)紫(与苯酚反应)氧化还原氧化还原赤橙黄绿青蓝紫铁树开花【案例2】二氧化碳与过氧化钠反应的增补实验:方法1:加热法。AB石灰水浓硫酸Na2O2NaHCO3石棉绒或玻璃丝方法2:吹气法。裹有过氧化钠粉末的棉花团吹气口石棉网2Na2O2+2CO2==2Na2CO3+O2↑H△<0方法3:悬置法1、装置图铁丝包裹过氧化钠的棉花团沸水2、操作及现象①将少量过氧化钠固体包裹在棉花中,用一根铁丝将其连接在铁架台上。②在棉花的正下方放置一盛有沸水的烧杯,此时,水蒸气上升至棉花处,过一会儿,棉花燃烧,未反应完的过氧化钠掉入烧杯中,向烧杯中滴入1~2滴酚酞溶液,溶液变红。③利用同样装置。在烧杯中加入稀盐酸,再放几块大理石,待产生的二氧化碳上升至棉花处,同样可以看到棉花燃烧起来。3、优点:增强趣味性;同一装置可做两个实验。2、根据反应原理改进传统实验【案例3】实验室制乙烯的改进存在问题:反应物变黑;产生的气体有剌激性气味等异常现象。反应原理:CH3CH2OH+H2SO4CH3CH2OSO2OH+H2O硫酸氢乙酯CH3CH2OSO2OH CH2==CH2↑+H2SO4CH3CH2OH+CH3CH2OH CH3CH2OCH2CH3+H2O>150℃130~140℃改进:在圆底烧瓶中加入5mL无水乙醇和10mL浓硫酸,再加入几片洗净的碎瓷片。在烧瓶口配上带温度计及长玻璃管(起回流作用)的胶塞。加热,当温度升到80℃时迅速加入氧化钙3g,反应物的温度迅速上升,达到170℃左右时,使气体通过装有氢氧化钠溶液的洗气瓶,再收集乙烯。3、根据实验条件改进传统实验影响化学反应实验的条件有浓度、用量、催化剂、反应物的接触面积、温度等。【案例4】一氧化碳还原氧化铜的实验改进(见图4——反应物的接触面积)石灰水铜箔CO铜丝改进后的装置COCuO石灰水改进前的装置图4一氧化碳还原氧化铜的实验改进4、根据实验装置进行实验改进气体发生装置,气体净化、吸收和尾气处理装置,环保化密闭的实验装置(化学实验绿色化),综合系列化的实验装置等。【案例5】锌和碘实验装置的改进(见图3《中化参》1988年第6期)Zn(s)+I2(s)=ZnI2(s)△H<0水水锌粉和碘粉的混合物改进前的装置锌粉和碘粉的混合物5%的淀粉溶液水改进后的装置图3锌和碘实验装置的改进煤油水钠铁钉长颈漏斗【案例6】钠和水反应的实验改进1取一个150mL或125mL烧杯,向其中加满水,然后倒出40-50mL水,把一块黄豆大的钠(经测量约为1g,标准状况产生氢气约为50mL)投入剩余烧杯水中,迅速用玻璃片(要比烧杯口大)盖在烧杯口上,观察现象。待钠完全反应后,将玻璃片向一侧平移(用左手捏牢),使烧杯露出2~3cm的空隙,然后迅速将已燃烧的火柴棒插入烧杯中,观察现象。最后向烧杯中滴入几滴酚酞,观察现象。钠和水反应的实验改进2:煤油水K【案例7】钾和水反应的增补实验:煤油:0.80g/cm3K:0.86g/cm3水:1.0g/cm3【案例9】快捷高效的“喷泉实验”新做法改进前的装置NH3改进后的装置图2NH3矿泉水瓶5、根据操作过程进行优化(1)力求简化。图10加热铜板使乙醇催化氧化【案例10】加热铜板使乙醇催化氧化的实验(见图10)。注:氧化铜粉与乙醇在加热的条件下也不反应——未达到催化剂的活性温度;氧化铜不是新生态。(2)增强探究性。【案例11】铁在氧五燃烧为什么会放出耀眼的白光而不产生火焰固体燃烧蒸发燃烧如硫、磷、石蜡钠、钾等挥发燃烧如萘、樟脑分解燃烧如纸张表面燃烧如固态的碳、铝、镍、铁等★以上4种形式的燃烧中,蒸发燃烧、挥发燃烧和分解燃烧,最后都是可燃性气体或蒸汽的燃烧。这些燃烧,都要依靠气体扩散来进行,因此有火焰产生。而表面燃烧是在固—气界面上,固体表面直接燃烧,因此,属于无焰燃烧。【案例11】2011年安徽中考题(3)加大可视性(或直观性)红墨水操作:通过缓缓拉动注射器的活塞,吸入VmL空气,就有VmL红墨水进入集气瓶。四、实验改进的典型案例“空五测定氧气的体积分数”【案例12】二氧化碳性质实验的组合设计1234455b1a2b266oo1.能上下移动的硬质铜丝2.装在尼龙袋里的石灰石3.稀盐酸4.干燥的蓝色石蕊试纸5.湿润的蓝色石蕊试纸6.澄清的石灰水图7a1【案例13】燃烧的条件探究热水白烟白磷红磷改进1:将白磷和红磷密封在大试管中,并放于热水里。——避免污染空。改进2:将一只大试管罩住热水中铜圈内的白磷,用大试管中的空气排开白磷周围的水,使热水下的白磷与空气接触。——省略氧气装置且避免污染空。白磷热水白烟图12燃烧的条件探究【案例14】“氧化铁还原反应”实验的改进CO石灰水Fe2O3尾气处理改进前的实验装置Fe2O3石灰水改进后的实验装置CH4【案例15】“碳酸钙与盐酸反应前后质量的测定”实验改进锥形瓶(100mL)足量的石灰石20mL一次性注射器适量的稀盐酸【案例16】“测定空五氧气体积分数”实验新装置注射器(20mL)硫酸铜溶液锥形瓶(约56mL)白磷五、实验研究【案例17】氢氧化亚铁由白色转为灰绿色,再由灰绿色转化为红褐色沉淀,其中灰绿色物质的成分到底是什么?实验探究(增补实验1):将白色颜料和红褐色颜料按1︰1、3︰1、1︰3比例进行混合,发现混合后的颜色不是灰绿色,而是灰红色。阅读探究:某同学查阅资料后,得到Fe(OH)2有如下信息:资料名称物理性质描述化学性质描述《大学普通化学(下册)》傅鹰著P637白色沉淀此沉淀易被氧化成微绿色Fe3(OH)8《普通化学教程》(下册)P788白色能强烈吸收O2,迅速变成棕色Fe(OH)3。这时作为氧化的中间产物为土绿色,其中含有Fe2+、Fe3+。灰绿色的固体是一种八面体结构的水合铁酸亚铁盐[Fe(FeO2)2·(H2O)4〕,或Fe(OH)2·2Fe(OH)3,亚铁离子处于八面体的中心,因此相对氢氧化亚铁来讲较稳定,不容易氧化为氢氧化铁。H2OH2OH2OH2OFeO22—FeO22—【案例18】黑色铜之“谜”将铁片插入稀硫酸中表面变黑(或将铁片插入硫酸铜溶液中表面变黑)的原因是什么?铁片表面变黑的原因:铁片与氢离子发生反应时,金属晶体的表面有规则的结构被破坏,照射在金属表面上的可见光没有反射而全部被吸收,故而显黑色。绿色黄色蓝色绿黄黄绿色蓝绿绿蓝红色橙黄橙红紫色紫色色环拮(jie)抗原理:红与绿、黄与蓝、黑与白共成三对,在光波作用下起作用而颜色互补。【案例19】CO(H2)还原Fe2O3生成的黒色粉末是什么?加热反应通入CO时间产物冷却方式产物颜色产物检验冷却前冷却后冷却后加稀盐酸冷却后加硫酸铜溶液0.5min露置在空五冷却至室温黑色红色红色固体逐渐溶解,溶液由无色变为黄色,无气泡产生。红色固体无明显变化。0.5min隔绝空气冷却至室温黑色黑色黑色固体表面有少量气泡产生少量黑色固体逐渐变为红色物质2min露置在空五冷却至室温黑色红色红色固体逐渐溶解,溶液由无色变为黄色,无气泡产生。红色固体无明显变化。2min隔绝空气冷却1min后,再露置在空五冷却至室温黑色黑色黑色固体表面有少量气泡产生少量黑色固体逐渐变为红色物质2min隔绝空气冷却至室温黑色黑色黑色固体表面有大量气泡产生大量黑色固体逐渐变为红色物质(2)原因分析氧化性:Fe2O3>Fe3O4>Fe反应:易→难。当温度高于300℃,氧化铁容易还原为Fe3O4;当温度高于600℃,Fe3O4才容易还原为FeO;只有当温度高700℃时,FeO才可以大量还原成单质铁。演示实验酒精灯温度为400℃~500℃,黑色粉末的主要成分是Fe3O4,另含有少量FeO和单质铁;实验表明,该黑色粉末具有铁磁性。【案例20】氢氧化钾乙醇溶液放置为什么会变棕黄色?(胡列扬,杭州外国语学校《中化参》2012第5期P49)取20mL乙醇(分析纯)+过量的KOH固体(分析纯)第二天颜色稍有变化,一个月后已经变为深棕色,KOH固体表面还可看到少量炭黑。取过量的KOH固体放入100mL烧杯中,注入无水酒精至饱和(溶液下面余有固体)。然后分装于4支试管。两支为饱和溶液,无固体,另两支试管中均留有KOH固体。向其中两支试管中通入纯氧气(饱和溶液和留有KOH固体溶液各一支),贴上标签,留之观察。18h后,留有KOH固体试管都偏黄,越接近固体颜色越深,通入氧气的试管比未通氧气的试管颜色明显深一些,无固体试管中溶液未变色。结论:①氧气必参加反应。②固体KOH对氧化还原反应有促进作用。③氧化产物复杂多样。反应1:2CH3CH2OH+O2→2CH3CHO+2H2O反应2:2CH3CHO+4KOH+3O2→2C+6H2O+2K2CO3【案例21】对消去反应实验的研究与改进苏教版高二教材(有机化学基础),专门设计了溴乙烷与饱和氢氧化钾乙醇溶液发生消去反应的实验,该实验从2007年到现在教材已作了3次修改,修改频率之高实属罕见。但从另一个侧面也反映出,该实验的确不好做。对此,我们对该实验进行了研究和改进。经我们反复实验研究发现,该实验的成功关键有4点:(1)卤代烃选择;(2)反应温度控制;(3)反应混合液的接触面积;(4)碱的量要充足。(2)反应温度控制反应温度控制,主要从3个方面:①尽可能不让卤代烃及乙醇汽化。②采用水浴加热,防止温度过高,避免卤代烃汽化。③温度控制在71℃-75℃。(3)反应混合液的接触面积要尽可能增大反应混合液的接触面积,一是用锥形瓶代替大试管,二是反应过程中要不断振荡锥形瓶。(4)碱的量要充足加人氢氧化钠或氢氧化钾的物质的量要大于卤代烃的物质的量(由密度、体积、式量计算出),如10mL1,2-二氯乙烷(密度为1.257g/cm3),其物质的量约为0.127mol,加入氢氧化钠或氢氧化钾的物质的量应大于0.127mol,即加入氢氧化钠的质量应大于5.1g,加入氢氧化钾的质量应大于7.1g。不需要氢氧化钠或氢氧化钾的乙醇饱和溶液,因为常温下氢氧化钠(或氢氧化钾)在乙醇中的溶解度不大,但温度高于70℃时,溶解度大大增加。乙醇的量适当就可以了,如体积是卤代烃的1.5倍。 实验改进(1)实验装置说明:将连有导管的单孔橡皮塞塞紧锥形瓶,放到大烧杯中进行水浴加热,将无色透明的塑料饮料瓶中充满水,并放入水槽中,用排水法收集气体。向内挤压酸性高锰酸钾溶液说明:将收集好气体的塑料饮料瓶,用连有导管的单孔橡皮塞塞紧,导管的另一端通入酸性高锰酸钾溶液中。(2)实验步骤称取6g氢氧化钠固体,放入锥形瓶中,向其中加入15mL无水酒精,振荡约1分钟,向其中加入10mL1,2-二氯乙烷(密度为1.257g/cm3),迅速用带导管的单孔橡皮塞塞紧,将导管的另一端伸入倒置的充满水的无色透明的塑料饮料瓶口中。然后将锥形瓶放入73-75℃的水浴加热,不断振荡锥形瓶,大约5-6分钟后即可。此时停止收集,将导管移出水面,并将锥形瓶放入冷水中。将饮料瓶口在水下用瓶盖拧紧后,从水中取出,正方在桌面上,然后打开瓶盖,用带导管的单孔橡皮塞塞紧,将导管的另一端分别伸入盛有2mL稀的高锰酸钾溶液的试管中,缓缓挤压塑料饮料瓶,使气体缓缓冒出,观察高锰酸钾溶液是否褪色。上述实验完毕后,点燃酒精灯,将铜丝烧红,将导管口靠近并对准铜丝及火焰,挤压塑料饮料瓶,使气体喷出,观察火焰颜色。(3)实验现象振荡锥形瓶后,反应混合液很快变为牛奶状,气泡不断冒出,5-6分钟后收集到的气体约200-250mL。将产生的气体通入稀的高锰酸钾溶液中,看到溶液褪色。将气体喷向红热的铜丝及火焰,火焰呈绿色,证明该气体是氯乙烯。(4)改进说明①将酒精灯加热改为水浴加热。②将水浴温度控制在71-75℃。③用锥形瓶代替大试管。④用1,2-二氯乙烷代替溴乙烷⑤用氢氧化钠固体和乙醇代替氢氧化钾的乙醇饱和溶液⑥用无色透明的塑料饮料瓶代替试管,用排水法收集气体【案例22】非琼脂类盐桥的制作(刘英丽)H2SiO3溶胶方案1:用K2SiO3溶液和盐酸制硅酸凝胶方案2:用饱和的氯化钾溶液直接制备盐桥方案3:用氯化钾和糯米粉制盐桥☆苏霍姆林斯基说过:“才能增长才智,学生的能力和才干来自于他们的指尖,手指那些细小的溪流在不断地补充创新思维的源泉。”★苏霍姆林斯基还说过:“如果你想让教师的劳动能够给教师带来一些乐趣,使天天上课不至于变成一种单调乏味的义务,那你就应当引导每一位教师走上从事研究的这条幸福道路上来。”☆夸美纽斯语:★寻求并找出一种教学的方法,使教员因此可以少教,但是学生可以多学!★追求伟大的事情在过去是高贵的,在现在是高贵的,到将来永远是高贵的!刘猛张英华(北京房山区教科所副主任\\房山区优秀班主任)★在追求中奋进,在阅读中成长,在写作中提升,在实践中超越!



















