








《金属及其化合物 第1节 钠及钠的重要化合物PPT课件下载》是由用户上传到老师板报网,本为文库资料,大小为1.28 MB,总共有39页,格式为ppt。授权方式为VIP用户下载,成为老师板报网VIP用户马上下载此课件。文件完整,下载后可编辑修改。
- 文库资料
- 39页
- 1.28 MB
- VIP模板
- ppt
- 数字产品不支持退货
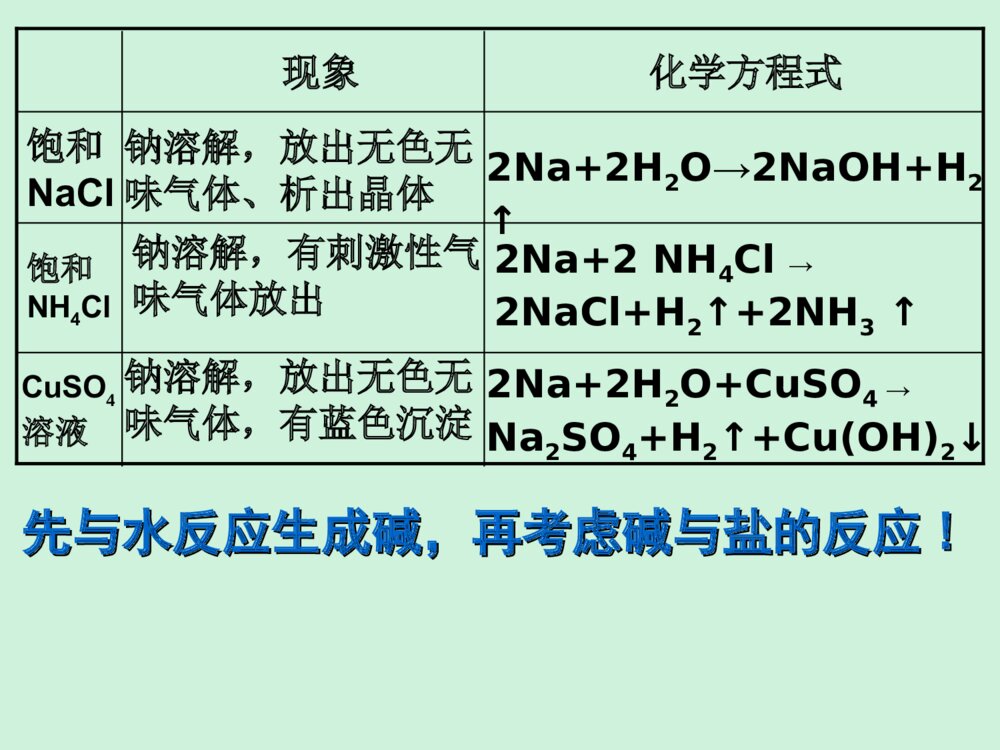
第一节 钠及钠的重要化合物金属及其化合物教学目标:1、了解钠和钠氧化物的重要物理性质2、关注钠和钠的氧化物在生产、生活中的应用实例3、了解钠与氧气、水、酸、碱、盐等物质的反应情况4、了解氧化钠与水、酸、碱等物质反应情况5、过氧化钠与H2O、CO2反应情况6、碳酸钠和碳酸氢钠、氢氧化钠等在生产和生活中的应用7、碳酸钠和碳酸氢钠、氢氧化钠等重要的物理性质8、比较碳酸钠和碳酸氢钠的溶解性、热稳定性9、碳酸钠和碳酸氢钠与酸的反应,10、掌握碳酸钠和碳酸氢钠的鉴别方法11、CO32-、HCO3-与其他离子的水解反应重要的金属知识回顾一、金属的通性1.物理通性有 、 、 。2.化学通性是 性。主要表现在金属能与 、 、 、 反应。*一般说来,金属原子的半径越 ,最外层电子数越 ,金属的还原性越,金属的熔沸点、硬度越 。延展性导电性导热性还原非金属水酸某些盐大少小强二、由金属活动顺序表分析金属知识的规律金属活动性顺序表KCaNaMgAlZnFeSnPbHCuHgAgPtAu金属性Mn+氧化性与O2反应与酸中H+与碱反应与水中H+与盐溶液碱热分解存在形式冶炼方法由强到弱由弱到强常温易常温、能加热、能不能剧烈加热、能常温能不能常温、能与氧化性酸与王水与水反应铝、锌与强碱溶液反应与水反应前面的金属置换后面的金属不分解受热分解常温分解化合态化合、游离游离电解法(K-Al)热还原法热分解法淘取极易失去最外层的一个电子+1128金属活动性顺序表NaMgAlZnFeSnPb(H)CuHgAgPtAuKCa三、碱金属——代表物:金属钠钠的化学性质:非常活泼,为强还原剂(一)钠的物理性质:1、钠与非金属单质反应4Na+O2→2Na2O2Na+O2→Na2O2(淡黄色固体)-1银白色金属、质软、熔点低2Na+S→Na2S(研磨易爆炸)2Na+Cl2→2NaCl(白烟)(二)钠的化学性质:点燃点燃⑴浮:钠投入水中,浮在水面上(钠的密度比水的密度小)⑵熔:熔成银白色光亮的小球(与水反应放热且钠的熔点较低)⑶游:小球在水面上迅速四处游动(有气体生成推动小球)(4)响:有嘶嘶的响声,直至小球消失(反应剧烈,局部水沸腾气化)(5)红:反应后水溶液变红(溶液显碱性)2Na+2H2O→2NaOH+H22、钠与水的反应2e还原剂氧化剂3、钠与酸的反应比与水反应还激烈;先与酸反应,过量的Na再与水反应。2Na+2HCl→2NaCl+H2若将钠分别投入饱和NaCl、CuSO4、NH4Cl、FeCl3、FeCl2、Al2(SO4)3溶液中。写出反应的离子方程式或化学方程式。4、钠与盐溶液反应CuSO4溶液饱和NH4Cl饱和NaCl化学方程式现象钠溶解,放出无色无味气体、析出晶体2Na+2H2O→2NaOH+H2↑钠溶解,有刺激性气味气体放出2Na+2NH4Cl→2NaCl+H2↑+2NH3↑钠溶解,放出无色无味气体,有蓝色沉淀2Na+2H2O+CuSO4→Na2SO4+H2↑+Cu(OH)2↓先与水反应生成碱,再考虑碱与盐的反应先与水反应生成碱,再考虑碱与盐的反应!!5、钠与有机物的反应2Na+2C2H5OH2C2H5ONa+H2↑2Na+2CH3COOH2CH3COONa+H2↑2Na+2C6H5OH2C6H5ONa+H2↑酸性:CH3COOH>C6H5OH>H2O>C2H5OH(三)钠的存在、保存与制取元素存在形态:游离态(以单质形态存在)化合态(以化合物形态存在)存在:钠在自然界里没有游离态,只能以化合态存在。食盐(NaCl)纯碱(Na2CO3·10H2O)硝酸钠(NaNO3)保存:隔绝空气和水,加煤油密封。制取:电解熔融的氯化钠(四)钠的用途1、制Na2O22、制Na-K合金,做原子反应堆导热剂3、高压钠灯4、还原贵重金属(和氧气反应)(钠的导热性)(黄光射程远,透雾力强)(钠具有还原性)。碱金属的相似性和递变性碱金属的相似性和递变性⑴⑴结构的相似性和递变性结构的相似性和递变性①相似性:最外层一个电子,化学反应中容易失去一个电子,形成+1价的离子。化合物形式相同。 ②递变性:电子层数:Li



















