








《《硫及其化合物·化工生产中的重要非金属元素·硫和二氧化硫》高中化学PPT课件》是由用户上传到老师板报网,本为文库资料,大小为1.19 MB,总共有77页,格式为pptx。授权方式为VIP用户下载,成为老师板报网VIP用户马上下载此课件。文件完整,下载后可编辑修改。
- 文库资料
- 77页
- 1.19 MB
- VIP模板
- pptx
- 数字产品不支持退货
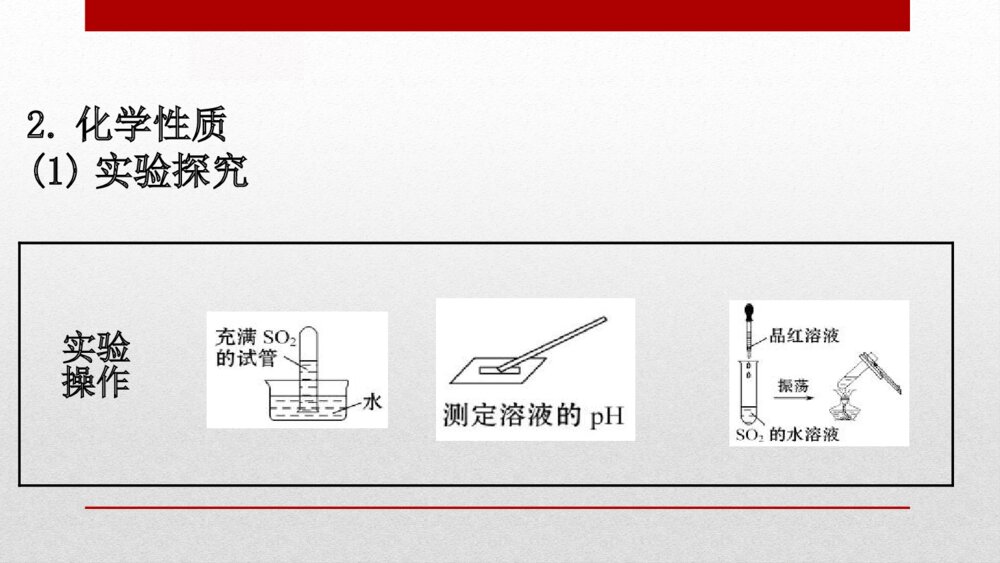
第五章 化工生产中的重要非金属元素 第一节 硫及其化合物第1课时 硫和二氧化硫一、硫1.物理性质俗称颜色状态硬度溶解性水酒精CS2硫黄___色晶体质___,易研成粉末___溶___溶___溶黄脆不微易【微思考】若试管内壁附着有单质硫时,如何洗涤除去?提示:用CS2洗涤——硫单质易溶于CS2。2.化学性质硫的化学性质比较活泼,能与许多金属单质及非金属单质发生化学反应。如:3.用途:硫黄主要用于制造硫酸、化肥、火柴及杀虫剂等,还用于制造黑火药、烟花爆竹等。【微思考】能不能根据Fe、Cu与S、Cl2反应的产物判断S和Cl2的氧化性的强弱?提示:可以。Fe、Cu与S反应生成低价的化合物,Fe、Cu与Cl2反应生成高价的化合物,故Cl2的氧化性大于S。二、二氧化硫1.物理性质颜色状态气味毒性密度溶解性___色气体_______气味有毒比空气______溶于水(1∶40)无刺激性大易2.化学性质(1)实验探究实验操作实验现象________________pH试纸_____振荡后______________,再加热溶液__________结论_____________________________________________________________________试管中液面上升变红溶液红色褪去恢复红色SO2易溶于水SO2的水溶液显酸性SO2具有漂白性,但生成的无色物质不稳定(2)可逆反应①正反应:向_______方向进行的反应;②逆反应:向_______方向进行的反应;③可逆反应:在_________下,既能向正反应方向进行,_____又能向逆反应方向进行的反应。生成物反应物同一条件同时【微思考】氢气与氧气反应可以生成水,电解水可以得到氢气与氧气,该反应是可逆反应吗?提示:不是。氢气与氧气反应可以生成水的条件是燃烧,与电解水的条件不同,故不是可逆反应。(3)SO2的“4种性质”3.用途制硫酸、漂白剂(漂白纸浆、毛、丝等)、杀菌消毒、食品添加剂。【情境·思考】某同学发现夏天爷爷买的白草帽,用了一段时间后变黄了,通过询问身边的人了解到草帽是用“硫黄熏”过的,你是否认可该说法?白草帽变黄的原因是什么?提示:“硫黄熏”这个说法不准确,漂白的原理是利用硫黄在加热条件下与氧气反应生成SO2,SO2具有漂白性,将草帽漂白,并非硫黄直接作用;SO2与有色物质结合生成无色物质,在受热(太阳光照射)等条件下分解放出SO2,又会恢复原色。知识点一 SO2和CO2性质的比较【重点释疑】SO2和CO2性质的比较SO2CO2物理性质色、味无色、刺激性气味无色、无味毒性有毒无毒溶解性易溶(1∶40)可溶(1∶1)SO2CO2化学性质与水反应H2O+SO2H2SO3H2O+CO2H2CO3与碱反应SO2+OH-(少量)====,SO2+2OH-(足量)====+H2OCO2+OH-(少量)====,CO2+2OH-(足量)====+H2O氧化性SO2+2H2S====3S↓+2H2OCO2+C2CO3HSO23SO23CO3HCO高温====3HSO23SO23CO3HCOSO2CO2化学性质还原性2SO2+O22SO3,也能被酸性KMnO4溶液、氯水、溴水等氧化无还原性漂白性有,但不稳定无△催化剂SO2CO2对环境的影响过量排放形成酸雨过量排放引起温室效应【思考·讨论】 (1)CO2和SO2均为酸性氧化物,在性质上具有一定的相似性,结合已有的知识探究能否用澄清石灰水鉴别CO2和SO2,为什么?提示:不能。少量的CO2和SO2通入澄清石灰水中,均产生白色沉淀;足量的CO2和SO2通入澄清石灰水中现象都是先变浑浊后变澄清。其中SO2与Ca(OH)2反应的离子方程式为SO2+Ca2++2OH-====CaSO3↓+H2O,CaSO3+SO2+H2O====Ca2++2。3HSO3HSO(2)如何检验某无色气体是SO2还是CO2?提示:将气体通入品红溶液中,若品红溶液褪为无色,加热,褪色后的溶液又恢复红色,则气体为SO2;若品红溶液不褪色,则为CO2。【案例示范】【典例】(2019·长沙高一检测)浓硫酸和木炭在加热时发生反应的化学方程式是2H2SO4(浓)+CCO2↑+2H2O+2SO2↑。用如图所示各装置设计一个实验,验证浓硫酸与木炭在加热条件下反应产生的各种产物。△====(1)这些装置的连接顺序(按产物气流从左到右的方向)是________→________→________→________(填装置的序号)。 (2)装置②中要检验产物中有水蒸气,则放入的药品是_________________________; 装置③中要检验产物中有二氧化碳气体,则放入的药品是______________;实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色,A瓶溶液的作用是_____________________, B瓶溶液的作用是 ______________, C瓶溶液的作用是 ______________。 【思维建模】解答有关检验SO2和CO2同时存在的问题的思维流程如下:【解析】(1)浓硫酸与木炭共热生成CO2、SO2和H2O,应先检验水蒸气的存在,因为在验证二氧化碳、二氧化硫的存在时都需通过溶液,会带出水蒸气;二氧化碳、二氧化硫都能使澄清的石灰水变浑浊,所以不能先通过澄清的石灰水来检验二氧化碳的存在,应先检验二氧化硫的存在并除去二氧化硫后再检验二氧化碳的存在。故检验流程为检验水蒸气→检验并除尽二氧化硫→检验二氧化碳。(2)检验水蒸气用无水硫酸铜,白色固体遇水变蓝则装置②中要检验产物中有水蒸气,则放入的药品是无水硫酸铜粉末;装置③中要检验产物中有二氧化碳气体,二氧化碳的检验方法为通入澄清的石灰水,使澄清的石灰水变浑浊,则放入的药品是澄清石灰水;实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色,因此装置A中盛有红色的品红溶液来检验二氧化硫;二氧化硫影响二氧化碳的检验,因此检验二氧化碳前先除尽二氧化硫,装置B中盛有的酸性高锰酸钾溶液除去二氧化硫,而不除去二氧化碳,装置C中的红色的品红溶液是用来证明SO2气体已完全除尽的。答案:(1)④ ② ① ③ (2)无水硫酸铜粉末 澄清石灰水 检验二氧化硫的存在 除去气体中的SO2 证明SO2气体已完全除尽【母题追问】(1)装置B中试剂能否使用氢氧化钠溶液?还可以使用什么试剂?提示:不能 溴水。若用氢氧化钠溶液,CO2也被吸收,则无法检验,溴水可以将SO2吸收而不影响CO2。(2)若装置按④①②③连接,得出的结论是什么?提示:能检测出SO2和CO2,不能检测出H2O。因为装置①中会带出水蒸气,故无法通过②中的现象证明反应有水生成。【方法规律】SO2和CO2的鉴别方法试剂现象及结论品红溶液使品红溶液褪色的是SO2;不能使品红溶液褪色的是CO2氢硫酸出现浑浊的是SO2,无明显现象的是CO2高锰酸钾溶液使紫色褪去的是SO2,无明显现象的是CO2试剂现象及结论溴水使橙色褪去的是SO2,无明显现象的是CO2碘水(含淀粉)使蓝色褪去的是SO2,无明显现象的是CO2硝酸酸化的硝酸钡溶液产生白色沉淀的是SO2,无明显现象的是CO2【迁移·应用】1.(2019·日照高一检测)能证明SO2具有漂白性的是( )A.酸性KMnO4溶液中通入SO2气体后紫红色消失B.滴有酚酞的NaOH溶液中通入SO2气体后红色消失C.品红溶液中通入SO2气体后红色消失D.溴水中通入SO2气体后橙色消失【解析】选C。SO2气体通入酸性KMnO4溶液后紫红色消失,通入溴水后橙色消失都是利用了SO2的还原性;滴有酚酞的NaOH溶液红色消失,是因为通入的SO2气体与水反应生成了酸,酸消耗了NaOH;只有SO2气体通入品红溶液后红色消失,才能证明SO2具有漂白性。2.(2019·临沂高一检测)实验室可用如图装置(略去部分夹持仪器)制取SO2并验证其性质。(1)盛装70%H2SO4溶液的仪器名称为________。仪器组装完成后,关闭两端活塞,向装置B的长颈漏斗内注入液体至形成一段液柱,若________,则整个装置气密性良好。 (2)装置B的作用之一是通过观察产生气泡的多少判断SO2生成的快慢,其中的液体最好选择________(填代号)。 a.蒸馏水b.饱和Na2CO3溶液c.饱和NaHSO3溶液d.饱和NaOH溶液(3)C试管中的试剂可以验证二氧化硫的氧化性,现象为_______________________。 (4)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行如下实验:方案Ⅰ:向第一份溶液中加入AgNO3溶液,有白色沉淀生成;方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;方案Ⅲ:向第三份溶液中加入BaCl2溶液,产生白色沉淀。上述方案合理的是方案______(填“Ⅰ”“Ⅱ”或“Ⅲ”);试管D中发生反应的离子方程式为____________________________。 (5)装置E的作用是________。装置F中为________溶液。 【解析】(1)根据仪器特点,该仪器名称为分液漏斗,液柱高度保持不变,说明气密性良好;(2)SO2易溶于水,能与NaOH溶液、Na2CO3溶液反应,但在饱和NaHSO3溶液中溶解度较小,c项正确;(3)SO2能将氧化,生成硫单质,所以现象为有浅黄色沉淀生成;2S2S(4)方案Ⅰ,氯水中加入AgNO3溶液也可得到白色沉淀;方案Ⅱ中二氧化硫和氯水均可使品红褪色;方案Ⅲ中产生沉淀可证明SO2与Cl2发生了氧化还原反应(因溶液显酸性,不会产生BaSO3沉淀,而是BaSO4沉淀),选方案Ⅲ;(5)E为安全瓶,防止倒吸;装置F起到吸收尾气中SO2的作用,可选用NaOH溶液。答案:(1)分液漏斗 液柱高度保持不变 (2)c (3)有浅黄色沉淀生成 (4)Ⅲ SO2+Cl2+2H2O====4H+++2Cl- (5)防止倒吸 NaOH(合理即可)24SO24SO【补偿训练】 (2019·东莞高一检测)检验SO2气体中是否混有CO2气体,可采用的方法是( )A.通过品红溶液B.通过澄清石灰水C.先通过NaOH溶液,再通过澄清石灰水D.先通过酸性KMnO4溶液,再通过澄清石灰水【解析】选D。A项检验的是SO2而不是CO2;B项中不管是否混有CO2,均有白色沉淀;C项中不管是否混有CO2,均无白色沉淀生成;D项在通过酸性KMnO4溶液时混合气体中仅SO2被吸收,再通过澄清石灰水若有白色沉淀,说明混有CO2;若无白色沉淀,说明不混有CO2。综上分析,D正确。知识点二 常见的漂白剂及漂白原理【重点释疑】常见的能用于漂白的物质的比较类型吸附型氧化型化合型物质活性炭氯气、漂白粉(液)、次氯酸二氧化硫类型吸附型氧化型化合型漂白原理吸附漂白利用次氯酸的强氧化性进行漂白与有色物质化合生成不稳定的无色物质变化类别物理变化氧化还原反应化学变化漂白特点不可逆加热恢复原色能漂白的物质一般用于溶液漂白可漂白所有有机色质具有选择性,如品红、棉、麻、草等【易错提醒】(1)漂白是指使有机色质褪色,漂白剂不一定使无机色质(如KMnO4、CuSO4·H2O等)褪色,即使能使无机色质褪色,也不称漂白作用(如SO2使KMnO4溶液褪色)。(2)活性炭的吸附是物理变化,而化合型、氧化型漂白均为化学变化。(3)Na2O2具有漂白性,但通常不用它作漂白剂,因为Na2O2具有较强的腐蚀性。【思考·讨论】 (1)分别将SO2及Cl2通入品红溶液中并加热,现象有何不同?若分别通入紫色石蕊试液中呢?提示:(2)将等物质的量的SO2和Cl2同时通入同一品红溶液中,有何现象?请解释原因。提示:等物质的量的SO2和Cl2同时通入同一品红溶液中,发生反应SO2+Cl2+2H2O====H2SO4+2HCl,失去漂白能力,品红溶液不褪色。【案例示范】【典例】(2019·聊城高一检测)下列说法正确的是( )A.SO2具有漂白性,能使品红溶液和酸性KMnO4溶液褪色且常作食品的漂白剂B.活性炭、胶体、H2O2、O3等都有漂白性C.氯气具有漂白性D.Na2O2也有漂白性,其漂白原理和SO2相似【解题指南】解答本题应注意以下两点:(1)SO2具有还原性,可以使一些具有氧化性的有色溶液褪色。(2)氯气本身没有漂白性,与水反应生成的次氯酸具有漂白性。【解析】选B。SO2使酸性KMnO4溶液褪色是因为其具有还原性而不是漂白性,且SO2有毒,不能用于食品漂白,A错误;活性炭、胶体具有吸附性,能吸附色素,H2O2、O3、Na2O2等有强氧化性,能氧化色素物质,B正确,D错误;氯气没有漂白性,C错误。【母题追问】(1)将A中反应后的溶液加热分别有什么现象?提示:加热后褪色的品红溶液恢复红色,而褪色后的酸性KMnO4溶液无明显现象。(2)上题涉及的物质既能用于漂白又能用于杀菌消毒的有哪些?提示:H2O2、O3、氯气、Na2O2。既能漂白又能杀菌消毒的物质具有(或与水反应产生的物质具有)强氧化性。【迁移·应用】1.(2019·抚州高一检测)A、B是两种常温下有刺激性气味的气体。将A通入品红溶液中,品红溶液变为无色;将B通入品红溶液中,品红溶液也变为无色。将A通入紫色石蕊溶液中,溶液变为红色;将B通入紫色石蕊溶液中,溶液先变红后褪色。将A和B按1︰1的体积比充分混合,通入品红溶液中,品红溶液不褪色,通入紫色石蕊溶液中,溶液只变红不褪色。试回答下列问题:(1)写出A、B的化学式:A________;B________。 (2)写出A与NaOH溶液反应的化学方程式:_________________或 _________________。 (3)写出B与NaOH溶液反应的离子方程式:__________________________。 (4)加热通入A后变为无色的品红溶液,现象是________________________;加热通入B后变为无色的品红溶液,现象是 _________________。 【解析】具有漂白作用,能使品红溶液褪色的气体有Cl2、SO2、O3等。A气体不能使紫色石蕊溶液褪色,但能使紫色石蕊溶液变红色,所以A为SO2:H2O+SO2H2SO3;B气体使紫色石蕊溶液先变红后褪色,为Cl2:H2O+Cl2HCl+HClO,HCl使紫色石蕊溶液变红,HClO能使紫色石蕊溶液变为无色。如果将Cl2与SO2等体积混合通入溶液中,则发生下列反应:Cl2+SO2+2H2O====H2SO4+2HCl,生成的盐酸和硫酸都没有漂白作用,它们只能使紫色石蕊溶液变红。答案:(1)SO2 Cl2(2)2NaOH+SO2(少量)====Na2SO3+H2ONaOH+SO2(过量)====NaHSO3(3)2OH-+Cl2Cl-+ClO-+H2O(4)溶液变为红色 无明显变化2.下列物质都可用于漂白,但漂白原理与其他三种物质不相同的是( )A.ClO2 B.SO2 C.H2O2 D.NaClO【解析】选B。ClO2、H2O2、NaClO均具有氧化性,具有漂白性,漂白的原理是与有色物质发生氧化还原反应,是永久性的和不可逆的过程;SO2具有漂白性,原理是与有色物质结合成一种无色的不稳定的物质,加热颜色又恢复,因此SO2的漂白是可逆的、非氧化还原反应的、暂时性的过程,答案选B。【素养提升】银耳俗称白木耳,属于真菌类的食物,它是现代人们特别喜欢的一种养生佳品。在选购的时候应该怎么选呢?越白的银耳越好吗?其实不然,过白的银耳很有可能是被不法的商家加入了漂白剂,会导致这些银耳残留二氧化硫。SO2和Cl2常用于漂白,为探究SO2和Cl2的漂白性,某同学将足量的SO2和Cl2分别通入石蕊试液中,发现通SO2的溶液只是变红,而通Cl2的溶液先变红后褪色。为了探索比较SO2和Cl2的漂白原理,该同学继续做了如下对比实验:a.将干燥的SO2和干燥的Cl2分别通到干燥的品红试纸上,发现红色试纸均不褪色;b.将SO2和Cl2分别通入品红溶液中,发现品红溶液均褪色;c.加热b中漂白后的溶液,发现前者恢复红色,并产生刺激性气味气体,后者不能;d.将SO2和Cl2分别持续通入紫色石蕊试液中,发现前者只变红,不褪色,后者先变红,后褪色。(1)由实验a可以得到什么结论?(科学探究与创新意识)(2)由实验a、b可以得到什么结论?(科学探究与创新意识)(3)由实验c、d可以得到什么结论?(科学探究与创新意识)【解析】实验a,说明干燥的SO2和Cl2均无漂白性;实验b,说明在水的参与下SO2、Cl2具有漂白性;实验c,说明HClO的漂白稳定,SO2的漂白不稳定,实验d说明SO2不能漂白所有有机色质。答案:(1)SO2和Cl2本身都没有漂白性(2)起漂白作用的分别是SO2和Cl2与水反应后的产物H2SO3和HClO(3)H2SO3只能与某些有机色质发生化合反应,生成不稳定的无色物质,产物受热分解再放出SO2;HClO能与很多有机色质发生氧化还原反应,生成物较稳定【课堂回眸】



















