





《人教版高中·化学能与热能PPT课件下载》是由用户上传到老师板报网,本为文库资料,大小为2.3 MB,总共有40页,格式为ppt。授权方式为VIP用户下载,成为老师板报网VIP用户马上下载此课件。文件完整,下载后可编辑修改。
- 文库资料
- 40页
- 2.3 MB
- VIP模板
- ppt
- 数字产品不支持退货
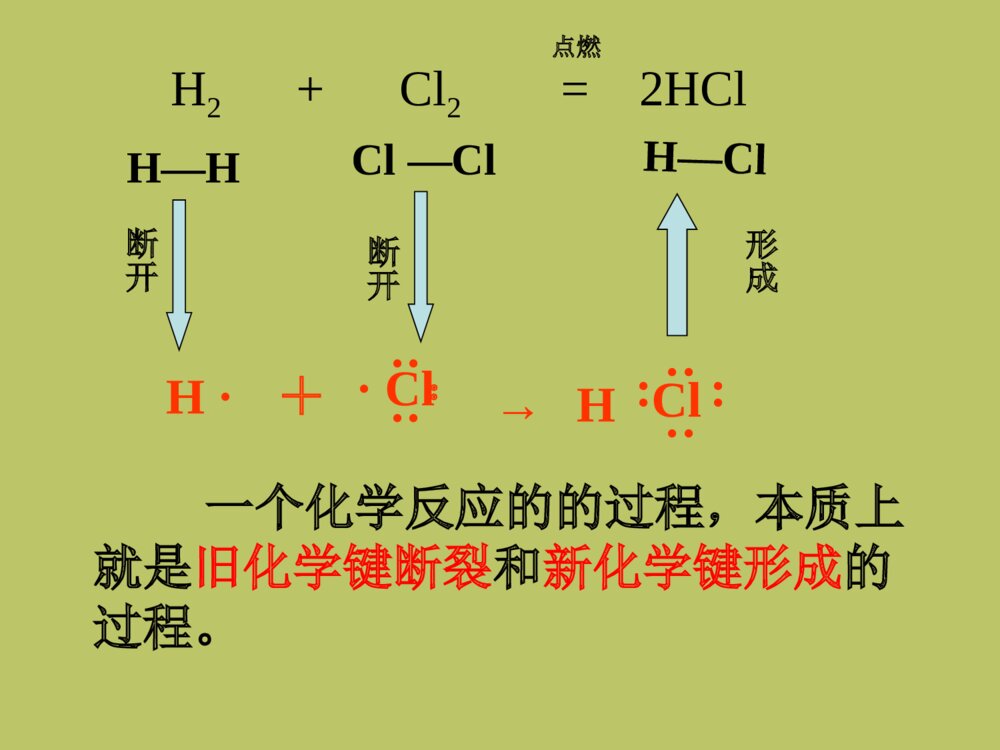
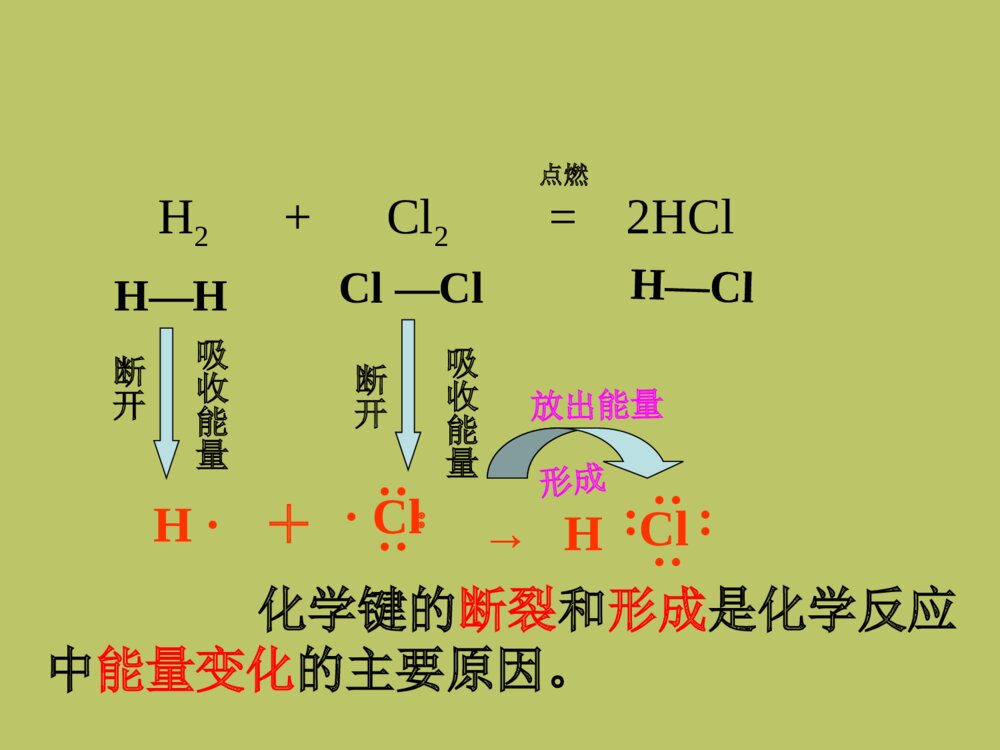
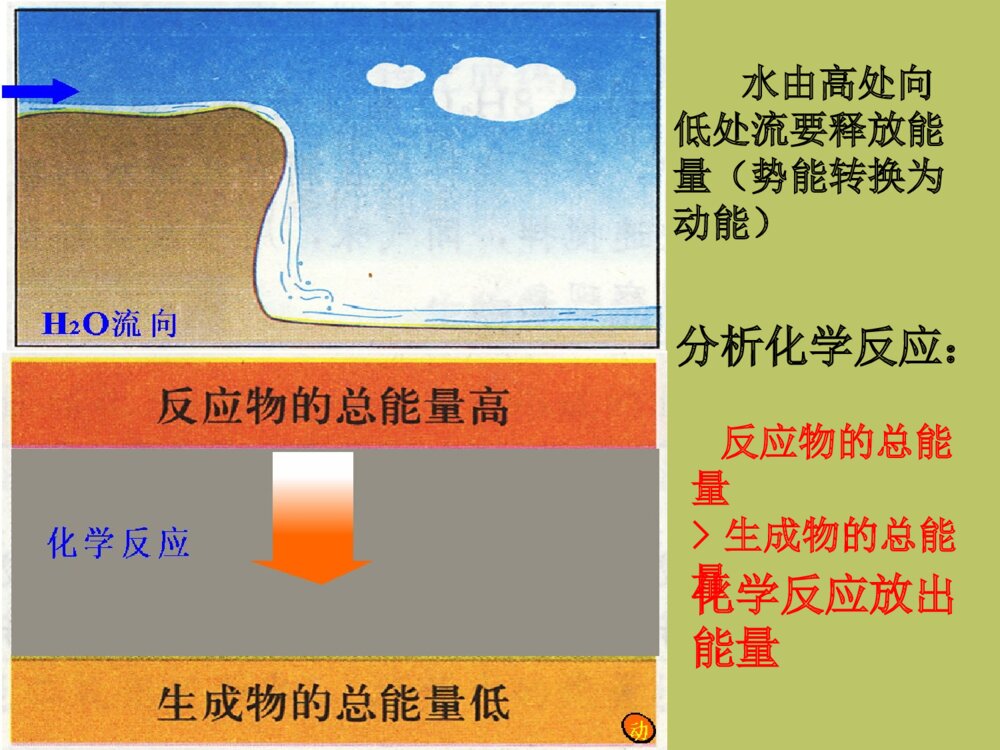
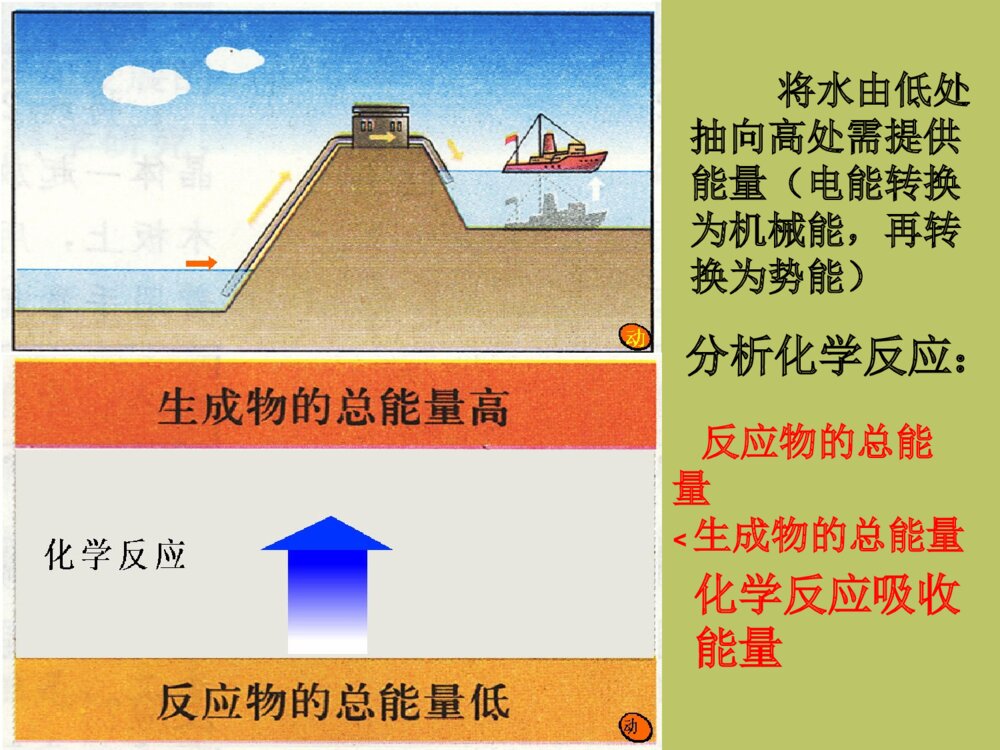
新课标人教版化学必修Ⅱ第二章 第一节第二章 第一节化学能与热能化学能与热能湘乡二中陈劲松2023年9月17日能源是人类赖以生存和发展的物质基础,我们每时每刻、分分秒秒都离不开它。迄今为止,人类所能利用的能源主要是化学能、电能、以及核能等等。但是,由于人类大量开发和浪费资源,造成了资源的不合理利用从而引发了不可回避的能源危机。能源、材料,信息被称为现代社会发展的三大支柱第一节化学能与热能一、化学键与化学反应中能量变化的关系1、化学反应的本质是?以氢气在氯气中燃烧为例,用化学键的观点分析反应的本质过程。H····Cl··:+→Cl····H····H2+Cl2=2HClH—HCl—ClH—Cl断开断开点燃一个化学反应的的过程,本质上就是旧化学键断裂和新化学键形成的过程。形成H····Cl··:+→Cl····H····H2+Cl2=2HClH—HCl—ClH—Cl吸收能量断开断开吸收能量形成放出能量点燃化学键的断裂和形成是化学反应中能量变化的主要原因。【思考与交流】在化学反应中,随着物质的变化,既有反应物中化学键的断裂,又有生成物中化学键的形成,化学能也随之而改变。那么,一个化学反应吸收能量还是放出能量是由什么决定的呢?2、一个化学反应吸收能量还是放出能量的决定因素水由高处向低处流要释放能量(势能转换为动能)分析化学反应:反应物的总能量>生成物的总能量化学反应放出能量将水由低处抽向高处需提供能量(电能转换为机械能,再转换为势能)分析化学反应:反应物的总能量<生成物的总能量化学反应吸收能量规律1、如果反应物所具有的总能量高于生成物所具有的总能量,那么在发生化学反应时,就有部分能量以热的形式释放出来;2、如果反应物所具有的总能量低于生成物所具有的总能量,那么在发生化学反应时,反应物就需要吸收能量,才能转化为生成物。能量反应过程反应过程反应物生成物能量放热反应吸热反应反应物生成物规律【归纳小结】一个化学反应是放热反应还是吸热反应取决于:取决于所有断键吸收的总能量与所有形成新键放出的总能量的相对大小,即取决于反应物的总能量与生成物的总能量的相对大小。反应物的能量之和E反生成物的能量之和E生(1)若E反>E生,(2)若E反0表示吸热反应2、计算方法:反应物的总能量减去生成物的总能量所得的数值3、分类:①燃烧热,②中和热3、分类:①燃烧热,②中和热①燃烧热在101KPa时,1mol纯物质完全燃烧生成稳定的化合物时所放出的热量叫做该物质的燃烧热②中和热在稀溶液中,酸跟碱发生中和反应生成1mol水所释放的热量叫中和热。室温下中和热约为57.3KJ/mol中和反应,燃烧反应均为放热反应1、当物质发生化学反应,断开反应物中的化学键要;而形成生成物中的化学键要。一个化学反应是释放能量还是吸收能量取决于。吸收能量放出能量反应物总能量与生成物总能量的相对大小课堂练习:2、若反应物的总能量>生成物的总能量,化学反应能量。若反应物的总能量<生成物的总能量,化学反应能量。放出吸收•3、一个确定的化学反应在发生过程中是吸收能量还是放出能量,决定于•___________________________________•_____________,有部分能量释放出来;__________,反应物要吸收能量,才•能转化为生成物。•4、是化学反应中能量变化的主要原因。反应物的总能量与生成物的总能量的相对大小。若E反>E生若E反



















