







《高中化学铅蓄电池PPT课件下载(共49页)》是由用户上传到老师板报网,本为文库资料,大小为2.45 MB,总共有49页,格式为ppt。授权方式为VIP用户下载,成为老师板报网VIP用户马上下载此课件。文件完整,下载后可编辑修改。
- 文库资料
- 49页
- 2.45 MB
- VIP模板
- ppt
- 数字产品不支持退货
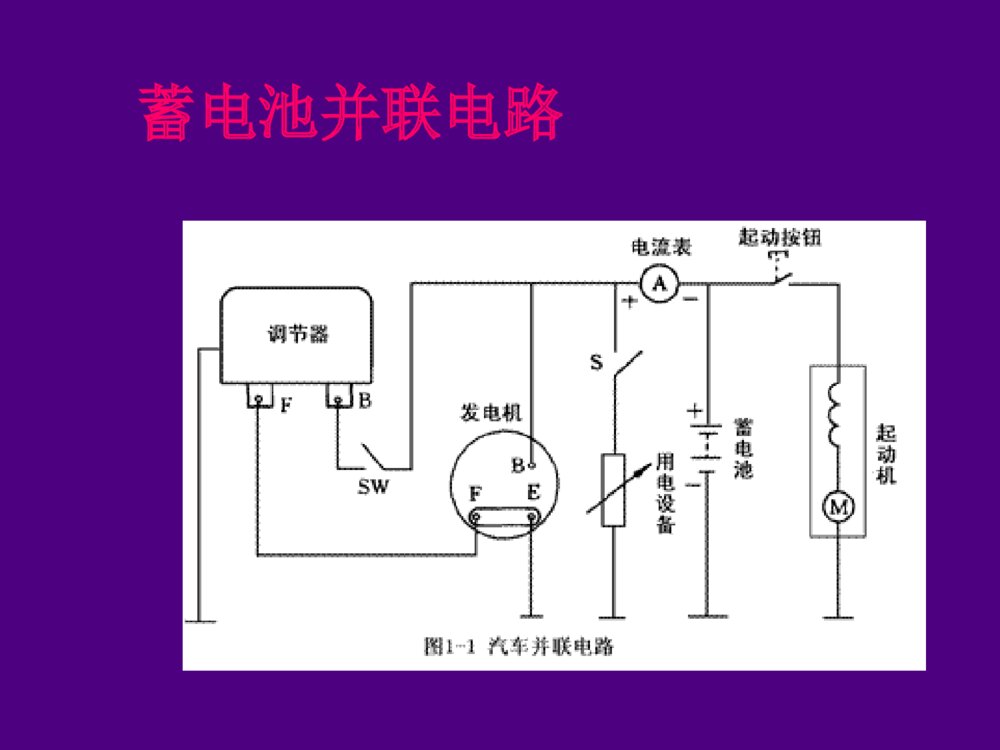
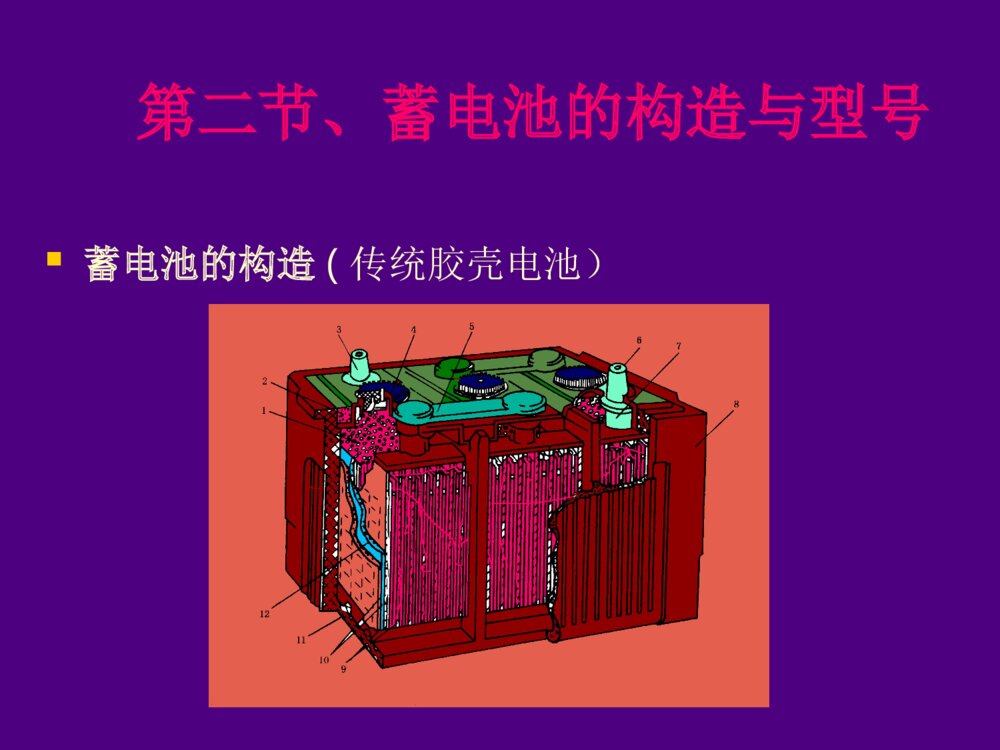
汽车起动用铅酸蓄电池第一节、汽车蓄电池概述蓄电池是一种将化学能转变为电能的装置,属于可逆的直流电源。应用最广泛的汽车蓄电池是铅酸蓄电池。蓄电池最主要的作用是:发动机工作时向起动机和点火装置供电。汽油机起动电流为200-600A有的柴油机起动电流达1000A。蓄电池并联电路按使用来分为:动力型蓄电池、起动型蓄电池、储能型蓄电池等按蓄电池的结构分为:普通起动用蓄电池(湿荷电蓄电池H、干荷电蓄电池A、非荷电蓄电池):需维护或少维护。免维护起动用蓄电池阀控蓄电池(胶体电解质蓄电池、AGM吸附式蓄电池)汽车上采用铅酸蓄电池,主要目的是使起动发动机。现代汽车起动用蓄电池主要使用:干荷电蓄电池免维护蓄电池不同类型的铅酸蓄电池干荷蓄电池极板处于干燥的已充电状态和无电解液贮存的蓄电池。干荷蓄电池加足电解液后,静放20~30min即可使用。干荷蓄电池的工艺特点在负极板的铅膏中加入抗氧化剂、负极板在化成后经过水洗和浸渍防氧剂、经特殊工艺干燥处理,提高了负极板上的海绵状纯铅的憎水性和抗氧化性,可以干荷电贮存。免维护蓄电池极板栅架采用铅钙锡合金制成,消除了锑的副作用:自放电少、使用中不需加水;采用袋式PE隔板,可避免活性物质脱落、极板短路:使用寿命长;采用新型安全通气装置:回收水汽外壳由聚丙烯塑料制成:重量轻、体积小。免维护蓄电池的产品特点水份散失少自放电小连接件腐蚀小起动性能好使用寿命长蓄电池的功用1.发动机启动时,向启动机和点火系统供电2.发动机低速运转时,向用电设备和发电机磁场绕组供电。(应用中应避免)3.发动机运转时,将发电机剩余电能转化为化学能储存起来;4.发电机过载时,协助发电机向用电设备供电5.蓄电池相当于一个大电容器,能吸收电路中出现的舒瞬时过电压,保护电子元件,保持汽车电器系统电压稳定对蓄电池的要求启动发动机时,蓄电池在5~10S内,要向启动机连续供给强大电流(汽油机200~600A,柴油机800~1000A)因此,对蓄电池的要求是:容量大、内阻小、有足够的启动能力。第二节、蓄电池的构造与型号蓄电池的构造(传统胶壳电池)第二节、蓄电池的构造与型号蓄电池的构造(塑壳干荷电、少维护电池)蓄电池的基本构造(现代免维护蓄电池)蓄电池槽排气盖蓄电池盖端子排气孔蓄电池的基本构造极板隔板外壳电解液极板极板:是蓄电池的基本部件,由它接受充入的电能和向外释放电能。极板分正极板和负极板两种。正极板上的活性物质是二氧化铅,呈棕红色;负极板上的活性物质是海绵状纯铅,呈青灰色。极板极板栅架活性物质隔板为了避免相互接触而短路,正负极板之间要用绝缘的隔板隔开。隔板材料应具有多孔性结构,以便电解液自由渗透,而且化学性能应稳定,具有良好的耐酸性和抗氧化性。电解液铅酸蓄电池的电解液,是由相对密度1.84的纯硫酸和蒸馏水配制而成。密度一般在1.24-1.31g/cm3的范围之内。电解液的纯度是影响蓄电池的电气性能和使用寿命的重要因素,一般工业用硫酸和普通水中,因含有铁、铜等有害杂质,绝对不能加入到蓄电池中去,否则容易自行放电,并且容易损坏极板。因此,蓄电池电解液要用规定的蓄电池专用硫酸和蒸馏水配制。外壳蓄电池外壳为一整体式结构的容器,极板、隔板和电解液均装入外壳内。蓄电池电压一般有6V和12V两种规格,因此,外壳内由间壁分成3个和6个互不相通的单格。外壳应耐酸、耐热、耐寒、抗震动,并具有足够的机械强度。外壳蓄电池的型号、规格蓄电池的产品型号:GB/T5008.2-2005对起动用铅酸蓄电池的规格、外形尺寸、端子位置等进行了详细的规定。GB/T5008.2-2005引用了原机械工业部部颁标准JB2599的规定,铅蓄电地产品型号分为三段。蓄电池的型号、规格以6—QA—60型电池为例:6-----代表电池单格数量为6个Q-----代表汽车起动用蓄电池A-----代表干式荷电,W---代表免维护60----表示电池容量为60Ah奇瑞汽车用蓄电池6-QW-75即是6个单格电池额定电压12伏额定容量75Ah起动型免维护蓄电池奇瑞汽车用蓄电池A11车用L2400电池B11车用6-QW-75电池T11车用6-QW-75电池S11车用6-QW-45电池S21车用6-QW-45电池商标标签内容警示标示标示的含义:1.注意阅读说明书2.注意有腐蚀性液体3.禁止靠近明火和火焰4.对蓄电池进行操作时注意穿戴好防护用品警示标示5.严禁儿童接近6.注意有爆炸性气体7.蓄电池禁止放入垃圾箱8.旧蓄电池应该进行适当的处理,并且可以回收再利用第三节、蓄电池的工作原理及特性双极硫酸盐化理论蓄电池中参与化学反应的物质,正极板上是pbO2负极板上是pb电解液是硫酸水溶液蓄电池放电时,正极板上的pbo2和负极板上的pb都变成pbso4水溶液电解液中的H2SO4减少,相对密度下降。蓄电池充电时,则按相反的方向变化。一、蓄电池的工作原理蓄电池的化学反应方程式为:1.电动势的建立蓄电池的电动势是正、负极浸入电解液后产生的。其反应过程见图1-8所示负极板:铅溶于电解液中,失电子生成Pb2+Pb-2e→Pb2+电子留在负极板上,和Pb2+吸引,使负极具有负电位,为-0.1V。电动势的建立正极板:PbO2溶于电解液 PbO2+2H2O→Pb(OH)4 Pb(OH)4→Pb4++4OH-OH-留在电解液中,Pb4+沉附在正极表面,使正极板有+2.0V在外电路未接通时,反应达到动态平衡时,静止电动势为:E=2.0-(-0.1)=2.1V电动势的建立2、放电过程将蓄电池的化学能转换成电能的过程称为放电过程。2、放电过程如果将蓄电池与外电路的负荷接通,电子e从负极板经过外电路的负荷流往正极板,使正极板的电位下降,从而破坏了原有的平衡状态。发生电化学反应。从理论上说,蓄电池这种放电将极板上所有物质全部转变为硫酸铅,但实际转化的只有30-50%。3、充电过程将电能转换成蓄电池化学能的过程称为充电过程,它是放电反应的逆过程。3、充电过程充电时蓄电池的正负两极接通直流电源当电源电压高于蓄电池的电动势E时,电流由蓄电池的正极流入,从蓄电池的负极流出,也就是电子由正极板经外电路流往负极板。这时正负极板发生的化学反应正好与放电过程相反,其化学反应过程如图所示。蓄电池充放电过程结论蓄电池在放电时,电解液中的硫酸将逐渐减少,而水将逐渐增多,电解液相对密度下降。蓄电池在充电时,电解液中的硫酸将逐渐增多,而水将逐渐减少,电解液相对密度增加。在充放电时,电解液浓度发生变化,主要是由于正极板的活性物质化学反应的结果,因此要求正极极处的电解液流动性要好。在装配蓄电池时,应将隔板有沟槽的一面对着正极板,以便电解液流通。二、蓄电池的工作特性蓄电池的静止电动势及基本电特性蓄电池的内阻蓄电池的放电特性蓄电池的充电特性1、蓄电池的静止电动势及基本电特性静止电动势ES蓄电池处于静止状态时,正负极板之间的电位差(即开路电压)称为静止电动势。开路电压:理论上,开路状态下的端电压并不等于电池的电动势。但是,开路电压在数值上很接近蓄电池的静止电动势,可以用开路电压代替静止电动势。一般规定铅蓄电池的额定开路电压为2.0V。开路电压(静止电动势)公式铅钙电池:ES=0.85+ρ25°C(V)或铅锑电池:ES=0.84+ρ25°C(V)汽车用蓄电池的电解液密度一般在1.12-1.30g/cm3之间,因此ES=1.97~2.15(V)1、蓄电池的静止电动势及基本电特性蓄电池端电压的测量:端电压包括开路电压、放电电压和充电电压,取决于蓄电池的工作状况。一般发动机未工作时测量蓄电池电压为开路电压为12V。(12~12.7V)一般发动机工作时测量蓄电池电压为充电电压为14V。(13.8~14.4V)起动时测量蓄电池电压为放电电电压约为8-11V。实际测量时采用放电计模拟启动状态。2、蓄电池的放电特性蓄电池的放电特性是指在恒流放电过程中,蓄电池的端电压和电解液相对密度随时间而变化的规律。将完全充足电的蓄电池以20h放电率的电流进行放电,在放电过程中不断地调节外接的电位器,使放电电流保持稳定不变,每隔一定的时间,测量端电压和电解液密度,得到如图所示的放电特性曲线。放电特性曲线2、蓄电池的放电特性(1)开始放电阶段端电压由2.14V迅速下降至2.1V极板孔隙内硫酸迅速消耗,电解液密度迅速下降,浓差极化增大,端电压迅速下降。(2)相对稳定阶段端电压由缓慢下降至1.85V极板孔隙外向孔隙内扩散的硫酸与孔隙内消耗的硫酸达到动态平衡,孔内外电解液密度一起缓慢下降,所以端电压缓慢下降。2、蓄电池的放电特性(3)迅速下降阶段端电压由1.85V迅速下降至1.75V。放电接近终了时,电化学极化、浓差极化、欧姆极化显著增大,端电压迅速下降。蓄电池放电终了的特征3、蓄电池的充电特性(恒流充电)在恒流充电过程中,蓄电池的端电压与电解液相对密度随时间而变化的规律。充电电源必须采用直流电源,以一定的电流人向一只完全放电的蓄电地进行充电。保持充电电流入不变,每隔一定时间测量单格电池的端电压和电解液相对密度。可以绘制出蓄电池的充电特性曲线,如图所示。蓄电池的充电特性(恒流充电)(1)充电开始阶段端电压迅速上升。开始充电时,孔隙内迅速生成硫酸,浓差极化增大,端电压迅速上升。(2)稳定上升阶段端电压缓慢上升至2.4V左右。孔隙内生成的硫酸向孔隙外扩散,当硫酸生成的速度与扩散速度达到平衡时,端电压随整个容器内电解液密度变化而缓慢上升。蓄电池的充电特性(恒流充电)(3)充电末期电压迅速上升到2.7V左右,且稳定不变,电解液呈沸腾状态。活性物质还原反应结束后的充电称为过充电,充电电流用于电解水,应避免长时间过充电。蓄电池的充满电(恒流充电)的特征端电压上升到最大值2.7V,并在2h~3h内不在增加。电解液相对密度上升到最大值1.28g/cm3蓄电池内产生大量气泡。第四节、蓄电池的生产工艺流程见培训材料。



















