







《高中必修一化学实验PPT课件下载》是由用户上传到老师板报网,本为文库资料,大小为862.5 KB,总共有36页,格式为ppt。授权方式为VIP用户下载,成为老师板报网VIP用户马上下载此课件。文件完整,下载后可编辑修改。
- 文库资料
- 36页
- 862.5 KB
- VIP模板
- ppt
- 数字产品不支持退货
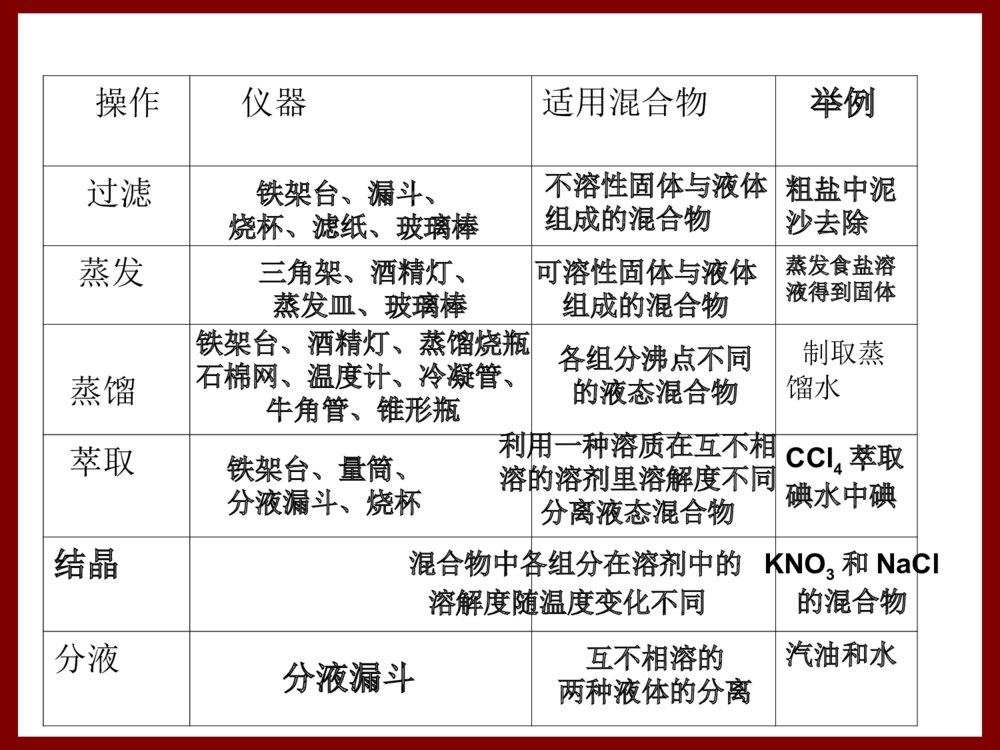
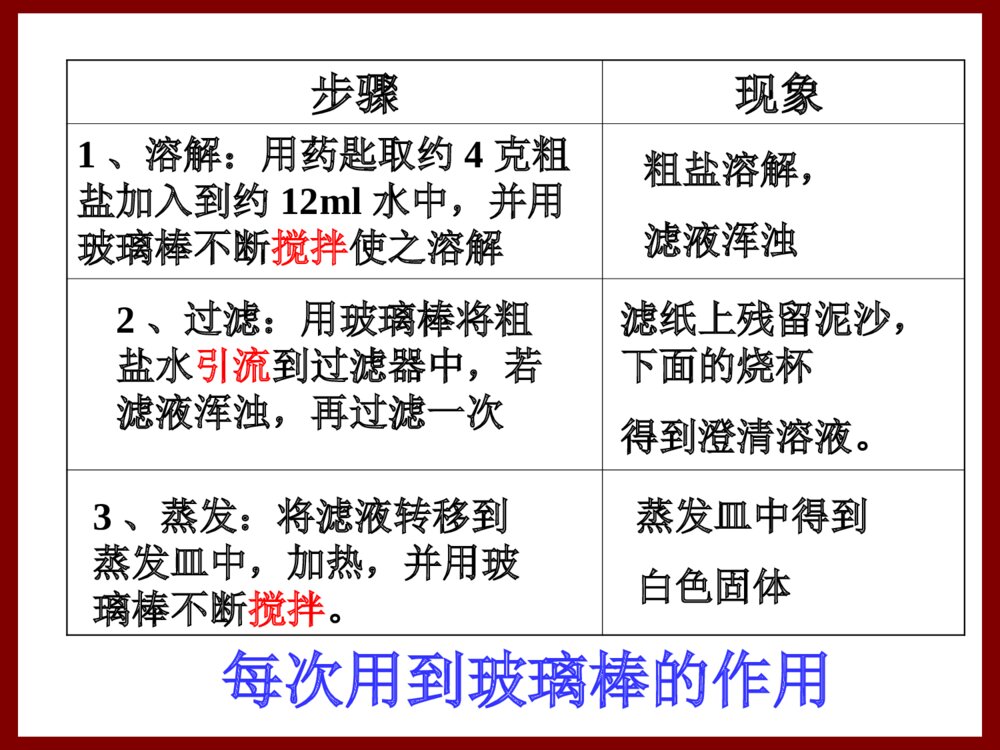
一化学实验安全1.不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛;2.不小心将碱迸溅到眼中,用水洗净后再用稀硼酸溶液淋洗;3.不慎将浓碱溶液溅到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液;4.不慎将浓硫酸倒在皮肤上,宜用干抹布拭去,在用大量水冲洗,最后涂上稀的NaHCO3溶液二分离和提纯有哪些方法,适用范围是什么,需要哪些仪器和用具?操作仪器适用混合物举例过滤粗盐中泥沙去除蒸发蒸发食盐溶液得到固体蒸馏制取蒸馏水萃取CCl4萃取碘水中碘结晶分液汽油和水铁架台、漏斗、烧杯、滤纸、玻璃棒不溶性固体与液体组成的混合物三角架、酒精灯、蒸发皿、玻璃棒可溶性固体与液体组成的混合物铁架台、酒精灯、蒸馏烧瓶石棉网、温度计、冷凝管、牛角管、锥形瓶各组分沸点不同的液态混合物铁架台、量筒、分液漏斗、烧杯利用一种溶质在互不相溶的溶剂里溶解度不同分离液态混合物互不相溶的两种液体的分离分液漏斗混合物中各组分在溶剂中的溶解度随温度变化不同KNO3和NaCl的混合物在过滤操作中应注意的问题贴:滤纸要紧贴漏斗内壁上,中间不留气泡;低:①滤纸边缘要低于漏斗口边缘,②漏斗内的液面要低于滤纸边缘;靠:①倾倒液体的烧杯口要紧靠引流的玻璃棒,②引流的玻璃棒的下端要靠在三层滤纸处,③漏斗下端的管口要紧靠承接滤液的烧杯内壁。三靠的目的都是防止液体飞溅。滤液浑浊的可能原因:①滤纸破损②仪器不干净③漏斗中的溶液液面高于滤纸的边缘。处理方法:将滤液再过滤一遍蒸发操作应注意什么问题?⑴蒸发皿的液体不超过容积的2/3(2)加热时,用玻璃棒不断搅拌⑶有较多晶体出现时,即停止加热(4)取下未冷却的蒸发皿时,要放在石棉网步骤现象1、溶解:用药匙取约4克粗盐加入到约12ml水中,并用玻璃棒不断搅拌使之溶解粗盐溶解,滤液浑浊2、过滤:用玻璃棒将粗盐水引流到过滤器中,若滤液浑浊,再过滤一次3、蒸发:将滤液转移到蒸发皿中,加热,并用玻璃棒不断搅拌。蒸发皿中得到白色固体滤纸上残留泥沙,下面的烧杯得到澄清溶液。每次用到玻璃棒的作用夯实基础1.实验室进行NaCl溶液蒸发时,一般有以下操作过程:①放置酒精灯 ②固定铁圈位置③放置蒸发皿 ④加热搅拌 ⑤停止加热,余热蒸干。其中正确的操作顺序是( )A.②③④⑤① B.①②③④⑤ C.②③①④⑤ D.②①③④⑤B仪器装置顺序:从下往上;从左往右2.在粗盐提纯的实验中,蒸发时正确的操作是( )A.把浑浊的液体倒入蒸发皿内加热B.开始析出晶体后用玻璃棒搅拌C.待水分完全蒸干后停止加热D.蒸发皿中发现大量固体时即停止加热D进行蒸馏操作时要注意①在蒸馏烧瓶中放入少量碎瓷片,防止液体暴沸;②温度计水银球的位置应与支管口下缘位于同一水平线上(?);③蒸馏烧瓶中所盛放液体不能超过其容积的2/3,也不能少于1/3;④冷凝管中冷却水从下口进,上口出(?);⑤加热温度不能超过混合物中沸点最高物质的沸点。蒸发与蒸馏的区别加热为了获得溶液的残留物(浓缩后的浓溶液或蒸干后的固体物质)时,要用蒸发;加热是为了收集蒸气的冷凝体时,要用蒸馏。萃取和分液如何来操作?萃取剂的选择需要注意什么?萃取的操作方法如下:①用普通漏斗把待萃取的溶液注入分液漏斗,再注入足量萃取液;②随即振荡,使溶质充分转移到萃取剂中。振荡的方法是用右手压住上口玻璃塞,左手握住活塞部分,反复倒转漏斗并用力振荡;③然后将分液漏斗置于铁架台的铁环上静置,待分层后进行分液;④蒸发萃取剂?即可得到纯净的溶质。为把溶质分离干净,一般需多次萃取。分液的操作方法①用普通漏斗把要分离的液体注入分液漏斗内,盖好玻璃塞;②将分液漏斗置于铁架台的铁圈上,静置,分层;③将玻璃塞打开,或使塞上的凹槽对准漏斗口上的小孔再盖好,使漏斗内外空气相通,以保证漏斗里的液体能够流出;④打开活塞,使下层液体慢慢流出,放入烧杯,待下层液体流完立即关闭活塞,注意不可使上层液体流出;⑤从漏斗上端口倒出上层液体。【归纳总结】1.选择萃取剂的原则是什么?①萃取剂与原溶剂不相溶;②被萃取物质在萃取剂中的溶解度要比在原溶剂中的溶解度大得多;③萃取剂与原溶质、溶剂均不能发生化学反应。常用的萃取剂有哪些?有机溶剂如苯(密度比水小),四氯化碳(密度比水大),汽油夯实基础:3.下列关于混合物分离的方法中,能够分离KNO3和NaCl的是( )A.溶解过滤 B.结晶 C.蒸馏 D.萃取B优化设计P9知识点2三离子的检验离子所加试剂现象离子方程式Cl-①AgNO3②稀HNO3产生不溶于稀硝酸的白色沉淀NaCl+AgNO3=AgCl↓+NaNO3SO42-①稀HCl②BaCl2滴加稀盐酸,无明显现象,再滴BaCl2溶液产生白色沉淀Na2SO4+BaCl2=BaSO4↓+2NaCl注意:每次应取少量进行;如:取少量待测溶液于试管中作业1:11(2)12思考:如何验证一种溶液可能是盐酸溶液?化学方法分离与提纯:1.四原则:不增(不引入新的杂质)、不减(不损耗样品)、易分(容易分离)、易复原(被提纯物质要分离)。2.除杂的思路:选择那些易与杂质反应时生成气体或沉淀的物质为试剂,然后再根据“不增”的原则确定加入试剂顺序。3.三必须:一除杂试剂必须过量;二过量试剂必须除尽(因为过量试剂带入新的杂质);三除杂途径选最佳。作业1:11(2)1.物质的量定义:表示含有一定数目粒子的集合体单位:摩尔,简称摩,符号mol符号:n对象:只适用于微观粒子;并用化学式指明粒子的种类;二化学计量在实验中的应用2.1mol物质所含粒子数的基准①与12g12C中所含C原子数相同②含有阿伏伽德罗常数(NA)个粒子③近似值6.02×1023/mol3.摩尔质量定义:单位物质的量(1mol)的物质所具有的质量符号:M单位:g/mol特点:在数值上等于该粒子的相对原子质量或相对分子质量4.气体摩尔体积定义:单位物质的量(1mol)的气体所占的体积符号:Vm单位:L/mol或L·mol-1定义:以单位体积溶液里所含溶质定义:以单位体积溶液里所含溶质BB的的物物质的量来表示溶液的组成的物理量质的量来表示溶液的组成的物理量单位:单位:mol/Lmol/L符号:符号:CCBB5.5.物质的量浓度物质的量浓度例题精选有一个空瓶质量为m1,该瓶充入空气后质量为m2。在相同状况下,若改为充入某气体A时,总质量为m3,则A的相对分子质量是()A29m2/m1B29m3/m1C29(m3-m1)/(m2-m1)D29(m2-m1)/(m3-m1)作业2:1c如果ag某气体中含有的分子数为b,则cg该气体在标准状况下占有的体积应表示为(式中NA为阿伏伽德罗常数)()A22.4bc/aNALB22.4ab/cNALC22.4bc/bNALD22.4b/acNALD关于气体摩尔体积(Vm)1.在标准状况下(273K,101KPa),1mol任何气体所占的体积都约是22.4L。2.温度和压强一定,1mol任何气体的体积相同(Vm相同)。3.气体摩尔体积与标准状况下气体摩尔体积22.4L/mol的关系?区分标准状况与常温常压标准状况:0℃,101KPa或273K,1.01×105Pa常温常压:25℃,101KPa或298K,1.01×105Pa影响物质体积的因素:微粒数目、微粒直径大小、粒子之间的平均距离物质因素粒子的数目粒子间平均距离粒子直径大小固、液态√气态√√√阿伏伽德罗定律(四同定律):1.同温同压下:相同体积的任何气体,都含有相同数目的粒子。2.不仅适用于单一气体,也适用于混合气体温度和压强一定,1mol任何气体的体积相同(Vm相等)。同温同压:,即气体的体积之比等于其物质的量之比,也等于其分子数之比气体的密度之比等于摩尔质量之比一定物质的量浓度溶液的配制①计算②称量(托盘天平)(量筒)③溶解(烧杯、玻璃棒)④转移和洗涤(容量瓶、玻璃棒)⑤定容(胶头滴管)⑥摇匀⑦装瓶贴签误差分析:下列操作使配制的溶液的浓度如何变化?配制步骤错误操作nVCB计算计算结果:m=5.85g,称5.9g称量砝码生锈(没有脱落)少量NaCl粘在滤纸上。被称量的物体错放在托盘天平右盘上溶解为促进溶解而加热,将热溶液转移至容量瓶中变大不变变大变大不变变大变小不变变小变小不变变小不变变小变大转移容量瓶使用前有少量水容量瓶使用前用标准液润洗除洗涤烧杯和玻璃棒外,还洗涤量筒转移溶液时有少量溶液或洗涤液洒在容量瓶外洗涤未洗涤溶解用的烧杯和玻璃棒或洗涤液未转入容量定容定容时仰视刻度超过刻度线,吸出一部分水摇匀摇匀后液面下降,补充水不变不变不变变大不变变大变大不变变大变小不变变小变小不变变小变大不变变小不变变小变小不变变大变小根据稀释前后溶质的物质的量不变:C(浓溶液)·V(浓溶液)=C(稀溶液)·V(稀溶液)物质的量浓度(c)与溶质的质量分数(w)之间的换算关系:。实验室里需要960ml0.1mol/L的硫酸铜溶液,以下操作正确的是()A.称取7.68g硫酸铜,加入1000ml水中B.称取12.0g胆矾配成1000ml溶液C.称取8.0g硫酸铜,加入1000ml水D.称取25g胆矾配成1000ml溶液D



















