





《酸和碱的化学性质PPT课件下载(共22页)》是由用户上传到老师板报网,本为文库资料,大小为861 KB,总共有22页,格式为ppt。授权方式为VIP用户下载,成为老师板报网VIP用户马上下载此课件。文件完整,下载后可编辑修改。
- 文库资料
- 22页
- 861 KB
- VIP模板
- ppt
- 数字产品不支持退货
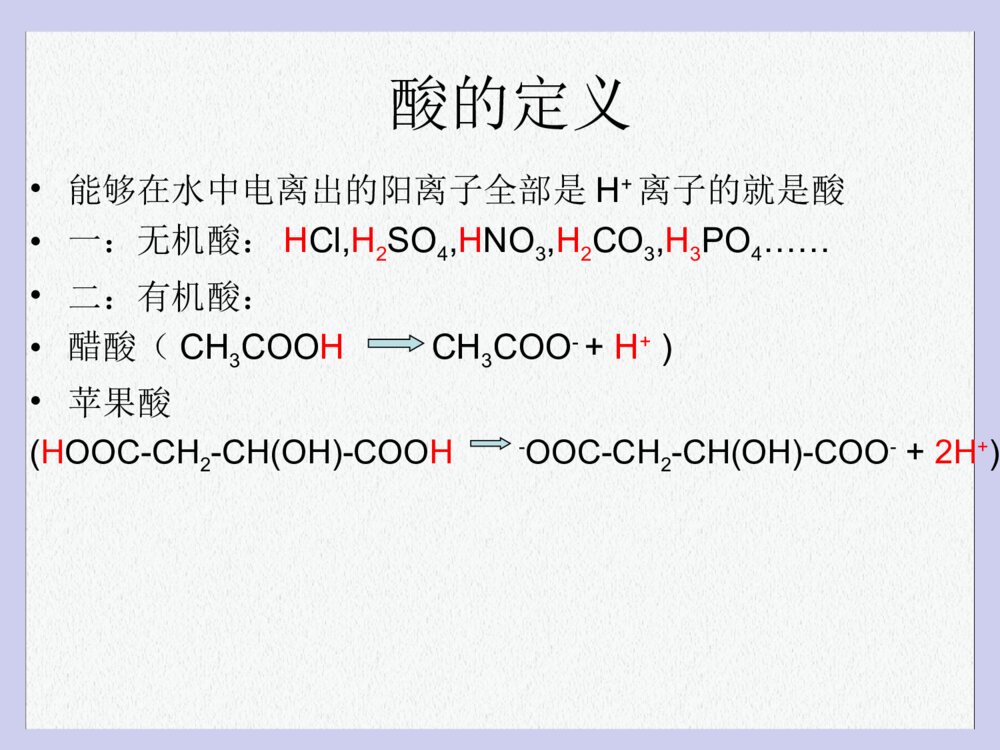
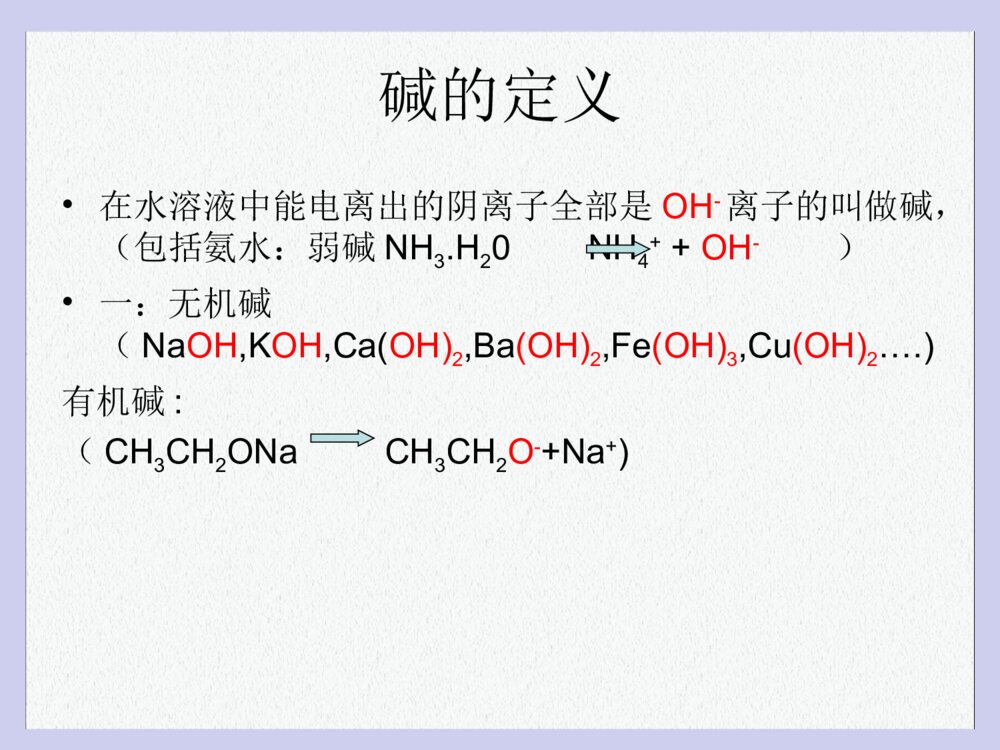
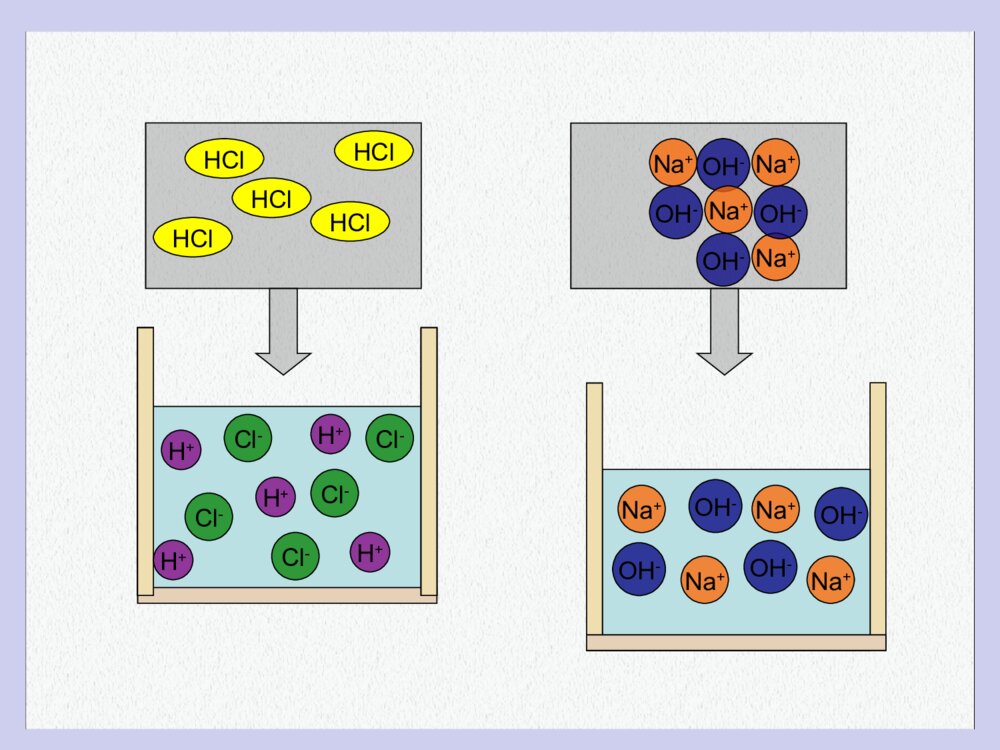
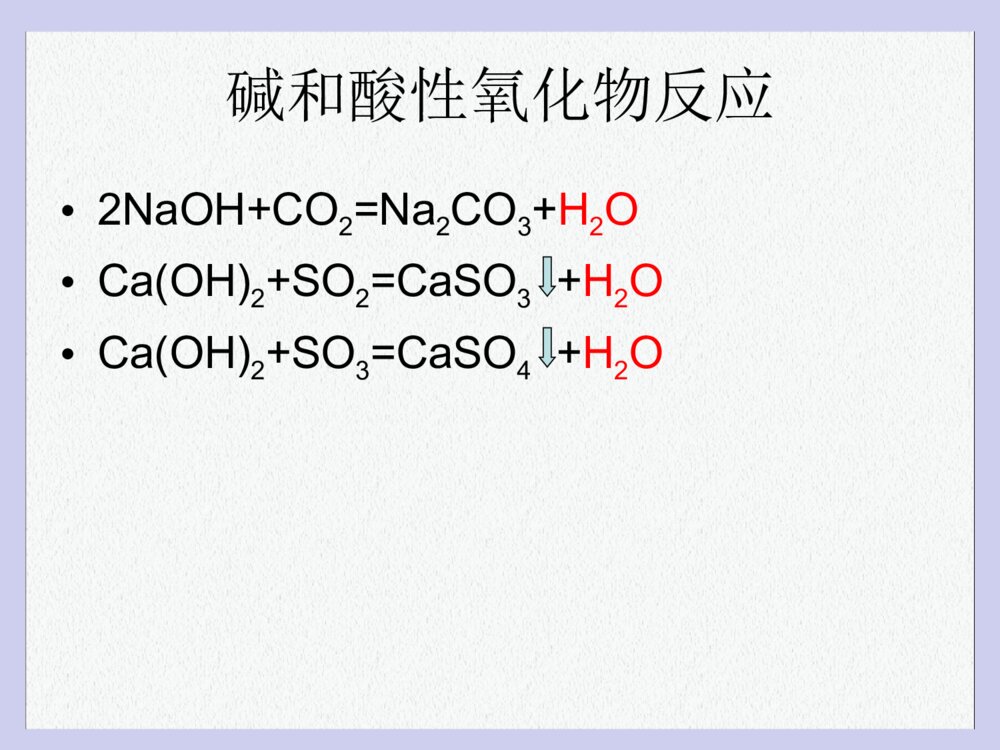
酸的定义•能够在水中电离出的阳离子全部是H+离子的就是酸•一:无机酸:HCl,H2SO4,HNO3,H2CO3,H3PO4……•二:有机酸:•醋酸(CH3COOHCH3COO-+H+)•苹果酸(HOOC-CH2-CH(OH)-COOH-OOC-CH2-CH(OH)-COO-+2H+)碱的定义•在水溶液中能电离出的阴离子全部是OH-离子的叫做碱,(包括氨水:弱碱NH3.H20NH4++OH-)•一:无机碱(NaOH,KOH,Ca(OH)2,Ba(OH)2,Fe(OH)3,Cu(OH)2….)有机碱:(CH3CH2ONaCH3CH2O-+Na+)盐的定义•盐属于离子化合物:盐由金属阳离子(和NH4+铵根离子)+酸根离子组成的离子化合物•金属阳离子:(Na+,Mg2+,K+,Ca2+.Fe3+,Fe2+,Cu2+,…..)以及(NH4+)•酸根阴离子:(Cl-,SO42-,CO32-,MnO4-,HCO3-,NO3-,PO43-......)HClHClHClHClHClCl-Cl-H+H+H+H+H+Cl-Cl-Cl-Na+OH-Na+Na+Na+Na+OH-OH-OH-OH-Na+Na+Na+OH-OH-OH-碱的化学性质•1,和酸性氧化物反应•2,和酸反应•3,和某些盐反应碱和酸反应:2NaOH+H2SO4=Na2SO4+2H2OCa(OH)2+2HCl=CaCl2+2H2OFe(OH)3+3HCl=FeCl3+3H2OCu(OH)2+H2SO4=CuSO4+2H2O2Al(OH)3+3H2SO4=Al2(SO4)3+6H2OCa(OH)2+H2CO3=CaCO3+2H2O碱和酸性氧化物反应•2NaOH+CO2=Na2CO3+H2O•Ca(OH)2+SO2=CaSO3+H2O•Ca(OH)2+SO3=CaSO4+H2O碱和某些盐反应•Ca(OH)2+Na2CO3=CaCO3+2NaOH•Ca(OH)2+CuSO4=CaSO4+Cu(OH)2•2NaOH+CuCl2=2NaCl+Cu(OH)2•2KOH+2NaHCO3=Na2CO3+K2CO3+2H2O•Ca(OH)2+2NH4Cl=CaCl2+2NH3+2H2O酸的化学性质•1,和大部分金属氧化物反应•2,和碱反应•3,和某些盐反应•4,和活泼金属反应酸(强酸)和活泼金属反应•2HCl+Zn=ZnCl2+H2•H2SO4+Fe=FeSO4+H2•2Al+3H2SO4=Al2(SO4)3+3H2•Mg+2HCl=MgCl2+H2酸和金属氧化物反应•2HCl+CaO=CaCl2+H2O•3H2SO4+Fe2O3=Fe2(SO4)3+6H2O•2HNO3+CuO=Cu(NO3)2+H2O•6HCl+2Al2O3=AlCl3+3H2O酸和某些盐反应•H2SO4+CaCO3=CaSO4+CO2+H2O•2HCl+Na2CO3=NaCl+CO2+H2O•HCl+AgNO3=HNO3+AgCl•H2SO4+2NaHCO3=Na2SO4+2CO2+2H2O一、酸的名称与化学式盐酸硫酸碳酸硝酸HClH2SO4H2CO3HNO3一、碱的名称与化学式氢氧化钠氢氧化钙氢氧化铜氢氧化铁氢氧化钾NaOHCa(OH)2Cu(OH)2Fe(OH)3KOH溶液的颜色含Fe3+的溶液是黄色含Fe2+的溶液是浅绿色含Cu2+的溶液蓝色动画演示加深印象。点拔:水的密度较小,浮在浓硫酸上面,溶解时放出大量热,使水立刻沸腾,使硫酸液滴向四周飞溅,这是非常危险的。讨论:打开瓶塞,久置于空气中的浓硫酸会有什么变化?交流:敞口放置在空气中的浓硫酸质量会增加,同时溶质的质量分数会减少。浓硫酸的特性•吸水性(干燥剂:O2、H2、N2、CO2、CO)(NH3不行)•强烈的腐蚀性打开瓶塞,久置于空气中的浓盐酸会有什么变化?思考交流:敞口放置在空气中的浓盐酸质量会减少,同时溶质的质量分数会减少。酸•强酸:(在水溶液中全部电离)H2SO4硫酸,HCl盐酸,HNO3硝酸,HClO4高氯酸等,它们在水溶液中彻底电离出(H+离子与酸根离子)•弱酸:(在水溶液中存在着电离平衡,即不能全部电解)碳酸,醋酸等属于弱酸。H2CO3H++HCO3-2H++CO32-盐•强酸强碱盐(即金属氧离子和酸根离子都不会水解)Na2SO4,KCl,Ba(NO3)2,KBr•强碱弱酸盐(酸根离子会水解)呈碱性CO32-+H2OHCO3-+OH-HCO3-+H2OH2CO3+OH-•弱碱强酸盐(金属离子会水解,或者铵根离子会水解)呈酸性NH4++H2ONH3.H2O+H+一般花瓣内通常含有两种色素。这些色素在不同的温度、不同的酸碱性环境下,呈现不同的颜色。不同的花,花瓣中两种色素的含量不同,由于花瓣内的酸碱性不同,因此花会呈现不同的颜色。同一种花,在开放的不同时期,花瓣中两种色素的含量不同,花瓣内的酸碱性不同,花也呈现不同的颜色。这就有“百花盛开,万紫千红”美丽景观的描绘。花的颜色



















