








《《气体摩尔体积》高一化学PPT课件》是由用户上传到老师板报网,本为文库资料,大小为286.5 KB,总共有12页,格式为ppt。授权方式为VIP用户下载,成为老师板报网VIP用户马上下载此课件。文件完整,下载后可编辑修改。
- 文库资料
- 12页
- 286.5 KB
- VIP模板
- ppt
- 数字产品不支持退货
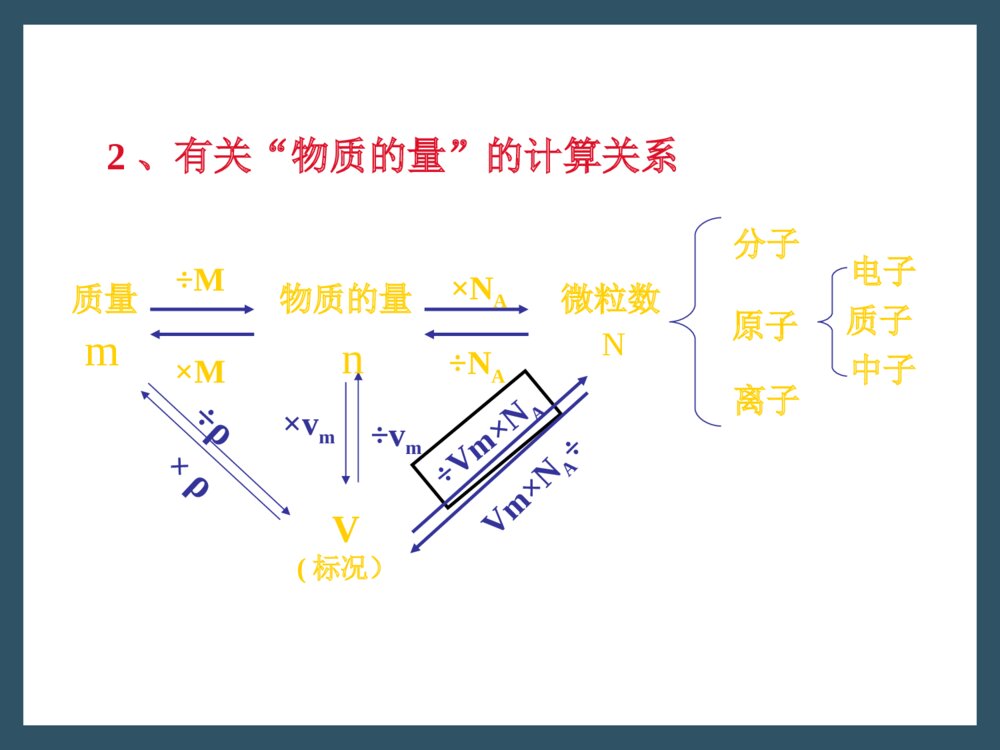
第二节气体摩尔体积(二)1.求S.T.P下的V①V=m/ρ②V=n×VmV=m/M×VmV=N/NA×Vm练习一1、每升天然水中通入0.002克氯气就达到消毒作用,可供饮用。0.002克氯气在标准状况下的体积为______mL。2、在相同的温度和压强下,下列气体密度最少的是:(A)、CO2(B)、H2(C)、O2(D)、Cl23、设阿伏加德罗常数为NA,标准状况下某种O2和N2的混合气体m克含有b个分子,则n克该混合气体在相同状况下所占的体积(L)应是:(A)、22.4nb/(mNA)(B)、22.4mb/(nNA)(C)、22.4nNA/(mb)(D)、nbNA/(22.4m)V(标况)÷vm×vm÷Vm×NAVm×NA÷分子离子电子原子质量物质的量微粒数质子中子÷M×M×NA÷NAmnN÷ρ×ρ2、有关“物质的量”的计算关系练习二1、在标准状况下氢气和一氧化碳的混合气体7升,质量为2.25克,求氢气和一氧化碳的质量分数和体积分数。2、将mA克锌加到mB克20%的盐酸溶液中去,反应结果共放出n升氢气(在标准状况下),则被还原的HCl的物质的量是:(A)、mA/65mol(B)、5mB/36.5mol(C)、mB/36.5mol(D)、n/11.2mol3、阿伏加德罗定律(1)、在相同的温度和压强下,相同体积的任何气体都含有相同数目的分子(2)、推论:(仅适用于气体)①、同温同压下,气体的体积与物质的量成正比;②、同温同体积下,气体的压强与物质的量成正比;③、同温同压下,气体的密度与相对分子质量成正比;练习三1、在标准状况下,等质量的CH4和CO比较,下列说法正确的是:(A)、密度之比为4:7(B)、分子数之比为4:7(C)、体积之比为7:4(D)、物质的量之比为:4:72、在标准状况下,m克气体A和n克气体B的分子数相同,下列说法中不正确的是:(A)、气体A与B的相对分子质量比为m:n(B)、同质量气体A与B的分子个数比为n:m(C)、同温同压下,A气体与B气体的密度比为n:m(D)、相同状况下,同体积的A气体与B气体质量比为m:n3、两个体积相同的容器,一个盛有NO,另一个盛有N2和O2,在同温同压下,两容器内的气体一定具有相同的:(A)、原子总数(B)、质子总数(C)、分子总数(D)、质量4、同温同压下,某容器充满O2重116克,若充满CO2重122克,现充满某气体X重114克,则该气体的相对分子质量为:(A)、28(B)、60(C)、32(D)、445、在一定的温度和压强下,1体积的A2气体和3体积的B2气体化合成2体积的C气体,则C的化学式为:(A)、AB3(B)、AB(C)、A3B(D)、A2B34、平均摩尔质量及其求算方法(1)、平均摩尔质量的定义:(2)、求算方法:①、M(混)=m(混)/n(混)②、已知标准状况下混合气体的密度[ρ(混)],则M(混)=22.4L/mol×ρ(混)③、已知同温同压下,则ρ(混)/ρ(A)=M(混)/M(A)=d(相对密度)④、已知混合物各成分的摩尔质量和在混合体系内的物质的量的分数或体积分数(对气体),则M(混)=M(A)×A%+M(B)×B%+M(C)×C%练习四1、由CH4和CO组成的混合气体,测得在标准状况下其密度为1克/升,则该混合气体中CH4和CO的质量比约是:(A)、1:1(B)、1:2(C)、2:3(D)、7:82、已知某混合气体的成分按体积分数计算是:80.0%CH4、15.0%C2H4和5.00%C2H6。试计算:(1)、0.500mol该混合气体的质量。(2)、该混合气体在标准状况下的密度。



















