







《高中化学 第三节 化学键PPT课件下载》是由用户上传到老师板报网,本为文库资料,大小为767 KB,总共有16页,格式为ppt。授权方式为VIP用户下载,成为老师板报网VIP用户马上下载此课件。文件完整,下载后可编辑修改。
- 文库资料
- 16页
- 767 KB
- VIP模板
- ppt
- 数字产品不支持退货
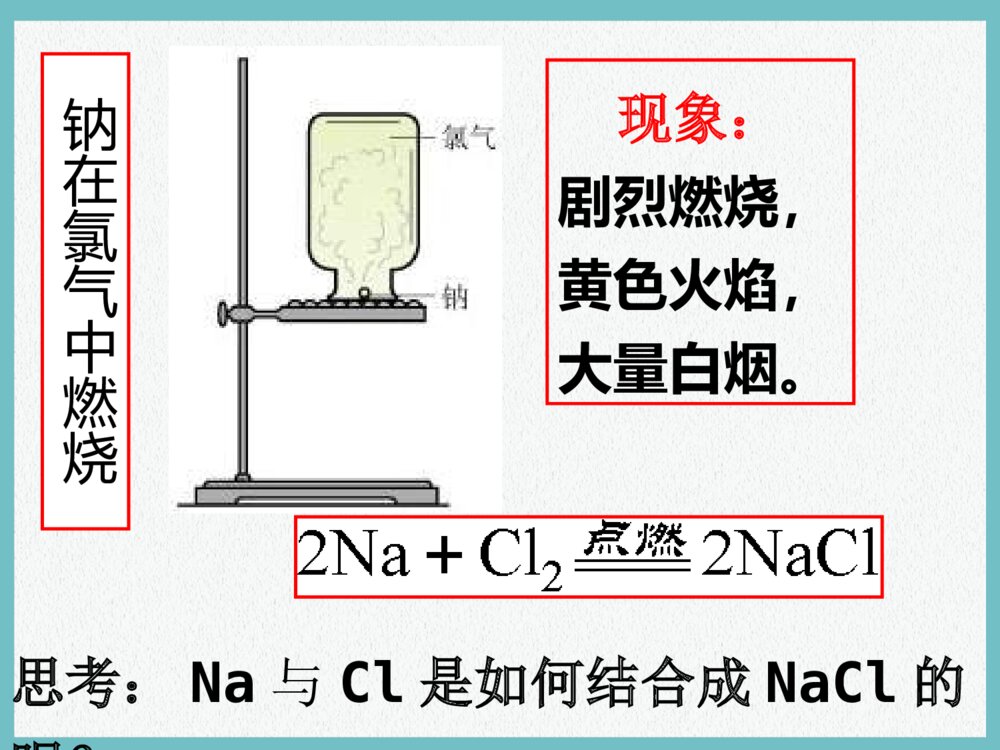
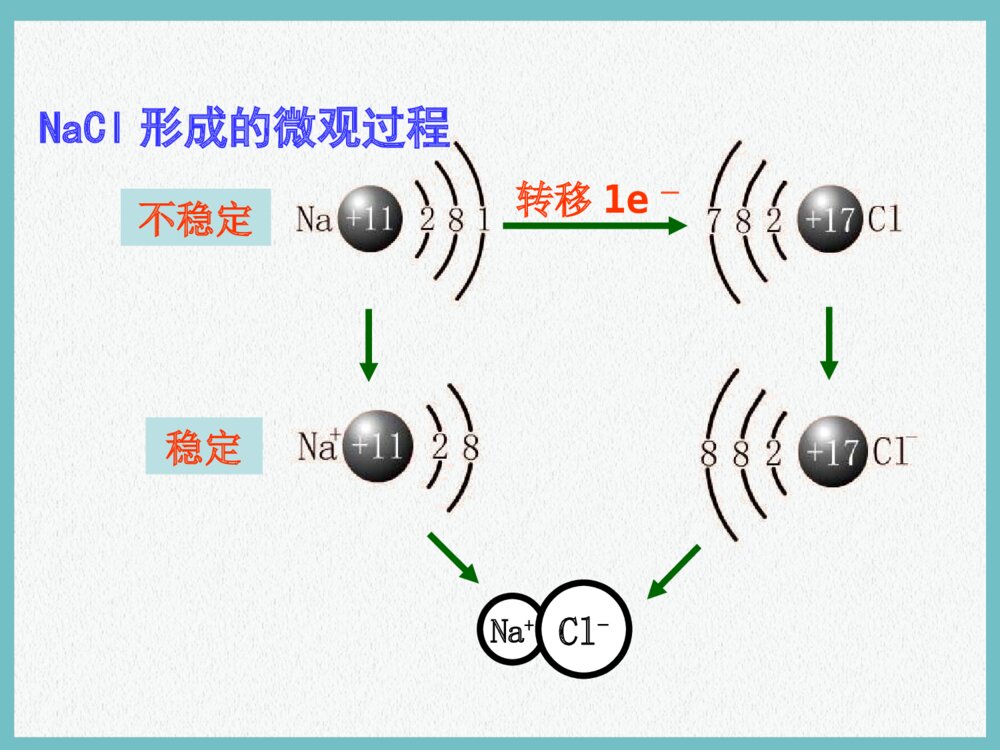
第三节化学键你想过吗?1.为什么一百多种元素可形成千千万万种物质?2.化合物中原子为什么总是按一定数目相结合?1.概念要点:a.相邻b.原子之间c.强烈作用——相邻的原子之间强烈的相互作用2.化学键主要类型:a.离子键b.共价键化学键钠在氯气中燃烧现象:剧烈燃烧,黄色火焰,大量白烟。思考:Na与Cl是如何结合成NaCl的呢?Na+Cl-转移1e-不稳定稳定NaCl形成的微观过程1.定义:象Na+与Cl-之间,带相反电荷离子之间的相互作用称为离子键。一、离子键4.离子化合物:由离子键构成的化合物阴、阳离子静电引力2.构成离子键的粒子:3.作用力:静电作用斥力思考哪些物质属于离子化合物,含有离子键?活泼的金属元素(IA,IIA)和活泼的非金属元素(VIA,VIIA)之间形成的化合物。强碱、常见金属氧化物、常见的盐:如:KCl、Na2O、MgCl2等如:NaOH、MgO、Na2O2、K2SO4、NH4Cl等在元素符号周围用“·”或“×”来表示原子最外层电子的式子。5、电子式:H·Na··Mg··O·····Cl·······(1)原子的电子式:(2)离子的电子式:H+Na+Mg2+[O]2-····::[Cl]-····::①金属阳离子的电子式就是其离子符号。②阴离子的电子式要标[]及“电荷数”。(3)离子化合物的电子式:③离子化合物的电子式就是由阴、阳离子的电子式合并而成。写出下列粒子的电子式:硫原子,溴离子,钾离子·S·····[Br]-····::K+氯化钠氟化镁Na+[Cl]-····::[F]-····::Mg2+[F]-····::(4)离子化合物的形成过程用电子式表示氯化钠的形成过程用电子式表示溴化钙的形成过程Cl·······Na·+→[Cl]-····::Na+Br·····:·Ca·Br·····:++→Ca2+[Br]-····::[Br]-····::[练习]⑴用电子式表示氧化镁的形成过程⑵用电子式表示硫化钾的形成过程箭头左方相同的原子可以合并箭头右方相同的微粒不可以合并注意·O·····[O]2-····::·Mg·+→Mg2+·S·····2K·+→K+[S]2-····::K+不能把“→”写成“=”由离子键构成的化合物一定是离子化合物区分:用电子式表示物质用电子式表示物质形成过程练习:下列各数值表示有关元素的原子序数,其所表示的各原子组中能以离子键相互结合成稳定化合物的是:A.10与12B.8与17C.11与17D.6与14C



















